Зачем эритроцитам двояковогнутая форма
Цельная кровь состоит из жидкой части (плазмы) и форменных элементов, к которым относят эритроциты, лейкоциты и кровяные пластинки — тромбоциты.
Функции крови:
1) транспортная — перенос газов (02 и С02), пластических (аминокислот, нуклеозидов, витаминов, минеральных веществ), энергетических (глюкоза, жиры) ресурсов к тканям, а конечных продуктов обмена — к органам выделения (желудочно-кишечный тракт, легкие, почки, потовые железы, кожа);
2) гомеостатическая — поддержание температуры тела, кислотно-основного состояния организма, водно-солевого обмена, тканевого гомеостаза и регенерации тканей;
3) защитная — обеспечение иммунных реакций, кровяного и тканевого барьеров против инфекции;
4) регуляторная — гуморальной и гормональной регуляции функций различньгх систем и тканей;
5) секреторная — образование клетками крови биологически активных веществ.
Функции и свойства эритроцитов
Эритроциты переносят 02 содержащимся в них гемоглобином от легких к тканям и С02 от тканей к альвеолам легких. Функции эритроцитов обусловлены высоким содержанием гемоглобина (95 % массы эритроцита), деформируемостью цитоскелета, благодаря чему эритроциты легко проникают через капилляры с диаметром меньше 3 мкм, хотя имеют диаметр от 7 до 8 мкм. Глюкоза является основным источником энергии в эритроците. Восстановление формы деформированного в капилляре эритроцита, активный мембранный транспорт катионов через мембрану эритроцита, синтез глютатиона обеспечиваются за счет энергии анаэробного гликолиза в цикле Эмбдена—Мейергофа. В ходе метаболизма глюкозы, протекающего в эритроците по побочному пути гликолиза, контролируемого ферментом дифосфоглицератмутазой, в эритроците образуется 2,3-дифосфоглицерат (2,3-ДФГ). Основное значение 2,3-ДФГ заключается в уменьшении сродства гемоглобина к кислороду.
В цикле Эмбдена—Мейергофа расходуется 90 % потребляемой эритроцитами глюкозы. Торможение гликолиза, возникающее, например, при старении эритроцита и уменьшающее в эритроците концентрацию АТФ, приводит к накоплению в ней ионов натрия и воды, ионов кальция, повреждению мембраны, что понижает механическую и осмотическую устойчивость эритроцита, и стареющий эритроцит разрушается. Энергия глюкозы в эритроците используется также в реакциях восстановления, защищающих компоненты эритроцита от окислительной денатурации, которая нарушает их функцию. Благодаря реакциям восстановления атомы железа гемоглобина поддерживаются в восстановленной, т. е. двухвалентной форме, что препятствует превращению гемоглобина в метгемоглобин, в котором железо окислено до трехвалентного, вследствие чего метгемоглобин неспособен к транспорту кислорода. Восстановление окисленного железа метгемоглобина до двухвалентного обеспечивается ферментом — метгемоглобинредуктазой. В восстановленном состоянии поддерживаются и серусодержащие группы, входящие в мембрану эритроцита, гемоглобин, ферменты, что сохраняет функциональные свойства этих структур.
Цикл Эмбден-Мейергоффа эритроцитов 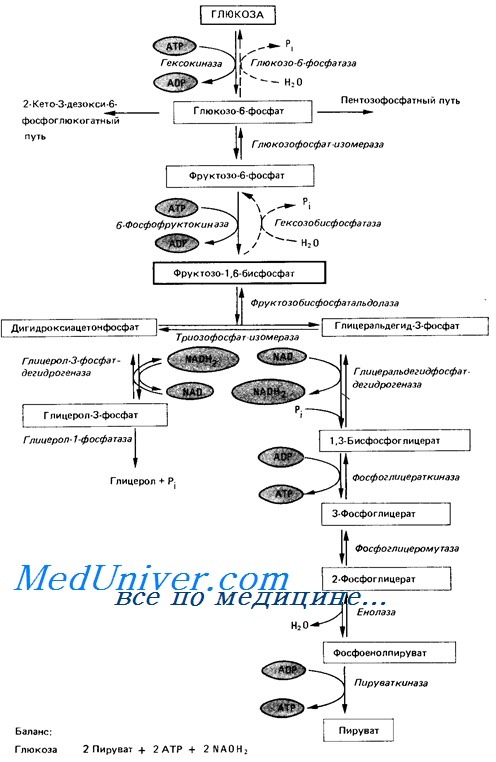
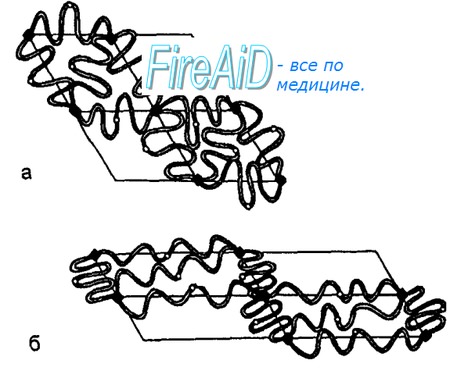
Эритроциты имеют дисковидную, двояковогнутую форму, их поверхность — около 145 мкм2, а объем достигает 85—90 мкм3. Такое соотношение площади к объему способствует деформабильно-сти (под последней понимают способность эритроцитов к обратимым изменениям размеров и формы) эритроцитов при их прохождении через капилляры. Форма и деформабильность эритроцитов поддерживаются липидами мембран — фосфолипидами (глицерофосфолипидами, сфинголипидами, фосфотидилэтаноламином, фосфатидилсирином и др.), гликолипидами и холестерином, а также белками их цитоскелета. В состав цитоскелета мембраны эритроцита входят белки — спектрин (основной белок цитоскелета), анкирин, актин, белки полосы 4.1, 4.2, 4.9, тропомиозин, тропомодулин, адцуцин. Основой мембраны эритроцита является липидный бислой, пронизанный интегральными белками цитоскелета — гликопротеинами и белком полосы 3. Последние связаны с частью белковой сети цитоскелета — комплексом спектрин—актин—белок полосы 4.1, локализованным на цитоплазматической поверхности липидного бислоя мембраны эритроцита (рис. 7.1).
Взаимодействие белкового цитоскелета с липидным бислоем мембраны обеспечивает стабильность структуры эритроцита, поведение эритроцита как упругого твердого тела при его деформации. Нековалентные межмолекулярные взаимодействия белков цитоскелета легко обеспечивают изменение размеров и формы эритроцитов (их деформацию) при прохождении этих клеток через микроциркуляторное русло, при выходе ретикулоцитов из костного мозга в кровь — благодаря изменению расположения молекул спектрина на внутренней поверхности липидного бислоя. Генетические аномалии белков цитоскелета у человека сопровождаются появлением дефектов мембраны эритроцитов. В результате последние приобретают измененную форму (так называемые сфероциты, элиптоциты и др.) и имеют повышенную склонность к гемолизу. Увеличение соотношения холестерин—фосфолипиды в мембране увеличивает ее вязкость, уменьшает текучесть и эластичность мембраны эритроцита. В результате снижается деформируемость эритроцита. Усиление окисления ненасыщенных жирных кислот фосфолипидов мембраны перекисью водорода или супероксидными радикалами вызывает гемолиз эритроцитов (разрушение эритроцитов с выходом гемоглобина в окружающую среду), повреждение молекулы гемоглобина эритроцита. Постоянно образующийся в эритроците глютатион, а также антиоксиданты (остокоферол), ферменты — глутатионредуктаза, супероксиддисмутаза и др. защищают компоненты эритроцита от этого повреждения.
До 52 % массы мембраны эритроцитов составляют белки гликопротеины, которые с олигосахаридами образуют антигены групп крови. Глико-протеины мембраны содержат сиаловую кислоту, которая придает отрицательный заряд эритроцитам, отталкивающий их друг от друга.
Энзимы мембраны — Ка+/К+-зависимая АТФаза обеспечивает активный транспорт Na+ из эритроцита и К+ в его цитоплазму. Са2+-зависимая АТФаза выводит Са2+ из эритроцита. Фермент эритроцита карбоангидраза катализирует реакцию: Са2+ Н20 Н2С03 о Н+ + НСО3, поэтому эритроцит транспортирует часть углекислого газа от тканей к легким в виде бикарбоната, до 30 % С02 переносится гемоглобином эритроцитов в форме карбаминового соединения с радикалом NH2 глобина.
Зачем эритроцитам двояковогнутая форма
Эритропоэз и механизмы его регуляции
В эмбриональном периоде кроветворение осуществляется вначале в кровяных островках желточного мешка, затем примерно спустя 5 недель эмбрионального развития – в печени. Селезенка включается в процесс кроветворения с 16 недели внутриутробного развития. Первые гемопоэтические элементы появляются в костном мозге на 2-ом месяце эмбрионального развития, однако миелоидный период кроветворения начинается на 4-5-м месяцах эмбрионального развития, вытесняя постепенно кроветворение в печени и селезенке. Костномозговой эритропоэз осуществляется вне синусов, в строме костного мозга, то есть эктраваскуляторно. К моменту рождения ребенка костный мозг развивается полностью, а экстрамедуллярное кроветворение практически завершается. Постэмбриональный период кроветворения начинается после рождения ребенка и продолжается на протяжении всей жизни. Гемопоэз осуществляется в специализированных гемопоэтических тканях: миелоидной (эпифизы трубчатых костей и полости многих губчатых костей) и лимфоидной (тимус, селезенка, лимфатические узлы). В миелоидной ткани образуются эритроциты, лейкоциты, тромбоциты. В лимфоидной ткани идет дальнейшая дифференцировка и созревание лимфоцитов, а также плазматических клеток – основных продуцентов антител.
Постэмбриональный гемопоэз обеспечивает процессы физиологической регенерации крови, то есть её обновление, что компенсирует физиологические процессы разрушения дифференцированных клеток крови.
В условиях нормы функциональная активность органов кроветворения и кроверазрушения строго сбалансирована, что обеспечивает относительное постоянство содержания эритроцитов и других клеток в периферической крови. Разрушение эритроцитов происходит примерно после 120-дневного пребывания их в системной циркуляции при участии тканевых макрофагов селезенки, лимфатических узлов, печени. Гемоглобин, освобождающийся в процессе распада эритроцитов, трансформируется в билирубин в клетках моноцитарно-макрофагальной системы, а затем в гембилирубин (непрямой билирубин), вступая во взаимодействие с белками крови или липопротеидами. Гембилирубин в свою очередь элиминируется из системного кровотока печеночными клетками, где превращается в прямой билирубин (соединение билирубина с глюкуроновой кислотой). Прямой билирубин вместе с желчью поступает в кишечник, постепенно превращается в другие желчные пигменты (стеркобилиноген, уробилиноген) которые, выделяясь с калом и мочой, придают им окраску. При внутриклеточном разрушении эритроцитов основным продуктом, образующимся после распада гемоглобина, является билирубин, а при внутрисосудистом гемолизе большие количества гемоглобина соединяются с α2-гликопротеином-гаптоглобином, который не проникает в мочу.
Основным регулятором эритропоэза является эритропоэтин – гликопротеид, интенсивно вырабатывающийся в условиях гипоксии. При гипоксических состояниях различного генеза концентрация эритропоэтина возрастает в десятки раз по сравнению с нормой. Основным источником синтеза эритропоэтина являются почки (до 90 %), печень (около 10 %), а также макрофаги костного мозга и селезенки. Для эритропоэтина характерен мембранный тип рецепции эритропоэтинчувствительными клетками костного мозга с последующими активацией митоза и дифференцировки клеток, в частности, стимуляцией транспорта железа в эритрокариоцитах, синтеза цепей глобина, ферментов образования гема, синтеза мембранных белков и эритроцитарных антигенов.
Эритропоэз стимулируется под влиянием катехоламинов, глюкокортикоидов, андрогенов, гормонов щитовидной железы, инсулина, плацентарного пролактина, ИЛ-3, ИЛ-6, ИЛ-9, ИЛ-11, КСФ, фолиевой кислоты, витаминов С, В12, железосодержащих препаратов.
Эритропоэз угнетается при повышенной оксигенации тканей, когда снижается образование эритропоэтина, а также под влиянием эстрогенов, глюкагона, ацетилхолина, интерферонов, ФНО-а, ИЛ-1, ИЛ-5, эритроцитарных кейлонов.
После рождения у ребенка в течение нескольких дней отмечают эритроцитоз – содержание эритроцитов составляет 5,5⋅1012/л, в то же время имеется высокое содержание гемоглобина (156-200 г/л). В течение первого года жизни изменяется антигенная структура эритроцитов, возникает прогрессирующее снижение фетального гемоглобина. К концу первого года жизни содержание фетального гемоглобина не превышает 1 %.
Общая характеристика эритроцитов
Эритроциты – самая многочисленная популяция клеток крови, обладающих разнообразными функциями, в частности дыхательной, трофической, детоксицирующей. Количество эритроцитов довольно вариабельно в условиях нормы: так, у женщин оно колеблется от 3,7⋅1012/л до 4,7⋅1012 /л, а у мужчин – от 4,5⋅1012/л до 5,5⋅1012 /л. Сдвиг этих показателей до нижней или верхней границы нормы может быть одним из признаков болезни.
Около 85 % всех эритроцитов имеют форму двояковогнутого диска, то есть являются дискоцитами. Форма эритроцита определяет цепь ауторегулирующих процессов, направленных на поддержание движения крови, её реологических свойств. В условиях патологии появляются эритроциты различной формы, такие состояния именуют пойкилоцитозом. Среди аномальных по форме эритроцитов различают овалоциты, аннулоциты, сфероциты, акантоциты, стоматоциты, щизоциты и другие формы, имеющие в ряде случаев определённое диагностическое значение.
Обычная в условиях нормы форма дискоцита значительно увеличивает площадь диффузии газов, электролитов и других субстратов. Средний диаметр эритроцита (нормоцита) в области краёв составляет 7,5 мкм, а максимальная толщина эритроцита в области краёв составляет 2 мкм. Эритроциты с диаметром от 2 до 6 мкм – микроциты, а с диаметром от 9 до 16 мкм – макроциты. Количество макро- и микроцитов в крови здорового человека в среднем составляет 15–20 %. Резкое увеличение содержания в крови микро- и макроцитов, именуемое анизоцитозом, является одним из признаков нарушения гемопоэза, характерным для анемий, лейкоцитозов, заболеваний инфекционно-аллергической природы. За время свой жизни в периферической крови эритроцит совершает кругооборот более 1 млн. раз, что вызывает развитие механических и метаболических изменений в эритроцитах. Эритроциты обладают пластичностью, то есть способностью к деформации при прохождении через узкие извитые капилляры диаметром 2,5–7,5 мкм. По мере старения их способность к деформации снижается, они застревают в капиллярах красной пульпы селезенки и там разрушаются в процессе фагоцитоза тканевыми макрофагами. Эластичность эритроцитов определяется особенностями структуры белка спектрина, гемоглобина, а также соотношением различных фракций липидов в мембране клеток.
Эритроциты играют важную роль в регуляции кислотно-основного состояния организма, в процессах свертывания крови и фибринолиза за счет адсорбции на их мембране разнообразных ферментных факторов этих систем. Эритроциты являются регуляторами водно-солевого обмена в связи со способностью депонировать воду и минеральные соли при нахождении их в венозной крови. Одной из главных функций эритроцитов является участие в иммунологических реакциях организма за счет наличия в мембранах эритроцитов комплекса полисахаридо-аминокислотных соединений, обладающих свойствами антигенов. Следует помнить, что суммарный объем эритроцитов приблизительно в 160 раз превышает таковой лейкоцитов и тромбоцитов, а потому кровь можно рассматривать как двухфазную систему, представляющую собой взвесь (суспензию) эритроцитов в плазме. При этом эритроцит подвергается в токе крови действию напряжения сдвига – оно более значительно у края и направлено в сторону стенки и менее выражено в центре сосуда. Разница действующих векторов силы у разных краёв обеспечивает вращательное движение эритроцитов в текущей жидкости, что при столкновении с тромбоцитами, имеющими меньший размер и худшую деформируемость по сравнению с эритроцитами, приводит к отбрасыванию кровяных пластинок к стенке сосуда. Благодаря этому пристеночный слой оказывается обогащенным тромбоцитами. Указанный эффект обусловлен величиной гематокрита, размером эритроцитов и тромбоцитов и ригидностью их мембран. Увеличение любого из указанных параметров сопровождается усилением передвижения кровяных пластинок к стенке сосуда, а при наличии повреждения эндотелия – адгезией к субэндотелию.
Буферные свойства эритроцитов. Как известно, на единицу объема эритроцит связывает в 60 раз большее количество О2, чем плазма крови. О2 хорошо растворим в воде, поэтому диффузия его в растворе происходит очень быстро. Связывание О2 с эритроцитами определяется парциальным давлением газа в плазме и сорбционными свойствами Нв. В капиллярах легких, где давление О2 высоко (рО2 = 133 гПа), высоко и сродство Нв к О2, что обеспечивает трансмембранный перенос газа и связывание его с гемоглобином. В капиллярах тканей, где рО2 равно 40-50 гПа, сродство Нв к О2 резко снижается. При этом происходит выход кислорода из эритроцитов.
Транспорт СО2 через мембрану эритроцита также осуществляется за счет диффузного давления (в капиллярах легких рСО2 = 53гПа, а в капиллярах тканей – 61 гПа). Диффузия СО2 в растворах происходит примерно в 20 раз быстрее, чем О2.
Высокая скорость равновесия содержания СО2 в системе эритроцит – плазма крови обеспечивается наличием в эритроцитах особого фермента – карбоангидразы, катализирующего реакции трансформации СО2 и Н2О в углекислоту (Н2СО3), а также мощными системами трансмембранного обмена анионами.
При понижении концентрации СО2 в эритроцитах возникает отрицательный заряд Нв, что приводит к уменьшению содержания внутриклеточной воды, а при увеличении содержания СО2 в эритроцитах – они набухают.
Известно, что осмотическое давление в эритроцитах несколько выше, чем в плазме крови, что связанно с высокой внутриклеточной концентрацией белков по сравнению с плазмой крови. При этом содержание низкомолекулярных осмотически активных веществ (ионов натрия) в эритроцитах значительно меньше, чем в плазме крови. Величина осмотического давления в эритроцитах обеспечивает достаточный или нормальный тургор этих клеток. Осмотическое давление плазмы и эритроцитов в условиях нормы находится в динамическом равновесии, что обуславливает стабильность структуры эритроцитов.
При помещении эритроцитов в коллоидно-осмотическую среду с более низким осмотическим давлением (гипотонические растворы) может наступить осмотический или коллоидно-осмотический гемолиз. Последний обусловлен тем, что вода поступает в эритроциты до того момента, пока не разрывается мембрана и гемоглобин выходит в окружающую среду.
В умеренногипотонической среде эритроциты приобретают сферическую форму, их называют в связи с этим сфероцитами. Способность эритроцитов сохранять свою структуру при развитии гипоосмотических состояний или в гипоосмотической среде получила название осмотической устойчивости, или резистентности эритроцитов. Верхняя граница резистентности или максимальная устойчивость эритроцитов соответствует примерно 0,5–0,4 % раствора хлорида натрия.
При помещении эритроцитов в гипертоническую среду происходит их сморщивание в связи с потерей воды и уменьшением объема.
Эритроцитам свойственна способность к оседанию. Удельная масса цельной крови в норме для взрослого составляет в среднем 1,05–1,06. Удельная масса эритроцитов (1,085–1,096) выше, чем плазмы крови (1,02–1,027), поэтому эритроциты в пробирке с кровью, лишенной возможности свертываться, способны медленно оседать на дно. Скорость оседания эритроцитов в значительной мере определяется белковым составом плазмы крови, в частности уровнем мелкодисперсных белков-альбуминов. В связи с этим важная роль в обеспечении величины СОЭ отводится соотношению альбуминово-глобулиновых фракций белков крови. СОЭ у мужчин в среднем составляет 1–10 мм/ч, у небеременных женщин 2-15 мм/ч. При некоторых патологических процессах и заболеваниях, а также во второй половине беременности СОЭ повышается, так как увеличивается содержание в крови грубодисперсных белков глобулиновой фракции, получивших название аггломеринов, а также за счет усиления образования фибриногена.
При замедлении скорости кровотока и повышении вязкости крови эритроциты проявляют способность к агрегации. Вначале агрегация носит обратимый характер, при этом образуются ложные агрегаты, или монетные столбики. В случае быстрого восстановления кровотока они распадаются на полноценные клетки с сохраненной мембраной и внутриклеточной структурой.
Пластичность или деформируемость – это способность эритроцитов к обратимой деформации при прохождении через узкие извитые капилляры, микропоры. Данное свойство определяется особенностями структуры мембраны эритроциты, наличием в ней особого белка спектрина.
Таким образом, основными физиологическими и физико-химическими свойствами эритроцитов являются следующие:
– способность к оседанию;
– способность к агрегации;
– деструкция после определенного периода циркуляции в кровотоке.
1. Дыхательная функция заключается в захвате и переносе кислорода к тканям и экскреции СО2 из организма. Это обеспечивается содержащимся в эритроцитах белком гемоглобином. Гемоглобин – сложный белок состоит из групп гема и белкового остатка – глобина. Содержание гемоглобина у мужчин составляет 130-160 г/л, у женщин 120-140 г/л.
2. Трофическая функция эритроцитов связана с их способностью транспортировать аминокислоты, нуклеотиды, пептиды к различным органам и тканям, способствуя обеспечению репаративных процессов. В ряде случаев эту функцию называют транспортной.
3. Детоксиксицирующая функция эритроцитов обусловлена их способностью адсорбировать токсические продукты эндогенного или экзогенного происхождения и частично инактивировать их.
4. Участие в процессах свертывания крови за счет адсорбции на их мембране плазменных факторов свертывания крови
5. Участие в регуляции кислотно-основного состояния организма (буферная функция) за счет гемоглобина обеспечивающего до 70 % буферной ёмкости крови.
6.– Ферментативная функция связана с наличием в эритроцитах большого количества ферментов, в частности карбоангидразы, метгемоглобинредуктазы, ферментов гликолиза.
Биохимия крови
| Сайт: | Образовательный портал МБФ (ВолгГМУ) |
| Курс: | Нарушения метаболизма. Биохимия специализированных тканей. (Для клин.ордов КЛД) |
| Книга: | Биохимия крови |
Оглавление
1. Общие сведения
2. свойства крови
3. Состав крови. Гематокрит
3.1. Плазма крови
Пла́зма кро́ви (от греч. πλάσμα — нечто сформированное, образованное) — жидкая часть крови, в которой взвешены форменные элементы — вторая часть крови. Процентное содержание плазмы в крови составляет 52—61 %. Макроскопически представляет собой однородную несколько мутную (иногда почти прозрачную) желтоватую жидкость, собирающуюся в верхней части сосуда с кровью после осаждения форменных элементов. Гистологически плазма является межклеточным веществом жидкой ткани крови.
Центрифуги-сепараторы выделяют из крови плазму. Плазма крови состоит из воды, в которой растворены вещества — белки (7—8 % от массы плазмы) и другие органические и минеральные соединения. Основными белками плазмы являются альбумины — 55—65 %, α1-глобулины — 2—4 %, α2-глобулины 6—12 %, β-глобулины8 — 12 %, γ-глобулины — 2-4 % и фибриноген — 0,2—0,4 %. В плазме крови растворены также питательные вещества (в частности глюкоза и липиды), гормоны, витамины, ферменты и промежуточные и конечные продукты обмена веществ, а также неорганические вещества.
В среднем 1 литр плазмы человека содержит 900—950 г воды, 65—85 г белка и 20 г низкомолекулярных соединений. Плотность плазмы составляет от 1,025 до 1,029, pH — 7,36—7,44.
Существует обширная практика собирания донорской плазмы крови. Плазма отделяется от эритроцитов центрифугированием с помощью специального аппарата, после чего эритроциты возвращаются донору. Этот процесс называется плазмаферезом.
Плазма с высокой концентрацией тромбоцитов (богатая тромбоцитами плазма) находит все большее применение в медицине в качестве стимулятора заживления и регенерации тканей организма. В настоящее время на её основе разработана многофункциональная медицинская методика, используемая в стоматологии и косметологии.
3.2. Форменные элементы
У взрослого человека форменные элементы крови составляют около 40—50 %, а плазма — 50—60 %. Форменные элементы крови представлены эритроцитами, тромбоцитами и лейкоцитами:
Кровь относится к быстро обновляющимся тканям. Физиологическая регенерация форменных элементов крови осуществляется за счёт разрушения старых клеток и образования новых органами кроветворения. Главным из них у человека и других млекопитающих является костный мозг. У человека красный, или кроветворный, костный мозг расположен в основном в тазовых костях и в длинных трубчатых костях. Основным фильтром крови является селезёнка (красная пульпа), осуществляющая в том числе и иммунологический её контроль (белая пульпа).
4. Биохимия эритроцита
4.1. Транспорт кислорода кровью
4.2. Созревание эритроцита
4.3. Структурно-метаболические особенности эритроцита
Особенности структурной организации мембраны эритроцитов
Эритроцит окружен плазматической мембраной, структура которой хорошо изучена, идентична таковой в других клетках. Цитоплазматическая мембрана эритроцитов включает бислой фосфолипидов, в то время как белки или «плавают» на поверхности мембран, или пронизывают липиды, обеспечивая прочность и вязкость мембран. Площадь мембраны одного эритроцита составляет около 140 мкм2.
На долю белков приходится примерно 49 %, липидов – 44 %, углеводов –7 %. Углеводы химически связаны либо с белками, либо с липидами и образуют соответственно гликопротеиды и гликолипиды.
Важнейшими компонентами мембраны эритроцитов являются липиды, включающие до 48 % холестерина, 17-28 % – фосфотидилхолина, 13-25 % – сфингомиелина и ряд других фосфолипидов.
Фосфотидилхолин мембраны эритроцитов несет нейтральный заряд, практически не вступает в реакции взаимодействия с положительно заряженными каналами Са2+,, обеспечивая тем самым атромбогенность эритроцитов. Благодаря таким свойствам, как текучесть, пластичность, эритроциты способны проходить через капилляры диаметром
Белки мембраны эритроцита делят на периферические и интегральные. К периферическим белкам относят спектрин, анкирин, белок 4.1., белок р55, адуцин и др. В группу интегральных белков входит фракция 3, а также гликофорины А, В, С, О, Е. Анкирин образует соединение с р-спектрином. В составе эритроцитов обнаружено около 340 мембранных и 250 растворимых белков.
Пластичность эритроцитов связана с фосфорилированием мембранных белков, особенно белков полосы 4.1.
Белок фракции 4.2. – паллидин обеспечивает связывание спектрин-актин-анкиринового комплекса с фракцией 3, относится к группе трансглутаминазных протеинов.
К числу сократительных белков мембраны эритроцитов относятся р-актин, тропомодулин, строматин и тропомиозин.
Гликофорины – интегральные белки мембраны эритроцитов, определяющие отрицательный заряд, способствующий отталкиванию эритроцитов друг от друг и от эндотелия сосуда.
Протеин 3 – основной белок актинов, регулирующий дефосфорилируемость эритроцита.
Как указывалось выше, мембрана эритроцита представляет собой сложный комплекс, включающий определенным образом организованные липиды, белки и углеводы, которые формируют наружный, средний и внутренний слои эритроцитарной мембраны.
Касаясь пространственного расположения различных химических компонентов эритроцитарной мембраны, следует отметить, что наружный слой образован гликопротеидами с разветвленными комплексами олигосахаридов, которые являются концевыми отделами групповых антигенов крови. Липидным компонентом наружного слоя являются фосфатидилхолин, сфингомиелин и неэстерифицированный холестерин. Липиды наружного слоя мембраны эритроцита играют важную роль в обеспечении постоянства структуры мембраны, избирательности ее проницаемости для различных субстратов и ионов. Вместе с фосфолипидами холестерин регулирует активность мембранно-связанных ферментов путем изменения вязкости мембраны, а также участвует в модификации вторичной структуры ферментов. Молярное отношение холестерин / фосфолипиды в мембранах клеток у человека и многих млекопитающих равно 0,9. Изменение этого соотношения в сторону увеличения наблюдается в пожилом возрасте, а также при некоторых заболеваниях, связанных с нарушением холестеринового обмена.
Снижение текучести мембраны эритроцита и изменение ее свойств отмечается также и при увеличении содержания сфингомиелина,
Средний бислой мембраны эритроцита представлен гидрофобными «хвостами» полярных липидов. Липидный бислой обладает выраженной текучестью, которая обеспечивается определенным соотношением между насыщенными и ненасыщенными жирными кислотами гидрофобной части бислоя. Интегральные белки, к которым относятся ферменты, рецепторы, транспортные белки, обладают активностью только в том случае, если находятся в гидрофобной части бислоя, где они приобретают необходимую для активности пространственную конфигурацию. Поэтому любые изменения в составе липидов эритроцитарной мембраны сопровождаются изменением ее текучести и нарушением работы интегральных белков.
Внутренний слой мембраны эритроцита, обращенный к цитоплазме, состоит из белков спектрина и актина. Спектрин является специфическим белком эритроцитов, его гибкие вытянутые молекулы, связываясь с микрофиламентами актина и липидами внутренней поверхности мембраны, формируют своеобразный скелет эритроцита. Небольшой процент липидов во внутреннем слое мембраны эритроцита представлен фосфатидилэтаноламином и фосфатидилсерином. От наличия спектрина зависит подвижность белков, удерживающих двойной бисой липидов.
Одним из важных гликопротеинов является гликофорин, содержащийся как на внешней, так и на внутренней поверхностях мембран эритроцитов. Гликофорин в своем составе содержит большое количество сиаловой кислоты и обладает значительным отрицательным зарядом. В мембране он располагается неравномерно, образует выступающие из мембраны участки, которые являются носителями иммунологических детерминант.
Строение и состояние эритроцитарной мембраны, низкая вязкость нормального гемоглобина обеспечивают значительные пластические свойства эритроцитам, благодаря которым эритроцит легко проходит по капиллярам, имеющим вдвое меньший диаметр, чем сама клетка, и может принимать самые разнообразные формы. Другим периферическим мембранным белком эритроцитов является анкирин, образующий соединение с молекулой Р-спектрина.
Функции эритроцитарной мембраны
Мембрана эритроцитов обеспечивает регуляцию электролитного баланса клетки за счет активного энергозависимого транспорта электролитов или пассивной диффузии соединений по осмотическому градиенту.
В мембране эритроцитов имеются ионно-проницаемые каналы для катионов Na+, K+, для O2, CO2, Cl– HCO3–.
Транспорт электролитов через эритроцитарную мембрану и поддержание его мембранного потенциала обеспечивается энергозависимыми Na+, K+, Ca2+ – АТФ-азными системами.
Мембрана эритроцитов хорошо проницаема для воды при участии так называемых белковых и липидных путей, а также анионов, газообразных соединений и плохо проницаема для одновалентных катионов калия и натрия.
Белковый путь трансмембранного переноса воды обеспечивается при участии пронизывающего мембрану эритроцитов белка «полосы 3», а также гликофорина.
Молекулярная природа липидного пути переноса воды через эритроцитарную мембрану практически не изучена. Прохождение молекул небольших гидрофильных неэлектролитов через эритроцитарную мембрану осуществляется также, как и перенос воды, за счет белкового и липидного путей. Перенос мочевины и глицерина через мембрану эритроцита обеспечивается за счет ферментативных реакций.
Перенос органических анионов через эритроцитарную мембрану обеспечивается, как и транспорт неорганических анионов, при участии белка «полосы 3».
Эритроцитарная мембрана обеспечивает активный транспорт глюкозы, кинетика которого обеспечивается зависимостью Михаэлиса-Ментен. Важная роль в транспорте глюкозы через эритроцитарную мембрану отводится полипептиду полосы 4,5 (белки с ММ 55 кД – возможные продукты распада полипептида полосы 3). Высказывается предположение о наличии специфического липидного окружения у белков – переносчиков сахаров в эритроцитарной мембране.
Неравномерное распределение моновалентных катионов в системе эритроцит – плазма крови поддерживается при участии энергозависимой Na+-помпы, осуществляющей трансмембранный обмен ионов Na+ эритроцитов на ионы К+ плазмы крови в соотношении 3:2. Кроме указанного трансмембранного обмена Na+/K+, Na+ помпа осуществляет еще, по крайней мере, четыре транспортных процесса: Na+→ Na+ обмен; K+→K+обмен; одновалентный вход ионов Na+, сопряженный с выходом К+.
Молекулярной основой Na+ помпы является фермент Na+, K+ –АТФ-аза – интегральный белок, прочно связанный с мембранными липидами, состоящий из 2х полипептидных субъединиц с ММ 80-100кД.
Транспортная система имеет 3 центра, связывающих ионов Na+, локализованных на цитоплазматической стороне мембраны. С наружной стороны мембраны на транспортной системе имеется 2 центра связывания ионов К+. Важная роль в поддержании высокой активности фермента отводится мембранным фосфолипидам.
Функционирование Са2+-помпы обеспечивается нуклеотидами, а также макроэргическими соединениями, преимущественно АТФ, ЦТФ, ГТФ, в меньшей степени ГТФ и ЦТФ.
Как в случае Nа+-помпы, функционирование Са2+помпы в эритроцитах связано с проявлениями активности Са2+, Mg2+ –АТФ-азы. В мембране одного эритроцита обнаруживается около 700 молекул Са2+, Mg2+ –АТФ-азы.
Наряду с барьерной и транспортной функциями, мембрана эритроцитов выполняет рецепторную функцию.
Экспериментально доказано наличие на мембране эритроцитов рецепторов к инсулину, эндотелину, церулоплазмину, а2-макроглобулину, α- и β-адренорецепторов. На поверхности эритроцитов находятся рецепторы к фибриногену, обладающие достаточно высокой специфичностью. Эритроциты также несут на мембране рецепторы к гистамину, ТхА2, простациклину.
В мембране эритроцитов обнаруживаются рецепторы для катехоламинов, снижающих подвижность жирных кислот липидов мембран эритроцитов, а также осмотическую устойчивость эритроцитов.
Установлена перестройка структуры мембраны эритроцитов под влиянием низких концентраций инсулина, гормона роста человека, простагландинов группы Е и Е2.
В мембранах эритроцитов высока и ц – АМФ активность. При увеличении концентраций в эритроцитах ц–АМФ ( до 10–6 М) усиливаются процессы фосфорилирования белков, что приводит в свою очередь к изменению степени фосфорилированности и проницаемости мембран эритроцитов для ионов Са2+.
Эритроцитарная мембрана содержит изоантигены различных систем иммунологических реакций, определяющих групповую принадлежность крови человека по этим системам.
4.4. Антигенная структура эритроцитарной мембраны
Эритроцитарная мембрана содержит различные антигены видовой, групповой и индивидуальной специфичности. Различают два вида изоантигенов эритроцитов, определяющих групповую специфичность крови человек – А и В агглютиногены. Соответственно в плазме или сыворотке крови обнаруживаются две разновидности изоантител – агглютинины α и β. В крови человека не содержатся одноименных агглютиногенов и агглютининов. Их встреча и взаимодействие может возникать при переливании несовместимых групп крови, приводить к развитию агглютинации и гемолиза эритроцитов.
Как известно, I (0) группа крови характеризуется отсутствием в эритроцитах агглютиногенов А и В при наличии в плазме или сыворотке крови агглютининов α и β, встречается у 40-50 % людей стран центральной Европы.
II (А) группа крови характеризуется наличием в мембране эритроцитов агглютиногена А, в то время как в плазме крови содержатся агглютинины β. Указанная группа крови распространена у 30–40 % людей.
III (В) группа крови характеризуется наличием агглютиногена В в мембране эритроцитов, а в плазме или сыворотке крови – наличием агглютининов типа α. Эта группа крови имеет место примерно у 10 % населения.
IV (АВ) группа крови характеризуется наличием в мембране эритроцитов фиксированных А и В агглютиногенов, при этом в плазме или сыворотке крови отсутствуют естественные агглютинины α и β. Данная группа крови встречается у 6 % населения.
Генетический контроль антигенной системы А,В,О мембран эритроцитов представлен генами О, Н, А, В, локализованными в длинном плече 9-й пары хромосом.
Агглютинины α и β относятся к классу Ig M, являются естественными антителами, образуются у ребенка на первом году жизни, достигая максимума к 8 – 10 годам.
Второе место среди антигенных свойств мембран эритроцитов по клинической значимости занимает система Rh – Hr. Впервые Резус-фактор был открыт в 1940 году К. Ландштейнером и А. Винером, содержится в эритроцитах у 85 % людей белой расы. У 15 % людей эти эритроцитарные антигены отсутствуют. В настоящее время установлена липопротеидная природа антигенов данной системы, их насчитывается около 20, они образуют различные комбинации в мембране эритроцитов. Наиболее распространенными резусантигенами являются 6 разновидностей: Rh0 (D), rh’ (C), rh’’ (E), Hr0 (d), hr’ (c), hr’’ (e). Наиболее сильным антигеном этой группы является Rh0 (D).
Антитела системы Rh и Hr – антирезусагглютинины являются приобретенными, иммунными, отсутствуют в крови Rh (-) людей с момента рождения, синтезируются при первом переливании Rh (+) крови Rh (-) реципиенту, а также при первой беременности Rh (-) женщины Rh(+) плодом. При первой беременности эти антитела синтезируются медленно в течение нескольких месяцев в небольшом титре, не вызывая серьезных осложнений у матери и плода. При повторном контакте резус-отрицательного человека с резус-положительными эритроцитами возможен резус-конфликт. Антитела системы Rh – Hr относятся к классу Ig G, поэтому они легко проникают через плацентарный барьер, вызывают реакции агглютинации и гемолиза эритроцитов плода, что сопровождается развитием гемолитической желтухи новорожденных. В случае повторного переливания несовместимой по Rh–антигенам крови донора и реципиента может наблюдаться гемотрансфузионный шок.
