Как найти число нейтронов
Как найти число протонов и нейтронов
Протоны и нейтроны, содержащиеся в ядерном ядре, называют нуклонами. От того что фактически каждая масса атома сконцентрирована в его ядре, то массовое число атома обозначает число нуклонов в ядре. С поддержкой периодической таблицы химических элементов Менделеева дозволено обнаружить число протонов и нейтронов. Для этого также дозволено применять другие методологии.
Вам понадобится
Инструкция
1. Всякому атому вещества соответствует элемент периодической таблицы Менделеева. Обнаружьте такой элемент для атома, число протонов и нейтронов в ядре которого надобно обнаружить. Определите ядерную массу этого элемента. Она находится в нижней части ячейки, где размещен химический элемент. Если массовое число представлено дробным значением, округлите его до целых. Это число будет равно числу нуклонов в атоме. Скажем, определите ядерную массу магния. Обнаружьте данный элемент в периодической таблице, он имеет обозначение Mg. Его массовое число равно 24,305. Округлите его до целого и получите 24. Это значит, что число протонов и нейтронов (нуклонов) в ядре атома этого элемента равно 24.
2. Определите число протонов в ядре атома. Для этого обнаружьте его в периодической таблице химических элементов. В верхней части ячейки элемента подмечен его порядковый номер по счету в таблице. Это и есть число протонов в ядре атома исследуемого элемента. Скажем, порядковый номер магния (Mg) равен 12. Это значит, что в его ядре содержится 12 протонов.
4. Позже определения числа протонов обнаружьте число нейтронов в ядре. Для этого от относительной ядерной массы ядра, обнаруженной при помощи периодической таблицы химических элементов, отнимите число протонов, содержащихся в ядре. От того что помимо нейтронов других тяжелых частиц в ядре атома не содержится, это и будет число нейтронов. Скажем, если необходимо обнаружить число протонов и нейтронов в ядре фосфора (Р), обнаружьте его в периодической таблице, определите массовое число и порядковый номер элемента. Массовое число фосфора равно 30,97376?31, а порядковый номер 15. Это значит, что в ядре атома этого химического элемента содержится 15 протонов и 31-15=16 нейтронов.
Совет 2: Как определить число нейтронов
Атом химического элемента состоит из ядерного ядра и электронов. В состав ядерного ядра входят два типа частиц – протоны и нейтроны. Примерно каждая масса атома сконцентрирована в ядре, потому что протоны и нейтроны гораздо тяжелее электронов.
Вам понадобится
Инструкция
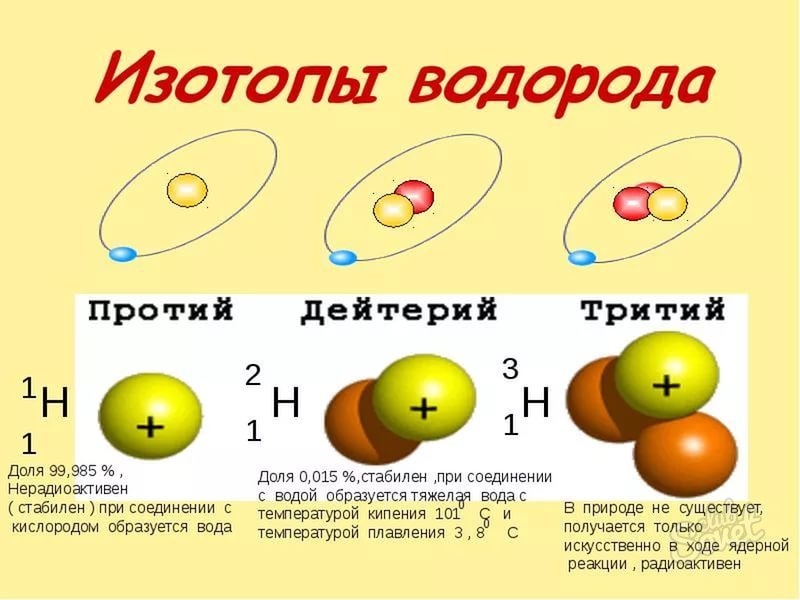
3. У различных изотопов одного химического элемента число A меняется, что отражено в записи этого изотопа. Определенные изотопы имеют свои подлинные наименования. Скажем, обыкновенное ядро водорода не имеет нейтронов и имеет один протон. Изотоп водорода дейтерий имеет один нейтрон (A = 2), а изотоп тритий – два нейтрона (A = 3).
4. Связанность числа нейтронов от числа протонов отражена на N-Z диаграмме ядерных ядер. Стабильность ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов особенно устойчивы при N/Z = 1, то есть при равенстве числа нейтронов и протонов. С ростом массового числа область стабильности сдвигается к величинам N/Z>1, достигая величины N/Z
1,5 для особенно тяжелых ядер.
Видео по теме
Совет 3: Как обнаружить число нейтронов
Атом химического элемента состоит из ядерного ядра и электронной оболочки. В состав ядерного ядра входят два типа частиц – протоны и нейтроны. Примерно каждая масса атома сконцентрирована в ядре, так как протоны и нейтроны гораздо тяжелее электронов.
Вам понадобится
Инструкция
2. Ядра атомов обозначают буквенным символом химического элемента из таблицы Менделеева. Справа от символа вверху и внизу стоят два числа. Верхнее число A – это массовое число атома. A = Z+N, где Z – заряд ядра (число протонов), а N – число нейтронов. Нижнее число – это Z – заряд ядра. Такая запись дает информацию о числе нейтронов в ядре. Видимо, что оно равно N = A-Z.
3. У различных изотопов одного химического элемента число A меняется, что дозволено увидеть в записи этого изотопа. Определенные изотопы имеют свои подлинные наименования. Скажем, обыкновенное ядро водорода не имеет нейтронов и имеет один протон. Изотоп водорода дейтерий имеет один нейтрон (A = 2, цифра 2 сверху, 1 снизу), а изотоп тритий – два нейтрона (A = 3, цифра 3 сверху, 1 снизу).
4. Связанность числа нейтронов от числа протонов отражена на так называемой N-Z диаграмме ядерных ядер. Стабильность ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов особенно устойчивы при N/Z = 1, то есть при равенстве числа нейтронов и протонов. С ростом массового числа область стабильности сдвигается к величинам N/Z>1, достигая величины N/Z
1,5 для особенно тяжелых ядер.
Видео по теме
Совет 4: Как обнаружить число протонов
Дабы обнаружить число протонов в атоме, определите его место в таблице Менделеева. Обнаружьте его порядковый номер в периодической таблице. Он будет равен числу протонов в ядерном ядре. Если изучается изотоп, посмотрите на пару чисел, описывающие его свойства, нижнее число будет равно числу протонов. В том случае, если знаменит заряд ядерного ядра, дозволено узнать число протонов, поделив его значение на заряд одного протона.
Вам понадобится
Инструкция
1. Определение числа протонов знаменитого атома.В том случае, когда знаменито, какой атом изучается, обнаружьте его расположение в периодической таблице. Определите его номер в этой таблице, обнаружив ячейку соответствующего элемента. В данной ячейке обнаружьте порядковый номер элемента, тот, что соответствует постигаемому атому. Данный порядковый номер и будет соответствовать числу протонов в ядерном ядре.
2. Как обнаружить протоны в изотопе.Многие атомы имеют изотопы, отличающиеся массами ядер. Именно следственно только лишь массы ядра неудовлетворительно для однозначного определения ядерного ядра. При изложении изотопа перед записью его химического обозначения неизменно записывается пара чисел. Верхнее число показывает массу атома в ядерных единицах массы, а нижнее обозначает заряд ядра. Вся единица заряда ядра в такой записи соответствует одному протону. Таким образом, число протонов равно нижнему числу в записи данного изотопа.
3. Как обнаружить протоны, зная заряд ядра.Зачастую свойства атома характеризуется зарядом его ядра. Для того дабы определить число протонов в нем, нужно перевести его в кулоны (если он подан в кратных единицах). После этого поделите заряд ядра на модуль заряда электрона. Это связано с тем, что от того что атом электрически нейтрален, то число протонов в нем равно числу электронов. Причем заряды их равны по модулю и противоположны по знаку (протон имеет правильный заряд, электрон – негативный). Следственно заряд ядра атома поделите на число 1,6022•10^(-19) кулон. В итоге получится число протонов. От того что способы измерения заряда атома неудовлетворительно точны, в том случае, если при делении получилось дробное число, округлите его до целого.
Видео по теме
Совет 5: Как вычислить число протонов в ядре изотопа
Атомы состоят из субатомных частиц — протонов, нейтронов и электронов. Протоны представляют собой правильно заряженные частицы, которые находятся в центре атома, в его ядре. Вычислить число протонов изотопа дозволено по ядерному номеру соответствующего химического элемента.
Модель атома
Для изложения свойств атома и его конструкции применяется модель, вестимая под наименованием «Модель атома по Бору». В соответствии с ней конструкция атома напоминает ясную систему — весомый центр (ядро) находится в центре, а больше легкие частицы движутся по орбите вокруг него. Нейтроны и протоны образуют позитивно заряженное ядро, а негативно заряженные электроны движутся вокруг центра, притягиваясь к нему электростатическими силами.Элементом называют вещество, состоящее из атомов одного типа, он определяется числом протонов в всем из них. Элементу присваивают свое имя и символ, скажем, водород (H) либо кислород (О). Химические свойства элемента зависят от числа электронов и, соответственно, числа протонов, содержащихся в атомах. Химические колляции атома не зависят от числа нейтронов, потому что нейтроны не имеют электрического заряда. Впрочем их число влияет на устойчивость ядра, изменяя всеобщую массу атома.
Изотопы и число протонов
Примеры
В качестве примера дозволено разглядеть изотопы водорода. В природе особенно распространены атомы водорода с одним протоном и без нейтронов. В то же время существуют изотопы водорода с одним либо двумя нейтронами, они имеют соответствующие наименования. Впрочем у них у всех один протон, что соответствует порядковому номеру водорода в периодической таблице. Изотоп водорода с одним нейтроном и массовым числом 2 называют дейтерием либо тяжелым водородом, он стабилен. Тритий, изотоп водорода с массовым числом 3 и двумя нейтронами, радиоактивен. Его изредка называют сверхтяжелым водородом, а ядро трития — тритоном.
Как определить нейтрон: «Как определить число нейтронов?» – Яндекс.Кью
Как определить число нейтронов протонов и электронов в изотопе?
Для того чтобы это сделать вам нужно знать 3 вещи:
Число протонов и электронов в атоме одинаково и равно порядковому номеру элемента в периодической таблице.
Число нейтронов вычисляется по формуле:
Где N — число нейтронов, A — атомная масса элемента (в целых числах), Z — заряд ядра атома (число протонов) или порядковый номер атома в периодической таблице Менделеева.
Что такое изотоп?
Изотопы это разновидности атомов химического элемента, которые имеют одинаковый заряд ядра (порядковый номер в таблице), но разные массовые числа.
Проще говоря, у изотопов в ядре атома одинаковое число протонов, но разное число нейтронов.
Примеры
Сколько электронов, протонов и нейтронов содержит атом изотопа титана 50 Ti?
Титан имеет порядковый номер 22. Значит в ядре содержится 22 протона, а в атоме 22 электрона.
Число нейтронов: N = 50 — 22 = 28 нейтронов.
Сколько электронов содержит нейтральный атом изотопа полония?
В данном случае нам даже не нужно знать массовое число изотопа, т.к. речь идет только об электронах. Порядковый номер полония 84, значит в ядре атома 84 протона, а в атоме 84 электрона.
Определите число протнов, нейтронов и электронов для изотопа 55 Mn.
Порядковый номер марганца 25. Значит в ядре атома 25 протонов, а в атоме 25 электронов.
Найдем число нейтронов: N = 55 — 25 = 30 нейтронов.
Определите число протонов изотопа калия.
В этом случае массовое число изотопа не имеет значения, т.к. речь идет о протонах, число которых у изотопов одинаково. 
Похожие вопросы:
— Какие атомы имеют одинаковое число нейтронов?
— Как определить общее число электронов в атоме?
Mathway | Популярные задачи
Информаторий — ФЭО
Структура материи
Строение атома
Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства. 
Каждый энергетический уровень делится на подуровни. На первом уровне только один подуровень — s. На втором уровне два подуровня — s и p. на третьем — s, p и d. На четвертом — s, p, d и f.
Максимальное число электронов на подуровнях
Максимальное число электронов на подуровне не зависит от номера уровня.
Заполнение энергетических уровней
1s Геометрия орбиталей
Примеры
Полезные ссылки
Электронная оболочка атома (видео)
Строение атома (Часть 1) (видео)
Строение атома (Часть 2) (видео)
Строение атома. 
Дополнительные материалы
Модели строения атома (видео)
Строение атома: Атомное ядро (видео)
Химия. Строение атома: Строение электронных оболочек (видео)
Строение атома (видео)
Как определить протон, нейтрон, электрон
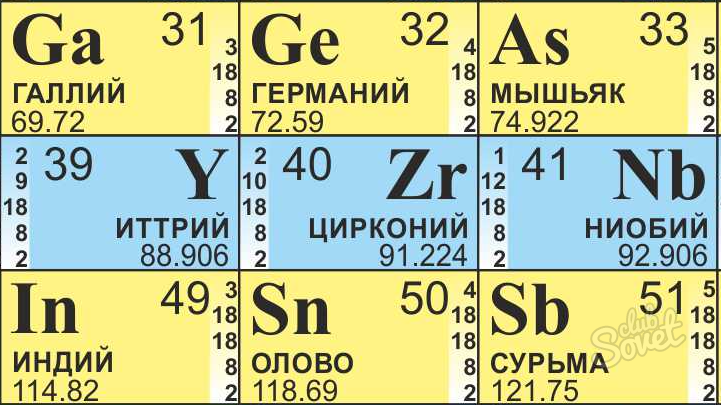
Таблица Д.И. Менделеева разделена на группы (располагаются вертикально), которых всего восемь, а также на периоды, расположенные горизонтально. Каждый химический элемент имеет свой порядковый номер и относительную атомную массу, что указано в каждой клетке периодической таблицы.Количество протонов (р) и электронов (ē) численно совпадает с порядковым номером элемента. Для определения числа нейтронов (n) необходимо из относительной атомной массы (Ar) вычесть номер химического элемента.
Ядерные реакции (задачи)
Ядерные реакции
1. Перечислить несколько ядерных реакций, в которых может образоваться изотоп 8 Be.
2. Какую минимальную кинетическую энергию в лабораторной системе Tmin должен иметь нейтрон, чтобы стала возможной реакция 16 O(n,α) 13 C?
3. Является ли реакция 6 Li(d,α) 4 He эндотермической или экзотермической? Даны удельные энергии связи ядер в МэВ: ε(d) = 1.11; ε() = 7.08; ε( 6 Li) = 5.33.
4. Определить пороги Tпор реакций фоторасщепления 12 С.
5. 
6. Определить, какую минимальную энергию должен иметь протон, чтобы стала возможной реакция p + d → p + p + n. Даны избытки масс. Δ( 1 H) = 7.289 МэВ, Δ( 2 H) = 13.136 МэВ,
Δ(n) = 8.071 МэВ.
7. Возможны ли реакции:
под действием α-частиц с кинетической энергией T = 10 МэВ?
8. Идентифицировать частицу X и рассчитать энергии реакции Q в следующих случаях:
| 1. 35 Сl + X→ 32 S + α; | 4. 23 Na + p→ 20 Ne + X; |
| 2. 10 B + X→ 7 Li + α; | 5. 23 Na + d→ 24 Mg + X; |
3.  7 Li + X → 7 Be + n; 7 Li + X → 7 Be + n; | 6. 23 Na + d→ 24 Na + X. |
9. Какую минимальную энергию Tmin должен иметь дейтрон, чтобы в результате неупругого рассеяния на ядре 10 B возбудить состояние с энергией Eвозб = 1.75 МэВ?
10. Вычислить порог реакции: 14 N + α→ 17 О + p, в двух случаях, если налетающей частицей является:
1) α-частица,
2) ядро 14 N. Энергия реакции Q = 1.18 МэВ. Объяснить результат.
11. Рассчитать энергии и пороги следующих реакций:
| 1. d( p,γ) 3 He; | 5. 32 S(γ,p ) 31 P; |
| 2. d( d, 3 He )n; | 6. 32 (γ,n ) 31 S; |
| 3. 7 Li( p,n ) 7 Be; | 7.  32 S(γ,α) 28 Si; 32 S(γ,α) 28 Si; |
| 4. 3 He(α,γ) 7 Be; | 8. 4 He(α,p) 7 Li; |
12. Какие ядра могут образовываться в результате реакций под действием: 1) протонов с энергией 10 МэВ на мишени из 7 Li; 2) ядер 7 Li с энергией 10 МэВ на водородной мишени?
13. Ядро 7 LI захватывает медленный нейтрон и испускает γ-квант. Чему равна энергия γ-кванта?
14. Определить в лабораторной системе кинетическую энергию ядра 9 Ве, образующегося при пороговом значении энергии нейтрона в реакции 12 C(n,α) 9 Be.
15. При облучении мишени из натурального бора наблюдалось появление радиоактивных изотопов с периодами полураспада 20.4 мин и 0.024 с. Какие образовались изотопы? Какие реакции привели к образованию этих изотопов?
17. α-Частица с кинетической энергией T = 10 МэВ испытывает упругое лобовое столкновение с ядром 12 С. Определить кинетическую энергию в л.с. ядра 12 C TC после столкновения.
20. α-Частицы с энергией T = 5 МэВ взаимодействуют с неподвижным ядром 7 Li. Определить величины импульсов в с.ц.и., образующихся в результате реакции 7 Li(α,n) 10 B нейтрона pα и ядра 10 B pBe.
21. С помощью реакции 32 S(α,p) 35 Cl исследуются низколежащие возбужденные состояния 35 Cl (1.219; 1.763; 2.646; 2.694; 3.003; 3.163 МэВ). Какие из этих состояний будут возбуждаться на пучке α-частиц с энергией 5.0 МэВ? Определить энергии протонов, наблюдаемых в этой реакции под углами 0 0 и 90 0 при Е =5.0 МэВ.
22. Используя импульсную диаграмму получить связь между углами в л.с. и с.ц.и.
24. Для получения нейтронов широко используется реакция t(d,n)α. Определить энергию нейтронов Tn, вылетающих под углом 90 0 в нейтронном генераторе, использующем дейтроны, ускоренные до энергии Тd = 0.2 МэВ.
25. Для получения нейтронов используется реакция 7 Li(p,n) 7 Be. Энергия протонов Tp = 5 МэВ. Для эксперимента необходимы нейтроны с энергией Tn = 1.75 МэВ. Под каким углом θn относительно направления протонного пучка будут вылетать нейтроны с такой энергией? Какой будет разброс энергий нейтронов ΔT, если их выделять с помощью коллиматора размером 1 см, расположенного на расстоянии 10 см от мишени.
26. Определить орбитальный момент трития lt, образующегося в реакции 27 Al(,t) 28 Si, если орбитальный момент налетающей α-частицы lα = 0.
30. Ядро 12 C поглощает γ-квант, в результате чего вылетает протон с орбитальным моментом l = 1. Определить мультипольность поглощенного γ-кванта, если конечное ядро образуется в основном состоянии?
31. Определить орбитальный момент дейтрона ld в реакции подхвата 15 N(n,d) 14 C, если орбитальный момент нейтрона ln = 0.
33. Ядро 40 Cа поглощает Е1 γ-квант. Какие одночастичные переходы возможны?
40. Интегральное сечение реакции 32 S(γ,p) 31 P с образованием конечного ядра 31 P в основном состоянии при энергии падающих γ-квантов, равной 18 МэВ, составляет 4 мб. Оценить величину интегрального сечения обратной реакции 31 P(p,γ) 32 S, отвечающей той же энергии возбуждения ядра 32 S, что и в реакции 32 S(γ,p) 31 P. Учесть, что это возбуждение снимается за счет γ-перехода в основное состояние.
42. Дифференциальное сечение реакции dσ/dΩ под углом 90 0 составляет 10 мб/ср. Рассчитать величину интегрального сечения, если угловая зависимость дифференциального сечения имеет вид 1+2sinθ.
43. Рассеяние медленных (Tn1 кэВ) нейтронов на ядре изотропно. Как можно объяснить этот факт?
44. Определить энергию возбуждения составного ядра, образующегося при захвате α-частицы с энергией T = 7 МэВ неподвижным ядром 10 В.
45. В сечении реакции 27 Аl (α,р) 30 Si наблюдаются максимумы при энергиях α-частиц T 3. 
46. С каким орбитальным моментом могут рассеиваться протоны с Тр = 2 МэВ на ядре 112 Sn?
47. Оценить сечение образования составного ядра при взаимодействии нейтронов с кинетической энергией Tn = 1 эВ с ядрами золота 197 Au.
48. Оценить сечение образования составного ядра при взаимодействии нейтронов с кинетической энергией Tn = 30 МэВ с ядрами золота 197 Au.
49. Сравнить полные сечения реакции для α-частиц с энергией 20 Мэв на ядрах 56 Fe и 197 Au.
50. Оценить сечение реакции 63 Cu(p,n) 63 Zn, если известны сечения реакций, идущих с образованием того же составного ядра с той же энергией возбуждения:
60 Ni(α,p) 63 Zn — 0. 
51. Оценить нейтронную ширину Гn изолированного уровня 0 + ядра 108 Rh (энергия уровня E0 = 1.21 эВ, полная ширина Г = 0.21 эВ), если при резонансном поглощении нейтронов с образованием этого уровня составного ядра сечение поглощения для энергии нейтронов Tn = 1 эВ σ = 2700 б. Спин ядра-мишени I( 107 Rh) = 1/2.
52. Получить, исходя из модели оболочек, отношение сечений реакций подхвата 16 O(p,d) 15 O, с образованием конечного ядра 15 O в основном состоянии (J P =1/2 — ) и в состоянии (J P =3/2 — ).
53. Для реакции срыва 35 Cl(d,p) 36 Cl найти возможные значения орбитального момента ln захваченного ядром нейтрона. 
56. Показать, что в реакции неупругого рассеяния дейтронов на ядре 10 B, идущей за счёт сильного взаимодействия, невозможно возбуждение уровней этого ядра с изоспином I = 1.
| Спектр нижних уровней ядра |
57. 
58. Оценить отношение сечений двух каналов реакции фоторасщепления ядра 16 O:
γ + 16 O → 15 Ngs + p, (а)
γ + 16 O → 15 N*(J P = 3/2 − ) + p. (б)
Физики получили самый тяжелый изотоп кальция
O. B. Tarasov et al./ Physical Review Letters, 2018
Физики впервые синтезировали самый тяжелый на сегодняшний день изотоп кальция 60 Ca, ядро которого содержит 20 протонов и 40 нейтронов. Также впервые были получены самые тяжелые изотопы для других элементов: фосфора, серы, хлора, аргона, калия и скандия. 
Максимальное количество нейтронов в ядре каждого элемента, при котором это ядро будет жить хоть какое-то время, определяется силами, связывающими нуклоны между собой. Для описания устойчивых конфигураций атомных ядер существует несколько теоретических моделей, ни одна из которых на сегодняшний день не может однозначно определить границу нуклонной устойчивости. Самые устойчивые нуклонные конфигурации часто описываются с использованием магических чисел, которые соответствуют полностью заполненным оболочкам нейтронов или протонов.
Например, ядро кальция интересно тем, что число протонов в нем всегда магическое — 20, а при определенных числах нейтронов ядро кальция становится «дважды магическим». Для этого в ядре должно быть 20, 28, 32 или 34 нейтрона. 
Каждое открытие самых легких и самых тяжелых изотопов для отдельных элементов позволяет сместить границу нуклонной стабильности и подтвердить или опровергнуть существующие теоретические модели. Группа физиков из России, США, и Японии под руководством Олега Тарасова (O. B. Tarasov) из Университета штата Мичиган предложили новый метод синтеза тяжелых изотопов с большим количеством нейтронов. Для этого ученые облучали вращающуюся мишень из бериллия 9 Be пучком ядер цинка 70 Zn с энергией 345 электронвольт. Образующиеся при этом частицы фиксировались с помощью спектрометра для идентификации частиц.
Общая диаграмма зарегистрированных в ходе эксперимента ядер: по вертикальной оси приведен номер элемента, по горизонтальной — отношение массового числа к заряду ядра. Красной линией обозначена граница самых тяжелых изотопов до этого исследования
O. B. Tarasov et al./ Physical Review Letters, 2018
В результате ученым зарегистрировали восемь новых изотопов, которые не удавалось получить ранее. Все эти изотопы (фосфор 47 P, сера 49 S, хлор 52 Cl, аргон 54 Ar, калий 57 K, кальций 59, 60 Ca и скандий 62 Sc) оказались самыми тяжелыми из известных на сегодняшний день для своих элементов. Также было зарегистрировано одно ядро 59 K, однако эти данные пока нельзя считать статистически значимыми. 
По словам авторов работы, полученные результаты позволили подтвердить некоторые из теоретических моделей, которые предполагают, что для кальция возможно образование и более тяжелых ядер, вплоть до 70 Ca.
Стоит отметить, что интерес вызывают не только изотопы с большим количеством нейтронов, но нейтрон-дефицитные ядра. Так, в 2015 году физикам удалось синтезировать сразу несколько изотопов, которые, наоборот, были самыми легкими из известных для урана, нептуния, берклия и америция. Эти ядерные структуры, которые находятся на границе нуклонной стабильности могут помочь в развитии теоретических моделей ядра атома.
Определение нейтрона по Merriam-Webster
: незаряженная элементарная частица, имеющая массу, почти равную массе протона, и присутствует во всех известных атомных ядрах, кроме ядра водорода.
нейтронов: определение и концепция | Изучение.
Числа
Нейтрон на 0,2% больше протона. Вместе нейтрон и протон составляют 99,99% всей массы атома. Нейтрон на самом деле имеет ту же массу, что и электрон и протон вместе взятые. Атомная масса атома находится путем сложения количества протонов и нейтронов. Поскольку атомный номер относится к количеству протонов в атоме, мы можем использовать как атомную массу, так и атомный номер, чтобы вычислить количество нейтронов.Используя приведенное ниже простое уравнение, мы можем найти количество нейтронов в атоме.
Атомная масса — атомный номер = количество нейтронов
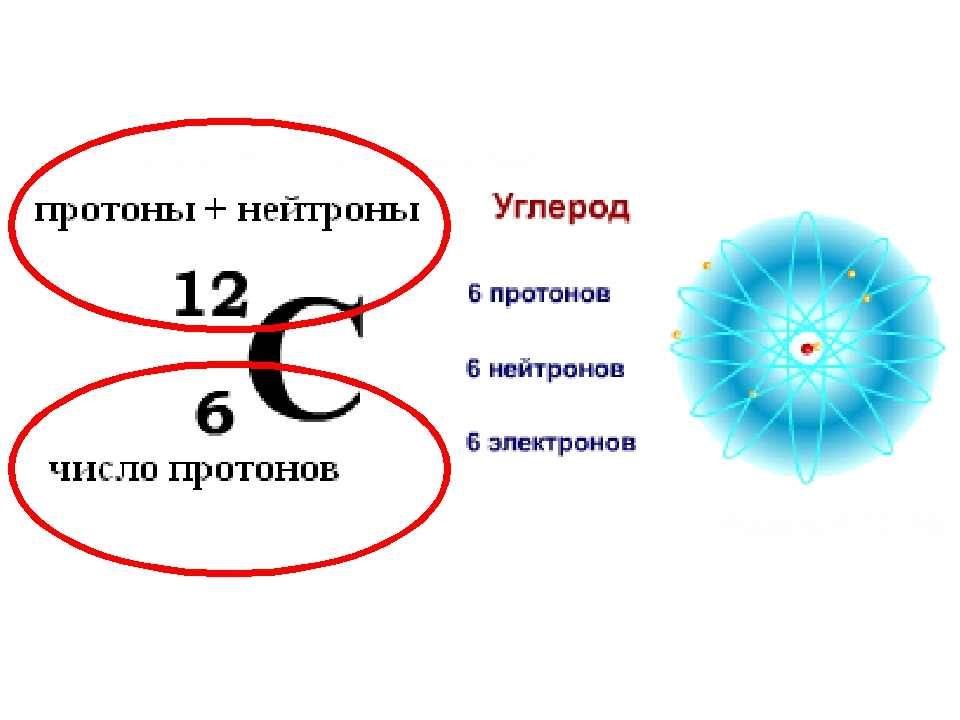
Например, углерод имеет атомную массу 12 и атомный номер 6. Итак, если мы поместим эти числа в наше уравнение, оно будет выглядеть так…
12 ( Атомная масса) — 6 (атомный номер) = 6 нейтронов.
Изотопы и радиоактивность
Атомы одного и того же элемента могут иметь разное количество нейтронов, поэтому, когда ученые говорят об атомной массе, они имеют в виду среднюю атомную массу. 
Ученые нашли способы добавления нейтронов к ядру, чтобы получить изотопы большего размера. Теперь добавление нейтронов не влияет на заряд атома, поскольку нейтрон не имеет заряда. Однако это увеличивает радиоактивность атома. Это может сделать атомы очень нестабильными, которые могут выделять большие уровни энергии.
У нейтронов есть еще пара интересных хитростей.Например, нейтроны могут существовать вне ядра атома. Не забывайте, что когда нейтрон уходит от атома, этот процесс называется радиоактивным распадом. Нейтроны обладают многими другими научными качествами и по-прежнему являются важной частью различных научно-исследовательских проектов. И последний лакомый кусочек: когда вы смотрите во Вселенную, нейтроны составляют половину всей видимой материи.
Резюме урока
Нейтроны — самые большие из субатомных частиц. 
Памятные термины
Результаты обучения
После того, как вы накопите свои знания о нейтронах, вы захотите:
нейтронов
См. 
Последний раз обновлялся в мае 2008 г.
4.11: Нейтроны — Химия LibreTexts
Что такое нейтрон?
Нейтрон — одна из трех основных частиц, составляющих атом. Две другие частицы — это протон и электрон. Атомы всех элементов, за исключением большинства атомов водорода, имеют нейтроны в своем ядре. Ядро — это небольшая плотная область в центре атома, где также находятся протоны. <-15>\) метров.
Одинаковый элемент, разное количество нейтронов
Все атомы данного элемента имеют одинаковое количество протонов и электронов. Однако количество нейтронов может быть разным для атомов одного и того же элемента. Например, почти 99 процентов атомов углерода имеют шесть нейтронов, а остальные имеют семь или восемь нейтронов. 
Частицы в нейтронах
Сводка
Нейтрон — одна из трех основных частиц, составляющих атом.Он находится в ядре и имеет нейтральный электрический заряд. Его масса и диаметр примерно такие же, как у протона. Нейтроны присутствуют во всех атомах, кроме большинства атомов водорода. Все атомы данного элемента имеют одинаковое количество протонов и электронов, но они могут различаться по количеству нейтронов. 
Узнать больше
Прочтите статью о нейтронах по следующему URL-адресу, а затем заполните приведенные ниже утверждения.
1. ________ создаются, когда вы меняете нормальное количество нейтронов в атоме.
2. Если к атому добавить много нейтронов, он станет __________.
3. Лишние нейтроны могут выбиваться из ядра в процессе _________________.
4. Единственный элемент, в котором обычно отсутствуют нейтроны, — это ________.
Авторы и авторство
Фонд CK-12 Шэрон Бьюик, Ричард Парсонс, Тереза Форсайт, Шонна Робинсон и Жан Дюпон.
4.4: Свойства протонов, нейтронов и электронов
Электронов
Электроны — это один из трех основных типов частиц, из которых состоят атомы. В отличие от протонов и нейтронов, которые состоят из более мелких и простых частиц, электроны являются элементарными частицами, которые не состоят из более мелких частиц. Это тип фундаментальных частиц, называемых лептонами. Все лептоны имеют электрический заряд \ (- 1 \) или \ (0 \). Электроны очень маленькие. Масса электрона составляет всего около 1/2000 массы протона или нейтрона, поэтому электроны практически ничего не вносят в общую массу атома.Электроны имеют электрический заряд \ (- 1 \), который равен, но противоположен заряду протона, который равен \ (+ 1 \). Все атомы имеют такое же количество электронов, что и протоны, поэтому положительный и отрицательный заряды «уравновешиваются», делая атомы электрически нейтральными.
В отличие от протонов и нейтронов, которые находятся внутри ядра в центре атома, электроны находятся вне ядра. Поскольку противоположные электрические заряды притягиваются друг к другу, отрицательные электроны притягиваются к положительному ядру. 
Рисунок \ (\ PageIndex <1>\): Электроны намного меньше протонов или нейтронов. Если бы электрон был массой пенни, протон или нейтрон имели бы массу большого шара для боулинга!
Протоны
Протон — одна из трех основных частиц, составляющих атом. <-15>\) метров.
Как вы уже догадались по названию, нейтрон нейтрон. Другими словами, он совершенно не заряжен и поэтому не привлекается и не отталкивается от других объектов. Нейтроны есть в каждом атоме (за одним исключением), и они связаны вместе с другими нейтронами и протонами в атомном ядре.
Прежде чем мы продолжим, мы должны обсудить, как различные типы субатомных частиц взаимодействуют друг с другом. 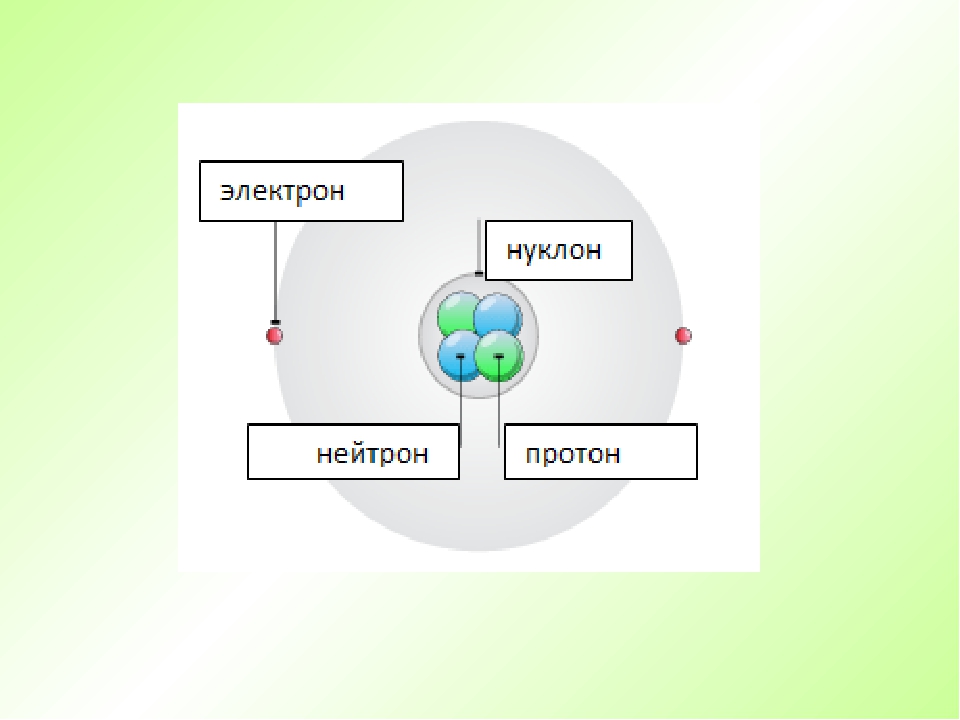
Хотя электроны, протоны и нейтроны — все типы субатомных частиц, они не все одинакового размера. Когда вы сравниваете массы электронов, протонов и нейтронов, вы обнаруживаете, что электроны имеют чрезвычайно малую массу по сравнению с протонами или нейтронами. С другой стороны, массы протонов и нейтронов довольно похожи, хотя технически масса нейтрона немного больше массы протона.Поскольку протоны и нейтроны намного массивнее электронов, почти вся масса любого атома исходит от ядра, которое содержит все нейтроны и протоны.
| Частица | Символ | Масса (а.  е.м.) е.м.) | Относительная масса (протон = 1) | Относительный заряд | Расположение |
|---|---|---|---|---|---|
| протон | п. + | 1 | 1 | +1 | внутри ядра |
| электрон | e — | 5.45 × 10 −4 | 0,00055 | -1 | вне ядра |
| нейтрон | n 0 | 1 | 1 | 0 | внутри ядра |
Отрицательный и положительный заряды равной величины нейтрализуют друг друга. Это означает, что отрицательный заряд электрона идеально уравновешивает положительный заряд протона. Другими словами, нейтральный атом должен иметь ровно один электрон на каждый протон.Если нейтральный атом имеет 1 протон, он должен иметь 1 электрон. Если у нейтрального атома 2 протона, у него должно быть 2 электрона. Если у нейтрального атома 10 протонов, у него должно быть 10 электронов. Вы уловили идею. Чтобы быть нейтральным, атом должен иметь одинаковое количество электронов и протонов.
Сводка
Материалы и авторство
Эта страница была создана на основе содержимого следующими участниками и отредактирована (тематически или всесторонне) командой разработчиков LibreTexts в соответствии со стилем, представлением и качеством платформы:
Что такое нейтрон | Определение и свойства
Макроскопическое сечение получено из микроскопического и плотности материала:
Σ = σ.№
Нейтронные сечения являются ключевыми параметрами ядерного топлива.Нейтронные сечения необходимо рассчитывать для свежих ТВС, как правило, в двумерных моделях топливной решетки.
Нейтронное сечение переменное и зависит от:
См. Также: JANIS (программное обеспечение ядерной информации на основе Java)
См. Также: Взаимодействие нейтронов с веществом
См. Также: Нейтронное сечение
Закон 1 / v
Этот закон применим только для сечения поглощения и только в области 1 / v.
Пример сечений в 1 / v области:
Сечение поглощения 238U при 20 ° C = 293K (
0.0253 эВ) составляет:
Поперечное сечение поглощения 238U при 1000 ° C = 1273K равно:
Это уменьшение поперечного сечения вызвано только изменением температуры окружающей среды.
Резонансный захват нейтронов
Сечение поглощения часто сильно зависит от энергии нейтронов.Обратите внимание, что при делении ядра образуются нейтроны со средней энергией 2 МэВ (200 ТДж / кг, т.е. 20000 км / с). Нейтрон можно условно разделить на три диапазона энергии:
Резонансные нейтроны называются резонансными из-за их особого поведения. При резонансных энергиях поперечное сечение может достигать пиков, более чем в 100 раз превышающих базовое значение поперечного сечения.При этих энергиях захват нейтрона значительно превышает вероятность деления. Поэтому очень важно (для тепловых реакторов), чтобы быстро преодолели этот диапазон энергий и эксплуатировали реактор с тепловыми нейтронами, что привело бы к увеличению вероятности деления.
Доплеровское уширение
Эффект Доплера улучшает стабильность реактора. Расширенный резонанс (нагрев топлива) приводит к более высокой вероятности поглощения, таким образом, вызывает добавление отрицательной реактивности (снижение мощности реактора).
Ядра расположены в атомах, которые сами находятся в непрерывном движении благодаря своей тепловой энергии.В результате этих тепловых движений нейтрона, падающего на мишень, кажутся ядрам в мишени имеющими непрерывный разброс по энергии. Это, в свою очередь, влияет на наблюдаемую форму резонанса. Резонанс становится на короче и на шире, чем когда ядра находятся в покое.
В следующей таблице показано нейтронных сечений наиболее распространенных изотопов активной зоны реактора.
Структура атома
Обзор атомной структуры
Атомы состоят из частиц, называемых протонами, нейтронами и электронами, которые отвечают за массу и заряд атомов.
Цели обучения
Обсудить электронные и структурные свойства атома
Ключевые выводы
Ключевые моменты
Ключевые термины
Атом — это наименьшая единица вещества, которая сохраняет все химические свойства элемента. Атомы объединяются в молекулы, которые затем взаимодействуют с образованием твердых тел, газов или жидкостей. Например, вода состоит из атомов водорода и кислорода, которые объединились в молекулы воды.Многие биологические процессы посвящены расщеплению молекул на составляющие их атомы, чтобы из них можно было собрать более полезную молекулу.
Атомные частицы
Атомы состоят из трех основных частиц: протонов, электронов и нейтронов. Ядро (центр) атома содержит протоны (положительно заряженные) и нейтроны (без заряда). Внешние области атома называются электронными оболочками и содержат электроны (отрицательно заряженные). Атомы имеют разные свойства в зависимости от расположения и количества их основных частиц.
Атом водорода (H) содержит только один протон, один электрон и не содержит нейтронов. Это можно определить, используя атомный номер и массовое число элемента (см. Понятие атомных номеров и массовых чисел).
Структура атома : Изображенные здесь элементы, такие как гелий, состоят из атомов. Атомы состоят из протонов и нейтронов, расположенных внутри ядра, а электроны находятся на орбиталях, окружающих ядро.
Атомная масса
Электроны вносят большой вклад в заряд атома, поскольку каждый электрон имеет отрицательный заряд, равный положительному заряду протона. Ученые определяют эти обвинения как «+1» и «-1». В незаряженном нейтральном атоме количество электронов, вращающихся вокруг ядра, равно количеству протонов внутри ядра. В этих атомах положительный и отрицательный заряды нейтрализуют друг друга, в результате чего получается атом без чистого заряда.
Изучение свойств электрона : Сравните поведение электронов с поведением других заряженных частиц, чтобы обнаружить такие свойства электронов, как заряд и масса.
Объем атомов
С учетом размеров протонов, нейтронов и электронов большая часть объема атома — более 99 процентов — фактически является пустым пространством. Несмотря на все это пустое пространство, твердые объекты не проходят сквозь друг друга. Электроны, окружающие все атомы, заряжены отрицательно и заставляют атомы отталкиваться друг от друга, не позволяя атомам занимать одно и то же пространство. Эти межмолекулярные силы не позволяют вам провалиться сквозь такой предмет, как стул.
Interactive: создайте атом : создайте атом из протонов, нейтронов и электронов и посмотрите, как изменяются элемент, заряд и масса. Тогда сыграйте в игру, чтобы проверить свои идеи!
Атомный номер и массовое число
Атомный номер — это количество протонов в элементе, а массовое число — это количество протонов плюс количество нейтронов.
Цели обучения
Определите соотношение между массовым числом атома, его атомным номером, его атомной массой и количеством субатомных частиц.
Ключевые выводы
Ключевые моменты
Ключевые термины
Атомный номер
Нейтральные атомы элемента содержат равное количество протонов и электронов. Число протонов определяет атомный номер элемента (Z) и отличает один элемент от другого.Например, атомный номер углерода (Z) равен 6, потому что у него 6 протонов. Количество нейтронов может изменяться для получения изотопов, которые представляют собой атомы одного и того же элемента, имеющие разное количество нейтронов. Число электронов также может быть различным в атомах одного и того же элемента, в результате чего образуются ионы (заряженные атомы). Например, железо Fe может существовать в нейтральном состоянии или в ионных состояниях +2 и +3.
Массовое число
Массовое число элемента (A) — это сумма количества протонов и количества нейтронов.Небольшой вклад массы электронов не учитывается при вычислении массового числа. Это приближение массы можно использовать, чтобы легко вычислить, сколько нейтронов имеет элемент, просто вычтя количество протонов из массового числа. Протоны и нейтроны весят около одной атомной единицы массы или а.е.м. Изотопы одного и того же элемента будут иметь одинаковый атомный номер, но разные массовые числа.
Атомный номер, химический символ и массовое число : Углерод имеет атомный номер шесть и два стабильных изотопа с массовыми числами двенадцать и тринадцать соответственно.Его средняя атомная масса 12,11.
Ученые определяют атомную массу, вычисляя среднее значение массовых чисел естественных изотопов. Часто полученное число содержит десятичную дробь. Например, атомная масса хлора (Cl) составляет 35,45 а.е.м., потому что хлор состоит из нескольких изотопов, некоторые (большинство) с атомной массой 35 а.е.м. (17 протонов и 18 нейтронов), а некоторые с атомной массой 37 а.е.м. (17 протонов и 20 нейтронов).
Зная атомный номер (Z) и массовое число (A), вы можете найти количество протонов, нейтронов и электронов в нейтральном атоме.Например, атом лития (Z = 3, A = 7 а.е.м.) содержит три протона (находится из Z), три электрона (поскольку количество протонов равно количеству электронов в атоме) и четыре нейтрона (7 — 3 = 4).
Изотопы
Изотопы — это различные формы элементов, которые имеют одинаковое количество протонов, но разное количество нейтронов.
Цели обучения
Обсудить свойства изотопов и их использование в радиометрическом датировании
Ключевые выводы
Ключевые моменты
Ключевые термины
Что такое изотоп?
Изотопы — это различные формы элементов, которые имеют одинаковое количество протонов, но разное количество нейтронов. Некоторые элементы, такие как углерод, калий и уран, содержат несколько изотопов природного происхождения. Изотопы определяются сначала их элементом, а затем суммой присутствующих протонов и нейтронов.
Хотя масса отдельных изотопов разная, их физические и химические свойства в основном не меняются.
Изотопы действительно различаются по стабильности. Углерод-12 ( 12 C) — самый распространенный изотоп углерода, составляющий 98,89% углерода на Земле. Углерод-14 ( 14 C) нестабилен и встречается только в следовых количествах.Нестабильные изотопы чаще всего испускают альфа-частицы (He 2+ ) и электроны. Также могут испускаться нейтроны, протоны и позитроны, а электроны могут быть захвачены для достижения более стабильной атомной конфигурации (более низкого уровня потенциальной энергии) посредством процесса, называемого радиоактивным распадом. Созданные новые атомы могут находиться в состоянии высокой энергии и испускать гамма-лучи, которые понижают энергию, но сами по себе не превращают атом в другой изотоп. Эти атомы называются радиоактивными изотопами или радиоизотопами.
Радиоуглеродное датирование
В живых организмах относительное количество 14 C в их теле примерно равно концентрации 14 C в атмосфере. Когда организм умирает, он больше не поглощает 14 C, поэтому соотношение между 14 C и 12 C будет снижаться по мере того, как 14 C постепенно возвращается к 14 N.Этот медленный процесс, который называется бета-распадом, высвобождает энергию за счет испускания электронов из ядра или позитронов.
Примерно через 5730 лет половина начальной концентрации 14 C будет преобразована обратно в 14 N. Это называется периодом полураспада, или временем, которое требуется для получения половины исходной концентрации вещества. изотоп, чтобы вернуться в более стабильную форму. Поскольку период полураспада 14 C большой, он используется для датирования ранее живых объектов, таких как старые кости или дерево.Сравнивая отношение концентрации 14 C, обнаруженной в объекте, к количеству 14 C в атмосфере, можно определить количество изотопа, который еще не распался. На основе этого количества можно точно рассчитать возраст материала, если предполагается, что возраст материала составляет менее 50 000 лет.
Как определить число нейтронов
В отличие от протонов, нейтроны не имеют электрического заряда, то есть их электрический заряд равен нулю. Поэтому, зная атомный номер элемента, нельзя однозначно сказать, сколько нейтронов содержится в его ядре. К примеру в ядре атома углерода всегда содержится 6 протонов, однако протонов в нем может быть 6 и 7. Разновидности ядер химического элемента с разным количеством нейтронов в ядре называются изотопами этого элемента. Изотопы могут быть как природными, так и полученными искусственно.
Зависимость числа нейтронов от числа протонов отражена на N-Z диаграмме атомных ядер. Устойчивость ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов наиболее устойчивы при N/Z = 1, то есть при равенстве количества нейтронов и протонов. С ростом массового числа область устойчивости сдвигается к величинам N/Z>1, достигая величины N/Z
1,5 для наиболее тяжелых ядер.
Как определить кол во протонов. Как найти нейтроны
Водород Ar = 1,001; 1 нуклон
Углерод Ar = 12,011; 12 нуклонов.
Нуклиды, изотопы, массовое число
Большинство элементов, содержащихся в природе, состоит из нескольких видов атомов, отличающихся значениями относительной атомной массы.
Пример. Хлор в природе встречается как смесь двух видов атомов, один из которых содержит 18, а другой – 20 нейтронов в ядре.
Изотопы элемента – это нуклиды, обладающие равным зарядом ядра (числом протонов). Изотопы элемента различаются только числом нейтронов и, следовательно, общим числом нуклонов.
Пример. Ядра двух природных изотопов хлора содержат по 17 протонов, но 18 и 20 нейтронов, т.е. 35 и 37 нуклонов соответственно.
Массовое число нуклида равно числу содержащихся в нем нуклонов (сумме протонов и нейтронов).
Массовое число = Число нуклонов в ядре.
Порядковый номер = Число протонов в ядре или число электронов в оболочке атома.
Разность между массовым числом и порядковым номером = Число нейтронов в ядре.
Строение электронной оболочки атома. Энергетические уровни
Строение электронной оболочки атома определяется различным запасом энергии E отдельных электронов в атоме. В соответствии с моделью атома Бора электроны могут занимать в атоме положения, которым отвечают точно определенные (квантованные) энергетические состояния.
Орбитальная модель атома
90 % получается та же орбитальная модель атома.
Атомная орбиталь – это геометрический образ, отвечающий объему пространства вокруг атомного ядра, который соответствует 90 %-ой вероятности нахождения в этом объеме электрона (как частицы) и одновременно 90 %-ой плотности заряда электрона (как волны).
Модель атомной орбитали (электронного облака) очень удобна для наглядного описания распределения электронной плотности в пространстве. При этом s-орбиталь имеет сферическую форму, р-орбиталь – форму гантели, d-орбиталь – четырехлепесткового цветка или удвоенной гантели, f-орбиталь – еще более сложную форму (рис. 3 ).
Если в атомной орбитали находится только один электрон (как в атоме водорода), то говорят об однократно занятой или полузаполненной, полузаселенной атомной орбитали. Если же в атомной орбитали находятся два электрона (как в атоме гелия), то говорят о двукратно занятой или полностью заполненной, полностью заселенной атомной орбитали. Полузаселенные АО играют важнейшую роль при формировании химических связей.
Спин – квантово-механическое свойство электрона, которое невозможно точно объяснить с помощью традиционных представлений на основе механического поведения макрочастиц. Без учета волновых свойств электрона спин можно интерпретировать путем сравнения электрона с шаром, вращающимся вокруг выбранной оси. Спин характеризует направление вращения и, следовательно, при двух возможных направлениях механического вращения должно существовать два разных спина электрона.
Спин – неотъемлемая характеристика электрона в атоме; два электрона на одной атомной орбитали обладают антипараллельными спинами.
Атомную орбиталь удобно изображать в виде квадрата, называемого квантовой ячейкой, а каждый электрон − вертикальной стрелкой, обозначающей один из двух возможных спинов электрона. Квантовая ячейка с одной стрелкой означает атомную орбиталь с одним электроном, т.е. полузаселенную орбиталь, с двумя стрелками − атомную орбиталь с двумя электронами, т.е. полностью заселенную орбиталь, без стрелок – вакантную орбиталь, т. е. без электронов.
Радиус атомной s-орбитали возрастает при увеличении номера энергетического уровня; 1s-АО расположена внутри 2s-АО, последняя – внутри 3s-АО и т.д. с центром, отвечающим атомному ядру. В целом строение электронной оболочки атома в орбитальной модели представляется слоистым. Каждый энергетический уровень, содержащий электроны, геометрически рассматривается как электронный слой.
Для сокращенного обозначения электрона, занимающего атомную s-орбиталь, используется обозначение самой s-АО с верхним цифровым индексом, указывающим число электронов. Например, 1s − обозначение единственного электрона атома водорода.
Электронная формула в сочетании с энергетической диаграммой электронной оболочки атома (рис. 3 ) отражают его электронную конфигурацию.
2.3. Энергетические подуровни
многоэлектронного атома. принципы
построения электронной оболочки
Квантово-механические расчеты показывают, что в многоэлектронных атомах энергия электронов одного уровня не одинакова; электроны заполняют атомные орбитали разных видов и имеют разную энергию.
Энергетический уровень характеризуется главным квантовым числом n. Для всех известных элементов значения n изменяются от 1 до 7. Электроны в многоэлектронном атоме, находящемся в основном (невозбужденном) состоянии, занимают энергетические уровни от первого до седьмого.
Под запросом «Как найти нейтроны» понимается метод поиска числа нейтронов в атоме. Нейтрон — это тяжелая частица, которая не имеет электрического заряда и вместе с протоном составляет атомное ядро элемента. Число нейтронов в атоме определяется с помощью таблицы Менделеева.
Как найти нейтроны — ищем число нейтронов в атомах
Как найти нейтроны — пример
М — атомная масса, n — атомный номер (число протонов), N — число нейтронов.
Как найти нейтроны — находим сколько нейтронов у изотопов
Как найти нейтроны — пример, изотоп О-17
Атомное ядро состоит из частиц с общим названием нуклоны. Известно два их вида – нейтроны и протоны. Количество нейтронов можно найти по массе атома, поскольку она практически равна массе атомного ядра (масса электронной оболочки пренебрежимо мала) и его заряду.
Вам понадобится
Инструкция
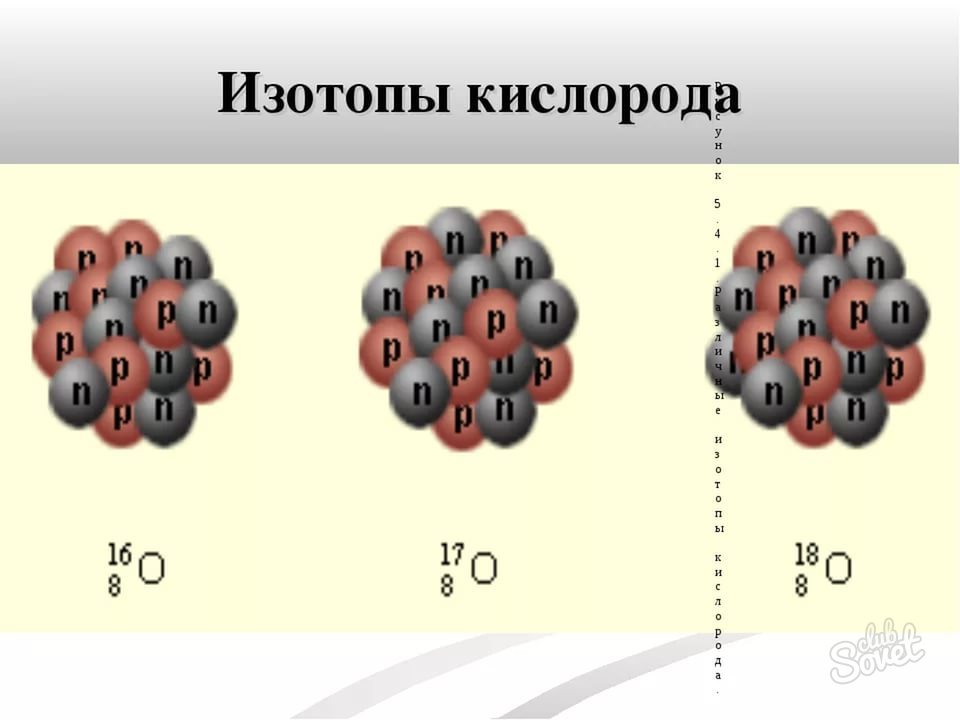
Для определенного изотопа всегда дается дополнительное пояснение. Перед обозначением элемента указывается его относительная атомная масса и порядковый номер в периодической таблице. В этом случае берите атомную массу, указанную в записи изотопа. Например, обычный кислород имеет массовое число 16 и порядковый номер 8, количество нейтронов в нем N=16-8=8. Его стабильный изотоп кислород-18, имеет соответствующее массовое число и количество нейтронов в ядре N=18-8=10.
Вам понадобится
Инструкция
В отличие от протонов, нейтроны не имеют электрического заряда, то есть их электрический заряд равен нулю. Поэтому, зная атомный номер элемента, нельзя однозначно сказать, сколько нейтронов содержится в его ядре. К примеру в ядре атома углерода всегда содержится 6 протонов, однако протонов в нем может быть 6 и 7. Разновидности ядер химического элемента с разным количеством нейтронов в ядре называются изотопами этого элемента. Изотопы могут быть как природными, так и полученными искусственно.
Зависимость числа нейтронов от числа протонов отражена на N-Z диаграмме атомных ядер. Устойчивость ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов наиболее устойчивы при N/Z = 1, то есть при равенстве количества нейтронов и протонов. С ростом массового числа область устойчивости сдвигается к величинам N/Z>1, достигая величины N/Z
Состав ядра атома. Расчет протонов и нейтронов
Согласно современным представлениям, атом состоит из ядра и расположенных вокруг него электронов. Ядро атома, в свою очередь, состоит из более малых элементарных частиц ‒ из определенного количества протонов и нейтронов (общепринятое название для которых – нуклоны), связанных между собой ядерными силами.
Количество протонов в ядре определяет строение электронной оболочки атома. А электронная оболочка определяет физико-химические свойства вещества. Число протонов соответствует порядковому номеру атома в периодической системе химических элементов Менделеева, именуется также зарядовое число, атомный номер, атомное число. Например, число протонов у атома Гелия – 2. В периодической таблице он стоит под номером 2 и обозначается как He2 Символом для обозначения количества протонов служит латинская буква Z. При записи формул зачастую цифра, указывающая на количество протонов, располагается снизу от символа элемента либо справа, либо слева: He2 / 2He.
ПРОЦЕСС РАСЧЁТА КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЧЕК ПО В ЯДРЕ АТОМА. В качестве примера мы не случайно рассмотрели Гелий-4 (He 4 2), ядро которого состоит из двух протонов и двух нейтронов. Поскольку ядро Гелия-4, именуемое альфа-частицей (α-частица) обладает наибольшей эффективностью в ядерных реакциях, его часто используют для экспериментов в этом направлении. Стоит отметить, что в формулах ядерных реакций зачастую вместо He 4 2 используется символ α.
Именно с участием альфа-частиц была проведена Э. Резерфордом первая в официальной истории физики реакция ядерного превращения. В ходе реакции α-частицами (He 4 2) «бомбардировались» ядра изотопа азота (N 14 7), вследствие чего образовался изотоп оксигена (O 17 8) и один протон (p 1 1)
Осуществим расчёт количества фантомных частичек По до и после данного преобразования.
ДЛЯ РАСЧЁТА КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЧЕК ПО НЕОБХОДИМО:
Шаг 1. Посчитать количество нейтронов и протонов в каждом ядре:
— количество протонов указано в нижнем показателе;
— количество нейтронов узнаем, отняв от общего массового числа (верхний показатель) количество протонов (нижний показатель).
Шаг 2. Посчитать количество фантомных частичек По в атомном ядре:
— умножить количество протонов на количество фантомных частичек По, содержащихся в 1 протоне;
— умножить количество нейтронов на количество фантомных частичек По, содержащихся в 1 нейтроне;
Шаг 3. Сложить количество фантомных частичек По:
— сложить полученное количество фантомных частичек По в протонах с полученным количеством в нейтронах в ядрах до реакции;
— сложить полученное количество фантомных частичек По в протонах с полученным количеством в нейтронах в ядрах после реакции;
— сравнить количество фантомных частичек По до реакции с количеством фантомных частичек По после реакции.
ПРИМЕР РАЗВЁРНУТОГО ВЫЧИСЛЕНИЯ КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЧЕК ПО В ЯДРАХ АТОМОВ.
(Ядерная реакция с участием α-частицы (He 4 2), провёденная Э. Резерфордом в 1919 году)
ДО РЕАКЦИИ (N 14 7 + He 4 2)
N 14 7
Количество протонов: 7
Количество нейтронов: 14-7 = 7
Количество фантомных частичек По:
в 1 протоне – 12 По, значит в 7 протонах: (12 х 7) = 84;
в 1 нейтроне – 33 По, значит в 7 нейтронах: (33 х 7) = 231;
Общее количество фантомных частичек По в ядре: 84+231 = 315
He 4 2
Количество протонов – 2
Количество нейтронов 4-2 = 2
Количество фантомных частичек По:
в 1 протоне – 12 По, значит в 2 протонах: (12 х 2) = 24
в 1 нейтроне – 33 По, значит в 2 нейтронах: (33 х 2) = 66
Общее количество фантомных частичек По в ядре: 24+66 = 90
Итого, количество фантомных частичек По до реакции
N 14 7 + He 4 2
315 + 90 = 405
ПОСЛЕ РЕАКЦИИ (O 17 8) и один протон (p 1 1):
O 17 8
Количество протонов: 8
Количество нейтронов: 17-8 = 9
Количество фантомных частичек По:
в 1 протоне – 12 По, значит в 8 протонах: (12 х 8) = 96
в 1 нейтроне – 33 По, значит в 9 нейтронах: (9 х 33) = 297
Общее количество фантомных частичек По в ядре: 96+297 = 393
p 1 1
Количество протонов: 1
Количество нейтронов: 1-1=0
Количество фантомных частичек По:
В 1 протоне – 12 По
Нейтроны отсутствуют.
Общее количество фантомных частичек По в ядре: 12
Итого, количество фантомных частичек По после реакции
(O 17 8 + p 1 1):
393 + 12 = 405
Сравним количество фантомных частичек По до и после реакции:
| До реакции | После реакции |
| 405 | 405 |
Количества фантомных частичек По до и после реакции равны.
ПРИМЕР СОКРАЩЁННОЙ ФОРМЫ ВЫЧИСЛЕНИЯ КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЧЕК ПО В ЯДЕРНОЙ РЕАКЦИИ.
Здесь и далее расчёты количества фантомных частичек По приведены в сокращённой форме, в которой отображено общее количество фантомных частичек По в каждом ядре, а также их сумма до и после реакции.
Известной ядерной реакцией является реакция взаимодействия α-частиц с изотопом бериллия, прикоторой впервые был обнаружен нейтрон, проявивший себя как самостоятельная частица в результате ядерного преобразования. Данная реакция была осуществлена в 1932 году английским физиком Джеймсом Чедвиком. Формула реакции:
Количества фантомных частичек По до и после реакции равны.
Школьная энциклопедия. Портал знаний
Как определить протоны и нейтроны по таблице. Как найти нейтроны
Под запросом «Как найти нейтроны» понимается метод поиска числа нейтронов в атоме. Нейтрон — это тяжелая частица, которая не имеет электрического заряда и вместе с протоном составляет атомное ядро элемента. Число нейтронов в атоме определяется с помощью таблицы Менделеева.
Как найти нейтроны — ищем число нейтронов в атомах
Как найти нейтроны — пример
М — атомная масса, n — атомный номер (число протонов), N — число нейтронов.
Как найти нейтроны — находим сколько нейтронов у изотопов
Как найти нейтроны — пример, изотоп О-17
Водород Ar = 1,001; 1 нуклон
Углерод Ar = 12,011; 12 нуклонов.
Нуклиды, изотопы, массовое число
Большинство элементов, содержащихся в природе, состоит из нескольких видов атомов, отличающихся значениями относительной атомной массы.
Пример. Хлор в природе встречается как смесь двух видов атомов, один из которых содержит 18, а другой – 20 нейтронов в ядре.
Изотопы элемента – это нуклиды, обладающие равным зарядом ядра (числом протонов). Изотопы элемента различаются только числом нейтронов и, следовательно, общим числом нуклонов.
Пример. Ядра двух природных изотопов хлора содержат по 17 протонов, но 18 и 20 нейтронов, т.е. 35 и 37 нуклонов соответственно.
Массовое число нуклида равно числу содержащихся в нем нуклонов (сумме протонов и нейтронов).
Массовое число = Число нуклонов в ядре.
Порядковый номер = Число протонов в ядре или число электронов в оболочке атома.
Разность между массовым числом и порядковым номером = Число нейтронов в ядре.
Строение электронной оболочки атома. Энергетические уровни
Строение электронной оболочки атома определяется различным запасом энергии E отдельных электронов в атоме. В соответствии с моделью атома Бора электроны могут занимать в атоме положения, которым отвечают точно определенные (квантованные) энергетические состояния.
Орбитальная модель атома
90 % получается та же орбитальная модель атома.
Атомная орбиталь – это геометрический образ, отвечающий объему пространства вокруг атомного ядра, который соответствует 90 %-ой вероятности нахождения в этом объеме электрона (как частицы) и одновременно 90 %-ой плотности заряда электрона (как волны).
Модель атомной орбитали (электронного облака) очень удобна для наглядного описания распределения электронной плотности в пространстве. При этом s-орбиталь имеет сферическую форму, р-орбиталь – форму гантели, d-орбиталь – четырехлепесткового цветка или удвоенной гантели, f-орбиталь – еще более сложную форму (рис. 3 ).
Если в атомной орбитали находится только один электрон (как в атоме водорода), то говорят об однократно занятой или полузаполненной, полузаселенной атомной орбитали. Если же в атомной орбитали находятся два электрона (как в атоме гелия), то говорят о двукратно занятой или полностью заполненной, полностью заселенной атомной орбитали. Полузаселенные АО играют важнейшую роль при формировании химических связей.
Спин – квантово-механическое свойство электрона, которое невозможно точно объяснить с помощью традиционных представлений на основе механического поведения макрочастиц. Без учета волновых свойств электрона спин можно интерпретировать путем сравнения электрона с шаром, вращающимся вокруг выбранной оси. Спин характеризует направление вращения и, следовательно, при двух возможных направлениях механического вращения должно существовать два разных спина электрона.
Спин – неотъемлемая характеристика электрона в атоме; два электрона на одной атомной орбитали обладают антипараллельными спинами.
Атомную орбиталь удобно изображать в виде квадрата, называемого квантовой ячейкой, а каждый электрон − вертикальной стрелкой, обозначающей один из двух возможных спинов электрона. Квантовая ячейка с одной стрелкой означает атомную орбиталь с одним электроном, т.е. полузаселенную орбиталь, с двумя стрелками − атомную орбиталь с двумя электронами, т.е. полностью заселенную орбиталь, без стрелок – вакантную орбиталь, т. е. без электронов.
Радиус атомной s-орбитали возрастает при увеличении номера энергетического уровня; 1s-АО расположена внутри 2s-АО, последняя – внутри 3s-АО и т.д. с центром, отвечающим атомному ядру. В целом строение электронной оболочки атома в орбитальной модели представляется слоистым. Каждый энергетический уровень, содержащий электроны, геометрически рассматривается как электронный слой.
Для сокращенного обозначения электрона, занимающего атомную s-орбиталь, используется обозначение самой s-АО с верхним цифровым индексом, указывающим число электронов. Например, 1s − обозначение единственного электрона атома водорода.
Электронная формула в сочетании с энергетической диаграммой электронной оболочки атома (рис. 3 ) отражают его электронную конфигурацию.
2.3. Энергетические подуровни
многоэлектронного атома. принципы
построения электронной оболочки
Квантово-механические расчеты показывают, что в многоэлектронных атомах энергия электронов одного уровня не одинакова; электроны заполняют атомные орбитали разных видов и имеют разную энергию.
Энергетический уровень характеризуется главным квантовым числом n. Для всех известных элементов значения n изменяются от 1 до 7. Электроны в многоэлектронном атоме, находящемся в основном (невозбужденном) состоянии, занимают энергетические уровни от первого до седьмого.
Атомное ядро состоит из частиц с общим названием нуклоны. Известно два их вида – нейтроны и протоны. Количество нейтронов можно найти по массе атома, поскольку она практически равна массе атомного ядра (масса электронной оболочки пренебрежимо мала) и его заряду.
Вам понадобится
Инструкция
Для определенного изотопа всегда дается дополнительное пояснение. Перед обозначением элемента указывается его относительная атомная масса и порядковый номер в периодической таблице. В этом случае берите атомную массу, указанную в записи изотопа. Например, обычный кислород имеет массовое число 16 и порядковый номер 8, количество нейтронов в нем N=16-8=8. Его стабильный изотоп кислород-18, имеет соответствующее массовое число и количество нейтронов в ядре N=18-8=10.
Вам понадобится
Инструкция
В отличие от протонов, нейтроны не имеют электрического заряда, то есть их электрический заряд равен нулю. Поэтому, зная атомный номер элемента, нельзя однозначно сказать, сколько нейтронов содержится в его ядре. К примеру в ядре атома углерода всегда содержится 6 протонов, однако протонов в нем может быть 6 и 7. Разновидности ядер химического элемента с разным количеством нейтронов в ядре называются изотопами этого элемента. Изотопы могут быть как природными, так и полученными искусственно.
Зависимость числа нейтронов от числа протонов отражена на N-Z диаграмме атомных ядер. Устойчивость ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов наиболее устойчивы при N/Z = 1, то есть при равенстве количества нейтронов и протонов. С ростом массового числа область устойчивости сдвигается к величинам N/Z>1, достигая величины N/Z
Как определить кол во протонов и нейтронов – «Как узнать сколько протонов, нейтронов и электронов находится в атоме фтора?» – Яндекс.Знатоки
Как определить число нейтронов — как определить число протонов и нейтронов в ядре. — 22 ответа
число протонов
В разделе Образование на вопрос как определить число протонов и нейтронов в ядре. заданный автором Простричь лучший ответ это Число протонов и число электронов в атоме равны порядковому номеру элемента (заряду ядра). Число нейтронов=атомная масса (Ar,указана в таблице Менделеева) — число протонов (т. е. заряд ядра). Например, у бериллия заряд ядра 4(т. е. его порядковый номер 4).Значит, протонов у него 4,электронов тоже 4,нейтронов = 9 — 4 = 5 (где 9 — округленная атомная масса, 4 — число протонов).
Ответ от 22 ответа[гуру]
Привет! Вот подборка тем с ответами на Ваш вопрос: как определить число протонов и нейтронов в ядре.
Ответ от Босоножка[активный]
порядковый номер в таблице менделева-протоны
масса ядра в а. е. м. — кол-во протонов = кол-во нейтронов
Ответ от Ѝдуард Фиш[гуру]
Линейная зависимость числа протонов от числа нейтронов определяет следующую простую закономерность …
Номер кругооборота определяет количество нейтронов, которое приходится на два протона в ядрах …
– 22,749 байт
Ответ от Михаил Михаил[гуру]
протов стока какой номер в таблице менделеева, протонов разница между округленным значением молеклурной массы и номер данного элементы в таблице менделеева
Ответ от Вровень[гуру]
Посмотри таблицу Менделеева. Там дается атомный вес и порядковый номер элемента. Порядковый номер — это число протонов. Число нейтронов = из атомного веса (округлить) вычесть порядковый номер элемента.
Ответ от °•°°•°°•[email protected]@°°°•°[активный]
протоны-а. е. м, нейтроны-а. ем-протоны
Ответ от Наталия Александрова[новичек]
да вычесть то можно. только атомный вес это среднее значение массы изотопов. а изотопы определяются разным количеством нейтронов
Ответ от Slava mikailov[новичек]
Ответ от Ёергий Корвинус[новичек]
Порядковый номер это исчисление, номирование. с 1 и тогдалее по количеству протонов
Ответ от МИЛЕДИ[новичек]
я мля
Ответ от Лаурка[активный]
а как потом найти новый химический элемент?
фтор
Ответ от Dima galayda[новичек]
Число протонов и число электронов в атоме равны порядковому номеру элемента (заряду ядра). Число нейтронов=атомная масса (Ar,указана в таблице Менделеева) — число протонов (т. е. заряд ядра). Например, у бериллия заряд ядра 4(т. е. его порядковый номер 4).Значит, протонов у него 4,электронов тоже 4,нейтронов = 9 — 4 = 5 (где 9 — округленная атомная масса, 4 — число протонов).
Ответ от Мурад Вагидов[новичек]
число протонов и электронов равно числу порядкового номера. А чтобы найти число нейтронов нужно из относительной атомной массы вычесть заряд ядра (порядковый номер)
Ответ от 2 ответа[гуру]
Привет! Вот еще темы с нужными ответами:
Атом на Википедии
Посмотрите статью на википедии про Атом
Атомное ядро на Википедии
Посмотрите статью на википедии про Атомное ядро
Зарядовое число на Википедии
Посмотрите статью на википедии про Зарядовое число
Количество вещества на Википедии
Посмотрите статью на википедии про Количество вещества
Нейтрон на Википедии
Посмотрите статью на википедии про Нейтрон
Протон на Википедии
Посмотрите статью на википедии про Протон
Пушкин Александр Сергеевич на Википедии
Посмотрите статью на википедии про Пушкин Александр Сергеевич
Мастер и Маргарита мюзикл 2014 на Википедии
Посмотрите статью на википедии про Мастер и Маргарита мюзикл 2014
Ответить на вопрос:
Как найти число протонов, нейтронов и электронов Как? Так!
Протоны, нейтроны и электроны – основные частицы, из которых состоит атом. Протоны заряжены положительно, электроны – отрицательно, а нейтроны и вовсе не имеют заряда. Масса электронов очень мала, а масса протонов и нейтронов практически одинакова. На самом деле, найти в атоме количество протонов, нейтронов и электронов довольно просто, нужно только научиться ориентироваться по периодической таблице химических элементов Д.И.Менделеева.
Часть 1 Как найти чисто протонов, электронов и нейтронов
Часть 2 Расчет электронов с присутствующими ионами
как определить число протонов,электронов и нейтронов в атомах например натрия?можете объяснить как это сделать на любом
как определить число протонов,электронов и нейтронов в атомах например натрия?можете объяснить как это сделать на любом
больше 1года назад
Войдите что бы оставлять комментарии
Число электронов= порядковый номер Протонов= атомная масса Нейтронов = Протонов — электронов
ответ написан больше 1года назад
не знаешь не пиши
комментарий написан больше 1года назад
комментарий написан больше 1года назад
атомную массу составляю массы и протов и нейтронов
комментарий написан больше 1года назад
Войдите что бы оставлять комментарии
Число протонов=порядковому номеру в табл. Менделеева число электронов=числу протонов, но со знаком — число нейтронов=атомная масса элемента (найдешь в таблице) — порядковый номер.
ответ написан больше 1года назад
Войдите что бы оставлять комментарии
нейтроны = относительно атомная масса- порядковый номер mg n=24-12 электроны и протоны численно =порядковому номеру mg p=12 е=12
ответ написан больше 1года назад
Войдите что бы оставлять комментарии
Для того чтобы определить количество протонов и электронов, мы можем вспомнить, что число электронов равна порядковому номеру например: S-сера. У серы порядковый номер=16, значить количество прот. и электр. =15 А чтобы найти нейтроны, нам нужно из массы-16. 32-16=16 Я надеюсь, что я вам помогла))))))))
ответ написан больше 1года назад
комментарий написан больше 1года назад
Войдите что бы оставлять комментарии
Возьмем любой элемент, например, ФОСФОР (P) Чтобы определить количество протонов и электронов, смотрим на порядковый номер элемента в таблице Менделеева. Он 15-й. Количество протонов и эелектронов = порядковый номер элемента. Значит. p=15 e=15 Теперь нейтроны. Из массвового числа элемента вычитаем порядк номер. Массовое число также из таблицы: у фосфора это 30,9 приблизительно 31 n=31-15=16.
Как найти число нейтронов
Атомный калькулятор представляет собой инструмент для расчета атомного номера и массового числа на основе количества компонентов атома — протонов, нейтронов и электронов (или наоборот).
Кроме того, вы можете определить заряд ионов с известным числом протонов и электронов. Статья ниже предоставит вам определение атома, компонентов атома, атомного номера и массового числа, а также краткое пошаговое руководство о том, как рассчитать количество компонентов атома.
Атом — это наименьшая составляющая единица материи, которая сохраняет свойства элемента. Типичный атом состоит из ядра и электронного облака. Компоненты атома — это положительно заряженные протоны и электрически нейтральные нейтроны в ядре, а также отрицательно заряженные электроны, вращающиеся вокруг этого ядра. Протоны и нейтроны называются нуклонами.
Атомы электрически нейтральны, потому что они имеют равное количество электронов и протонов. Однако, когда атом имеет неодинаковое количество протонов и электронов, он имеет электрический заряд, и они создают ионы. Если ион имеет больше протонов, чем электронов, он заряжен положительно и называется катионом. И наоборот, если ион имеет больше электронов, чем электронов, он отрицательно заряжен и называется анионом.
Некоторые атомы могут расщепляться на более мелкие части (более легкие ядра). Если вы хотите знать период полураспада, вы можете использовать Калькулятор периода полураспада, чтобы рассчитать количество ядер, оставшихся после определенного времени.
Атомный номер, атомная масса
Атом уникально идентифицируется с атомным номером (символ Z). Атомный номер — это число протонов, присутствующих в ядре. В случае незаряженных атомов атомный номер равен числу электронов. Напротив, в ионах число электронов является разностью между атомным номером и зарядом ионов. В катионах электронов меньше, чем протонов, а в анионах больше электронов, чем протонов.
Число нейтронов в данном элементе, однако, может варьироваться. Варианты одного и того же химического элемента с разным количеством нейтронов называются изотопами. Протоны и нейтроны определяют массу атома. Массовое число (символ А) представляет собой сумму чисел протонов и нейтронов.
Как рассчитать атомный номер, атомную массу и заряд или количество протонов, нейтронов и электронов? — полезные уравнения
Если вы знаете атомный номер (Z), атомную массу (A) и заряд (z), вы можете рассчитать число протонов (p), нейтронов (n) и электронов (e) по заданным математическим уравнениям (1-3):
С другой стороны, если вам известны числа протонов (p), нейтронов (n) и электронов (e), вы можете рассчитать атомный номер (Z), атомную массу (A) и заряд (z) (уравнения (4-6) )):
Как рассчитать атомный номер, атомную массу и заряд или количество протонов, нейтронов и электронов?
Выберите свой элемент. Предположим, что это атом натрия (Na). Заряд 0.
Найдите атомный номер (Z) и массовое число (A). Они равны 11 и 23 соответственно.
Рассчитайте количество протонов, нейтронов и электронов, используя математические выражения (1-3):
р = 11
Кроме того, вы также можете рассчитать атомный номер, атомную массу и заряд.
Выберите свой элемент. Давайте предположим, что это сульфид-анион (S 2- — анион серы).
Найти количество протонов, нейтронов и электронов. Они равны 16, 16 и 18 соответственно.
Рассчитайте атомный номер, атомную массу и заряд, используя математические выражения (4-6):
Z = 16
Конечно, вам не нужно выполнять все эти вычисления вручную! Введите любые три значения в этот калькулятор атомов и посмотрите, как он сделает всю работу за вас.
Пособие-репетитор по химии
ЗАНЯТИЕ 3
10-й класс (первый год обучения)
Продолжение. Начало см. в № 22,/2005; 1/2006
Современные представления о строении атома

| Частица | Обозначение | Заряд | Относительная атомная масса |
|---|---|---|---|
| Протон | p | + | 1 |
| Нейтрон | n | 0 | 1 |
| Электрон | e | – | 1/1840 |
После открытия основных элементарных частиц, входящих в состав атома, встал вопрос об их местонахождении, т.е. о строении атома. В 1911 г. Томсон предложил свою модель строения атома, которая получила условное название «пудинг с изюмом». Согласно этой модели атом представляет собой некую субстанцию, в которой равномерно распределены протоны, нейтроны и электроны. Число протонов равно числу электронов, поэтому атом в целом электронейтрален.
В 1913 г. Резерфорд ставит опыт, результаты которого модель Томсона объяснить не может (рис.).Это заставляет Резерфорда предложить свою модель строения атома, получившую название планетарной. Согласно этой модели атом состоит из ядра, в котором сконцентрирована основная масса атома, поскольку ядро содержит протоны и нейтроны; вокруг ядра на огромной скорости вращаются электроны. Поскольку модель Резерфорда содержала ряд противоречий, Н.Бором были введены постулаты, устраняющие эти противоречия.
Рис.
Схема установки в опыте Резерфорда:
1 – источник  -излучения;
-излучения;
2 – золотая фольга;
3 – экран с покрытием из сульфида цинка
1-й постулат. Электроны вращаются вокруг ядра не по произвольным, а по строго определенным, стационарным орбитам.
2-й постулат. При движении по стационарной орбите электрон не излучает и не поглощает энергию. Изменение энергии происходит при переходе электрона с одной стационарной орбиты на другую.
Но теория Резерфорда–Бора дает удовлетворительные результаты только для атома водорода. Современные представления о строении атома подчиняются квантовой модели строения атома, которая учитывает волновые свойства элементарных частиц. Приведем ее основные положения.
 | ||||||||||||
 | |||||||||||
| Элемент |  | Ar |
|---|---|---|
| Na | 29,11% | 23 |
| S | 40,51% | 32 |
| O | 30,38% | 165 |
Разделим все три числа соотношения на наименьшее (1,266), получим простое соотношение: 1 : 1: 1,5. Умножим все три числа на 2, получим: 2 : 2 : 3. Отсюда формула вещества – Na2S2O3.
1. Определить формулу вещества, состоящего из кислорода, азота, фосфора и водорода, если известно, что оно содержит 48,5% кислорода; количество атомов азота в нем в 2 раза больше количества атомов фосфора, а количество атомов водорода – в 2,25 раза больше количества атомов кислорода. Молярная масса вещества меньше 200 г/моль.
2. Неизвестная соль содержит элемент X, а также водород, азот и кислород в следующем массовом соотношении: 12 : 5 : 14 : 48 (в порядке перечисления). Определить формулу соли.
Ответ. Гидрокарбонат аммония NH4HCO3.
3. Написать формулу углеводорода, в котором масса углерода равна массе водорода.
4. В порции кристаллогидрата ацетата калия содержится 3,612•10 23 атомов углерода и 1,084•10 24 атомов водорода. Установить формулу кристаллогидрата.









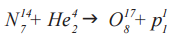
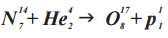
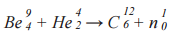


 -излучения;
-излучения; 




 1. Число протонов в атоме элемента, который находится в четвертом периоде и в главной подгруппе
1. Число протонов в атоме элемента, который находится в четвертом периоде и в главной подгруппе  -распадов включает эта серия ядерных превращений?
-распадов включает эта серия ядерных превращений? (Fe) в FeO – 77,8%.
(Fe) в FeO – 77,8%.
