Что такое щелочь
Щёлочи
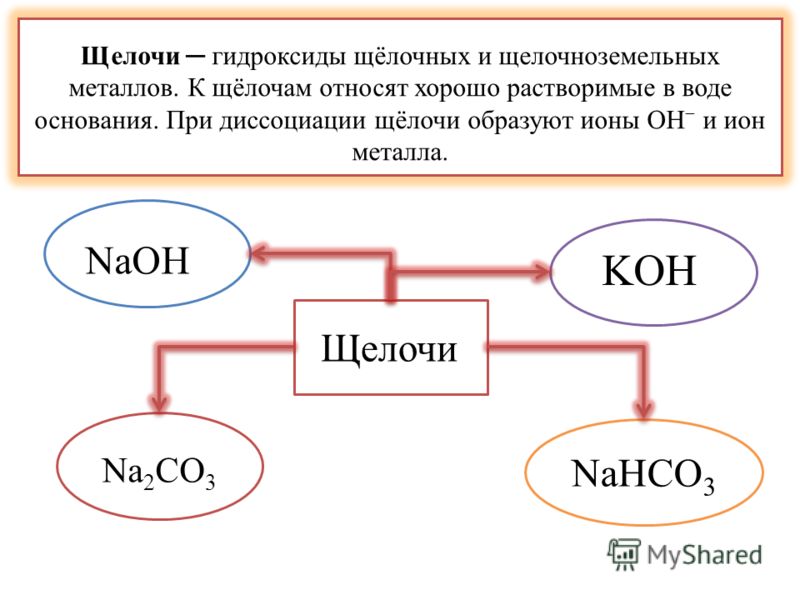
Щёлочи — гидроксиды щелочных, щёлочноземельных металлов и аммония. К щёлочам относят хорошо растворимые в воде основания. При диссоциации щёлочи образуют анионы OH − и катион металла.
К щёлочам относятся гидроксиды металлов подгрупп Iа и IIа (начиная с кальция) периодической системы, например NaOH (едкий натр), KOH (едкое кали), Ba(OH)2 (едкий барит). Едкие щёлочи — тривиальное название гидроксидов лития LiOH, натрия NaOH, калия КОН, рубидия RbOH, и цезия CsOH.
Физические свойства
Гидроксиды щелочных металлов (едкие щёлочи) представляют собой твёрдые, белые, очень гигроскопичные вещества. Щёлочи — сильные основания, очень хорошо растворимые в воде, причём реакция сопровождается значительным тепловыделением. Сила основания и растворимость в воде возрастает с увеличением радиуса катиона в каждой группе периодической системы. Самые сильные щёлочи — гидроксид цезия в группе Ia и гидроксид радия в группе IIa. Кроме того, едкие щёлочи растворимы в этаноле и метаноле.
Химические свойства
В твёрдом состоянии все щёлочи поглощают H2O из воздуха, а также CO2 (также и в состоянии раствора) из воздуха, постепенно превращаясь в карбонаты. Щёлочи широко применяются в промышленности. Важное химическое свойство щелочей — способность образовывать соли в реакции с кислотами.
Получение
Получают путём электролиза хлоридов щелочных металлов или действием воды на оксиды щелочных металлов.
Полезное
Смотреть что такое «Щёлочи» в других словарях:
не содержащий щёлочи — свободный от щёлочи — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы свободный от щёлочи EN alkali free … Справочник технического переводчика
Щёлочи — ЩЁЛОЧИ, гидроксиды щелочных (едкие щёлочи) и щёлочноземельных металлов. Щелочи сильные основания; едкие щелочи хорошо растворяются в воде, гидроксиды щёлочноземельных металлов плохо. Все щелочи чрезвычайно агрессивны, их растворы разрушают стекло … Иллюстрированный энциклопедический словарь
Едкие щёлочи — хорошо растворимые в воде гидроокиси щелочных металлов, например едкий натр NaOH, едкое кали КОН. Оказывают разъедающее действие на слизистые оболочки и кожу. Широко применяются во многих отраслях промышленности. См. Щёлочи … Большая советская энциклопедия
Щёлочи — (хим.) В настоящее время говорят почти исключительно обедких щёлочах, но прежде под Щ. разумели вообще вещества, растворы коихимеют щелочную реакцию и вкус. К числу Щ. относили тогда и карбонатыщелочных металлов. Сода и поташ, например, имеют… … Энциклопедия Брокгауза и Ефрона
ЩЁЛОЧИ — гидроксиды щелочных металлов (Li, Na, K, Rb, Cs, Fr) и щёлочноземельных металлов (Ca, Sr, Ba, Ra) (I и II группы периодической системы Д. И. Менделеева). Щ. твердые белые гигроскопические вещества. При их растворении в воде выделяется большое… … Российская энциклопедия по охране труда
заводнение раствором щёлочи — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN alkaline waterflooding … Справочник технического переводчика
оборудование для закачивания щёлочи (в пласт) — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN caustic flooding equipment … Справочник технического переводчика
раствор щёлочи — отработанная щёлочь щелочные отбросы — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы отработанная щёлочьщелочные отбросы EN alkali liquor … Справочник технического переводчика
устройство для распределения щёлочи в фильтре регенерации анионита — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN anion regeneration tank caustic distributor … Справочник технического переводчика
Щелочь
Щёлочи — гидроксиды щелочных и щёлочноземельных металлов. К щелочам относят растворимые в воде основания. При диссоциации щелочи образуют ионы OH- и ион металла.
К щелочам относятся гидроксиды металлов подгрупп Iа и IIа периодической системы, например NaOH(едкий натрий), KOH (едкий калий), Ba(OH)2 (едкий барий). Едкие щелочи — тривиальное название гидроксидов лития LiOH, натрия NaOH, калия КОН, рубидия RbOH, и цезия CsOH.
Физические свойства
Химические свойства
Поглощают H2O и CO2 из воздуха. Щёлочи широко применяются в промышленности. Важное химическое свойство щелочей — способность образовывать соли в реакции с кислотами.
Получение
Получают путём электролиза хлоридов щелочных металлов или действием воды на оксиды щелочных металлов.
Полезное
Смотреть что такое «Щелочь» в других словарях:
щелочь — сущ., кол во синонимов: 4 • алкали (1) • злюка (30) • каустик (1) • щёлочь (1) … Словарь синонимов
щелочь — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN alkali … Справочник технического переводчика
щелочь — šarmas statusas T sritis chemija atitikmenys: angl. alkali; alkaline solution; lye rus. щелок; щелочь ryšiai: sinonimas – šarminis tirpalas … Chemijos terminų aiškinamasis žodynas
щелочь — šarmas statusas T sritis chemija apibrėžtis Vandenyje tirpus šarminio ar šarminių žemių metalo hidroksidas. atitikmenys: angl. alkali rus. щелочь … Chemijos terminų aiškinamasis žodynas
Щелочь — щёлочь ж. Едкое, хорошо растворимое в воде химическое соединение, при взаимодействии которого с кислотами образуются соли, а при погружении в него лакмусовая бумажка окрашивается в синий цвет. Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
щелочь — ЩЁЛОЧЬ и; мн. род. щелочей; ж. Едкое, хорошо растворимое в воде химическое соединение, окрашивающее лакмусовую бумагу в синий цвет (при взаимодействии его с кислотами образуются соли) … Энциклопедический словарь
щелочь — з.б.п., чы, чæй, чьмæ … Орфографический словарь осетинского языка
Амарин щелочь — Амарин C 21H18N2 искусственная органическая щелочь, напоминающая по некоторым свойствам растительные алкалоиды; получается при обработке аммиаком спиртового раствора бензойного альдегида или же простым нагреванием около 120 130° изомерного с ним… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Амарин, щелочь — Амарин C21H18N2 искусственная органическая щелочь, напоминающая по некоторым свойствам растительные алкалоиды; получается при обработке аммиаком спиртового раствора бензойного альдегида или же простым нагреванием около 120 130° изомерного с ним… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
летучая щелочь — сущ., кол во синонимов: 1 • нашатырь (6) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Щелочь
Производство широкого спектра потребительских товаров зависит от использования щелочей 
Немного исторических моментов из истории получения щелочи.
Лебланский способ производства доминировал в мировом производстве до конца 19-го века, но после первой мировой войны был полностью вытеснен другим методом конверсии соли, который был усовершенствован в 1860-х годах Эрнестом Солве из Бельгии. В конце XIX века появились электролитические методы производства каустической соды, объемы которых быстро росли.
По методу Солве, аммиачно-содовый процесс производства кальцинированной соды протекал следующим образом: поваренная соль в виде сильного рассола химически обрабатывалась для устранения примесей кальция и магния и затем насыщалась рециркулирующим газом аммиака в башнях. После, аммиачный рассол насыщался газом с использованием газообразного диоксида углерода при умеренном давлении в башне другого типа. Эти два процесса дают бикарбонат аммония и хлорид натрия, двойное разложение которого дает желаемый бикарбонат натрия, а также хлорид аммония. Затем бикарбонат натрия нагревают до разложения его до необходимого карбоната натрия. Аммиак, вовлеченный в процесс, почти полностью восстанавливается путем обработки хлоридом аммония с известью, с получением аммиака и хлорида кальция. Восстановленный аммиак затем повторно используют в описанных выше процессах.
В нескольких местах в мире существуют значительные запасы минеральной формы кальцинированной соды, известной как природная щелочь. На таких месторождениях производят большую часть природной щелочи в мире из обширных месторождений в подземных шахтах.
Природный натрий металлический.
Прочитайте статью Щелочи (источник «Энциклопедический словарь химика»)и получите больше представления о том что такое щелочь, или посмотрите видеоролик об этом химическом реактиве Щелочи.
Использование щелочи в окружающей нас среде
Щелочь снискала широкое применение в нашей жизни. Благодаря щелочи можно в той или иной форме добиться смягчения воды и удалить из нее примеси, такие как марганец, фториды и органические танины. В тяжелых отраслях промышленности используют щелочь в виде извести для поглощения и нейтрализации оксидов серы в выбросах в атмосферу, тем самым уменьшая вероятность выпадения кислотных осадков. Диоксид серы, производимый промышленными предприятиями и выпускаемый в атмосферу, возвращается на землю в виде кислотных дождей или серной кислоты. Такие территории, подвергшихся воздействию кислотных дождей, обрабатываются с помощью авиации препаратами, в состав которых входит щелочь. Это позволяет контролировать и нейтрализовывать критический уровень рН воды и почвы на участках, где произошли такие техногенные выбросы. Внесение щелочи в отходы и сточные воды, поддерживая правильный уровень рН в окислительных процессах при их разложении. Стабилизирует образования осадка в сточных водах и уменьшает запах или образования патогенных бактерий. Обработанный негашеной известью ил из сточных водоемов, соответствует экологическим нормам, что делает его пригодным в дальнейшем в использовании в качестве удобрения на сельскохозяйственных землях.
Промышленное применение щелочи
В промышленных и горных работах применение щелочей в сточных водах помогает нейтрализовать вредные соединения и произвести их очистку. Обработка избыточной щелочью, повышает рН воды до 10,5-11 и может дезинфицировать воду и удалять тяжелые металлы. Щелочи, такие как известь, являются ключевыми в химическом производстве карбида кальция, лимонной кислоты, нефтехимии и магнезии. В бумажной промышленности карбонат кальция является каустифицирующим агентом для отбеливания. Сталелитейная промышленность зависит от извести в качестве компонента для удаления примесей, таких как газообразный монооксид углерода, кремния, марганца и фосфора.
Моющие средства образованные щелочью
Щелочные моющие средства помогают при очистке поверхностей с сильными загрязнениями. Эти экономичные, водорастворимые щелочи с рН от 9 до 12,5 могут нейтрализовать кислоты в различных типах грязи и отложениях.
Щелочь в производстве стекла и керамики
Щелочь является основным сырьем в производстве стекла. Известняк, а также песок, кальцинированная сода, известь и другие химикаты, обжигаются при чрезвычайно высоких температурах и превращаются в расплавленную массу. Стеклодувы и гончары используют щелочи для глазурей и флюсов, которые реагируют с кислотами с образованием силикатов (стекла) при нагревании. Концентрированные щелочи создают более насыщенный цвет в глазури.
Литература о щелочи
«Среди многочисленных веществ, которыми химики с давних времен пользовались в своих лабораториях, почетное место всегда занимали едкие щелочи — едкое кали и едкий натр. Сотни различных химических реакций осуществляются в лабораториях, на заводах и в быту при участии щелочей. С помощью едких кали и натра можно, например, сделать растворимыми большинство нерастворимых веществ, а самые сильные кислоты и удушливые пары можно благодаря щелочам лишить всей их жгучести и ядовитости.
Едкие щелочи — очень своеобразные вещества. На вид это беловатые, довольно твердые камни, ничем как будто не примечательные. Но попробуйте взять едкое кали или натр и зажать его в руке. Вы почувствуете легкое жжение, почти как от прикосновения к крапиве. Долго держать в руке едкие щелочи было бы нестерпимо больно: они могут разъесть кожу и мясо до кости. Вот почему их называют «едкими», в отличие от других, менее «злых» щелочей — всем известных соды и поташа. Из соды и поташа, кстати сказать, почти всегда и по лучались едкие натр и кали.
У едких щелочей сильнейшее влечение к воде. Оставьте кусок совершенно сухого едкого кали или натра на воздухе. Через короткое время на его поверхности неизвестно откуда появится жидкость, потом он весь станет мокрым и рыхлым и под конец расползется бесформенной массой, как кисель. Это из воздуха щелочь притягивает к себе пары воды и образует с влагой густой раствор. Кому впервые приходится погрузить пальцы в раствор едкой щелочи, тот с удивлением заявляет: — Как мыло! И это совершенно правильно. Щелочь — скользкая, как мыло. Больше того: мыло потому и «мыльно» на ощупь, что его изготовляют с помощью щелочей. Раствор едкой щелочи и на вкус напоминает мыло.
Но химик узнаёт едкую щелочь не по вкусу, а по тому, как это вещество ведет себя с краской лакмус и с кислотами. Бумажка, про питанная синей краской лакмус, мгновенно краснеет, когда ее опус кают в кислоту; а если этой покрасневшей бумажкой дотронуться до щелочи, то она тотчас же опять становится синей. Едкая щелочь и кислота не могут мирно существовать рядом ни одной секунды. Они тотчас же вступают в бурную реакцию, шипя и разогреваясь, и уничтожают друг друга до тех пор, пока в растворе не останется ни крупинки щелочи или ни капли кислоты. Только тогда наступает успо коение. Щелочь и кислота «нейтрализовали» друг друга, говорят в таких случаях. От соединения их между собой получается «нейтральная» соль — ни кислая, ни едкая. Так, например, от соединения жгучей соляной кислоты с едким натром получается обыкновеннейшая поваренная соль.»
Отличительные признаки щелочи.
Из выше прочитанного мы уже знаем, что противоположностью щелочи является кислота. Вместо горького вкуса 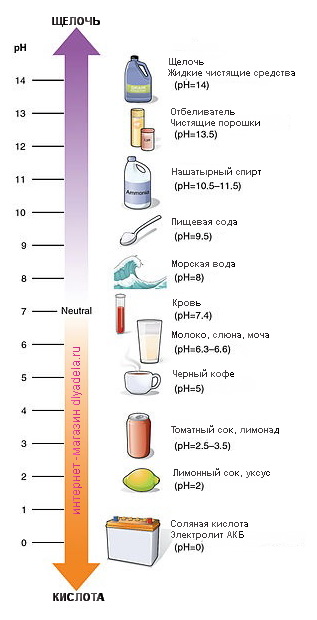
Почему вещество щелочное?
Таким образом, нам уже известно, что рН уровень представляет собой шкалу, значения которой колеблятся от 0-14 и указывают, является ли вещество щелочью или кислотой. Однако мы действительно не знаем, почему. Давайте рассмотрим этот вопрос более детально.
Уровень рH вещества зависит от того, как атомы расположены и объединены в веществе. Чистая вода находится прямо в середине шкалы и имеет pH 7. Это означает, что она содержит равное количество атомов водорода (H +) и гидроксидных атомов (OH-). Когда вещество имеет больше атомов водорода (Н +), это кислота. Когда вещество имеет больше гидроксидных атомов (OH-), оно является щелочным.
Где купить щелочь?
Купить щелочь в Новосибирске со степенью очистки ЧДА (чистая для анализов) в магазине «Для дела» можно на странице заказов: едкий натр NaOH или едкий кали KOH. Для иногородних покупателей товар может быть отправлен Почтой РФ или транспортными компаниями.
Кислоты и щёлочи

И получается такое вещество, которое не относится ни к кислотам, ни к щелочам. Оно не способно вызывать ожоги. Но это будет только при правильной пропорции кислоты и щёлочи (иногда для верности пользуются фенолфталеином, он окрашивает щёлочь в слегка фиолетовый цвет).
Кислота и щёлочи — это как две противоположности. Но они очень важны при изготовлении таких вещей как: удобрения, пластик, мыла, моющие средства, красок, бумаги и даже взрывчаток. Это далеко не весь список.
Что такое кислота
Кислота — это и есть что-то кислое, оно характеризуется кислым вкусом. Кислота содержится в уксусе – уксусная кислота, в лимоне – лимонная кислота, в молоке – молочная кислота, в желудке – соляная кислота и т.п. Но это всё так называемые слабые кислоты, помимо них существуют кислоты с большей концентрацией (серная, синильная кислоты и т.д. хотя этот учёный пробовал). Они гораздо опаснее для человека и пробовать их не рекомендуется никому. Они способны разъесть одежду, кожу, вызвать тяжёлый ожог на коже, разъесть бетон и другие вещества. Например, соляная кислота нам нужна для того, чтобы желудок быстрее переваривал пищу, а также для уничтожения большинства вредных бактерий, которые приходят вместе с пищей.
Что такое щелочь?
Щелочь — это те вещества, которые хорошо растворяются в воде. При этом реакция сопровождается с выделением тепла, с увеличением температуры. Если щёлочь сравнивать с кислотой, то на ощупь она намного «мыльнее», то есть скользкая. Вообще, щёлочи не сильно отстают от кислот по разъеданию и по силе. Они также могут с лёгкостью разъесть древесину, пластик, одежду и тому подобное.
Кстати, из щёлочей делают мыло, стекло, бумагу, ткань и это не весь список. Щёлочь можно найти у себя на кухне, ну или в магазине под названием пищевая сода. Кстати, пищевая сода это очень хороший помощник всем домохозяйкам.
Кислоты и щёлочи – отличия
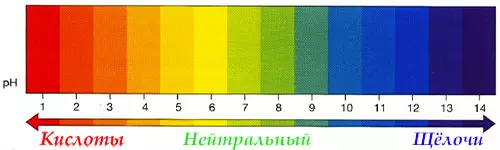
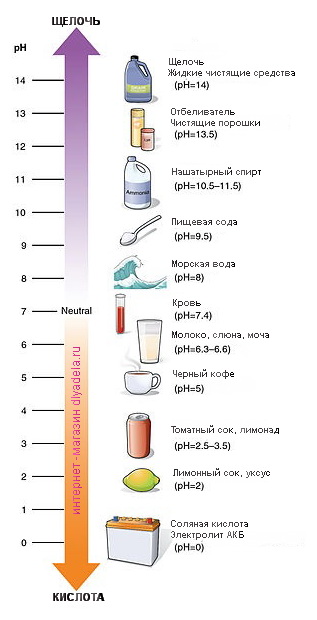
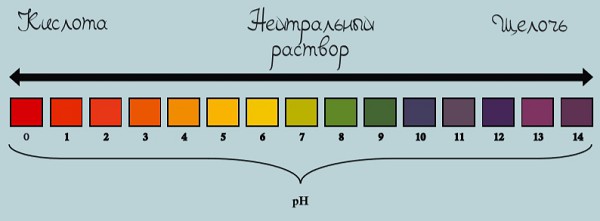
Кислоты и щёлочи отличают по показателям pH (шкала pH). Ниже Вы видите картинку – это специальная шкала, на которой имеются числа от 0 и до 14. Нулём обозначают самые сильные кислоты, а четырнадцатью – самую сильную щёлочь. Но какая же середина между этими числами? Может быть 5, может быть 7, а может быть 10? Серединой принято считать число 7 (нейтральное положение). То есть числа до 7 — это все кислоты, а больше 7 — это щёлочи.
pH продуктов
Сильные кислоты и слабые кислоты
Есть некоторые кислоты, которые мы можем употреблять, в то время как работа с другими предполагает строгие меры безопасности.
Сильные кислоты — это те, которые полностью диссоциируют или ионизируются в водных растворах.
Один из способов визуализировать, как отличить слабые и сильные кислоты, по аналогии с игроками в регби:
Примеры сильных кислот
Среди известных сильных кислот выделяют:
Примеры слабых кислот
Обычно кислоты органических соединений известны как слабые:
Показатель кислотности растворов рН, механизм действия
Именно для этой шкалы разработаны специальные индикаторы — лакмусы. Это обычная полоска, которая реагирует на среду. В кислотной среде она окрашивается в красный цвет, а в щелочной среде – в синий цвет. Она необходима не только в химии, но и в быту.
Например, если у Вас есть аквариум, то немаловажную роль играет кислотность воды. От неё зависит вся жизнь аквариума. К примеру, показатель кислотности воды для аквариумных рыбок колеблется от 5 до 9 рН. Если будет больше или меньше, то рыбка будет чувствовать себя не комфортно, а может и вовсе умереть. Всё тоже самое и с растениями для аквариумов.
Работа с кислотами и щёлочами
Работа с кислотами и щёлочами требует большой внимательности и осторожности. Ведь при попадании на кожу они вызывают сильные ожоги. Старайтесь работать в проветриваемом помещении. Вдыхать пары щёлочей и кислот также не рекомендуется. Для личной безопасности стоит воспользоваться очками, перчатками и специальной одеждой, чтобы не повредить глаза, руки и любимую одёжку.
При работе с кислотами следует помнить, что сначала вливают кислоту в раствор (воду), а не наоборот. В противном случае произойдёт бурная реакция, которая сопровождается брызгами. А сам процесс добавления кислоты в раствор следует делать очень медленно, при этом контролировать степень нагрева сосуда и обязательно добавлять кислоту по стенкам сосуда.
При работе со щёлочами первым следует добавлять понемногу щёлочь. К тому же запрещено пользоваться стеклянной посудой, рекомендуют фарфоровую или специальную посуду.
При химической обработке металлов (оксидирование, анодирование, травление и др.) погружать в раствор и вынимать из раствора изделие следует с помощью специальных приспособлений или инструментов, но никак не руками, даже если они в резиновых перчатках. Кстати, щёлочь входит в состав некоторых батареек.
Запомните, что при химических ожогах кожи поражённое место нужно промыть сильной струёй проточной воды. И окончательно нейтрализовать: от кислот — 3%-ным раствором питьевой соды, а щёлочь — 1%-ным раствором уксусной кислоты.
Щелочи: понятие, свойства и применение
К щелочам принято относить гидроксиды щелочных и щелочно-земельных металлов.
Все щелочи — это основания, но не наоборот, нельзя считать определения «основание» и «щелочь» синонимами.
Правильное химическое название щелочей — гидроксид (гидроокись), например, гидроокись натрия, гидроксид калия. Часто употребляются также названия, которые сложились исторически. Ввиду того, что щелочи разрушают материалы органического происхождения — кожу, ткани, бумагу, древесину, их называют едкими: например, едкий натр, едкий барий. Однако понятием «едкие щелочи» химики определяют гидроксиды щелочных металлов — лития, натрия, калия, рубидия, цезия.
Свойства щелочей
Щелочи — твердые вещества белого цвета; гигроскопичные, водорастворимые. Растворение в воде сопровождается активным выделением тепла. Вступают в реакции с кислотами, образуя соль и воду. Эта реакция нейтрализации является важнейшей из всех свойств щелочей. Кроме этого, гидроксиды реагируют с кислотными оксидами (образующими кислородосодержащие кислоты), с переходными металлами и их оксидами, с растворами солей.
Гидроксиды щелочных металлов растворяются в метиловом и этиловом спиртах, способны выдерживать температуры до +1000 °С (за исключением гидроксида лития).

Если сравнивать щелочи по химической активности, то она увеличивается при движении по столбцу таблицы Менделеева сверху вниз.
Концентрированные щелочи разрушают стекло, а расплавы щелочей — даже фарфор и платину, поэтому растворы щелочей не рекомендуется хранить в сосудах с пришлифованными стеклянными пробками и кранами, так как пробки и краны может заклинить. Хранят щелочи, обычно, в полиэтиленовых емкостях.
Именно щелочи, а не кислоты, вызывают более сильные ожоги, так как их сложнее смыть с кожи и они проникают глубоко в ткань. Смывать щелочь надо неконцентрированным раствором уксусной кислоты. Работать с ними необходимо в средствах защиты. Щелочной ожог требует немедленного обращения к врачу!
Применение щелочей
— В качестве электролитов.
— Для производства удобрений.
— В медицине, химических, косметических производствах.
— В рыбоводстве для стерилизации прудов.
В магазине «ПраймКемикалсГрупп» вы найдете самые востребованные щелочи по выгодным ценам.
Едкий натр
Самая популярная и востребованная в мире щелочь.
Применяется для омыления жиров в производстве косметических и моющих средств, для изготовления масел в процессе нефтепереработки, в качестве катализатора и реактива в химических реакциях; в пищепроме.
Едкое кали
Применяется для производства мыла, калийных удобрений, электролитов для батареек и аккумуляторов, синтетического каучука. Также — в качестве пищевой добавки; для профессиональной очистки изделий из нержавеющей стали.
Гидроксид алюминия
Востребован в медицине как отличный адсорбент, антацид, обволакивающее средство; ингредиент вакцин в фармацевтике. Кроме этого, вещество применяется в очистных сооружениях и в процессах получения чистого алюминия.
Гидроокись кальция
Популярная щелочь с очень широким спектром применения, которую в быту знают под названием «гашеная известь». Используется для дезинфекции, смягчения воды, в производстве удобрений, едкого натра, «хлорки», строительных материалов. Применяется для защиты деревьев и деревянных сооружений от вредителей и огня; в пищепроме как пищевая добавка и реактив при производстве сахара.
Гидроокись лития
Востребованное соединение в химпроме как сырье; в стекольной, керамической, 
Гидроокись бария
Применяется в химпроме как катализатор, а также в пищепроме для очистки жиров, сахара.
В аналитической химии применяются фиксаналы щелочей, которые можно купить у нас:
— стандарт-титр Натрий гидроокись (Натрий гидроксид) 0,1 H
— стандарт-титр Калий гидроокись (Калий гидроксид) 0,1 Н
Чем отличаются кислоты от щелочей
Кислоты и щёлочи отличают по показателям pH (шкала pH). Ниже Вы видите картинку – это специальная шкала, на которой имеются числа от 0 и до 14. Нулём обозначают самые сильные кислоты, а четырнадцатью – самую сильную щёлочь. Но какая же середина между этими числами? Может быть 5, может быть 7, а может быть 10? Серединой принято считать число 7 (нейтральное положение). То есть числа до 7 это все кислоты, а больше 7 это щёлочи.
Именно для этой шкалы разработаны специальные индикаторы — лакмусы. Это обычная полоска, которая реагирует на среду. В кислотной среде она окрашивается в красный цвет, а в щелочной среде – в синий цвет. Она необходима не только в химии, но и в быту.
Например, если у Вас есть аквариум, то немаловажную роль играет кислотность воды. От неё зависит вся жизнь аквариума. К примеру, показатель кислотности воды для аквариумных рыбок колеблется от 5 до 9 рН. Если будет больше или меньше, то рыбка будет чувствовать себя не комфортно, а может и вовсе умереть. Всё тоже самое и с растениями для аквариумов…
Кислоты
Кислоты — это соединения, содержащие водород и образующие ионы водорода (Н+) при растворении в воде. Ионы — это частицы с электрическим зарядом (см. статью «Химические связи»). Именно ионы придают кислотам их свойства, но существовать они могут только в растворе. Следовательно, свойства кислот проявляются исключительно в растворах. Молекула серной кислоты (H2SO4) состоит из атомов водорода, серы и кислорода. В состав соляной кислоты (НСl) входят водород и хлор. Кислота считается сильной, если большинство ее молекул распадаются в растворе, выделяя ионы водорода. Соляная, серная, азотная кислоты относятся к сильным. На контейнерах с сильными кислотами ставятся принятые во всем мире символы, означающие «опасно» и «высокая активность»Сила кислоты измеряется числом рН — водородным показателем. Сильные кислоты очень агрессивны; попав на поверхность предмета или на кожу, они прожигают её. На контейнерах с сильными кислотами ставятся принятые во всем мире символы, означающие «опасно» и «высокая активность».
Такие кислоты, как лимонная или уксусная, т.е. произведенные живыми организмами, называются органическими. Кислоты широко применяются в химической и медицинской промышленности, в производстве продуктов питания и синтетических волокон. Виноградный уксус содержит слабую кислоту, называемую уксусной. В помидорах есть органическая салициловая кислота. В цветных пятнах на коже морских улиток содержится кислота с неприятным вкусом, отпугивающая хищников. Для всех кислот характерно сходное поведение в химических реакциях. Например, при реакциях кислот с основаниями образуется нейтральное соединение — соль и вода. Реакции кислот с большинством металлов дают соль и водород. Реагируя с карбонатами, кислоты дают соль, углекислый газ и воду. Известный кулинарам пекарный порошок содержит гидрокарбонат натрия и винную кислоту. Когда в муку, содержащую пекарный порошок, добавляют воду, кислота и карбонат порошка вступают в реакцию, углекислый газ начинает выделятся в виде пузырьков, и это помогает тесту подниматься.
рН и индикаторы
Сила кислот и оснований определяется числом рН. Это мера концентрации ионов водорода в растворе. Число рН изменяется от 0 до 14. Чем меньше рН, тем выше концентрация водородных ионов. Раствор, рН которого меньше 7, — кислота. Апельсиновый сок имеет рН 4, значит, это кислота. Вещества с рН = 7 нейтральны, а вещества с рН больше 7 — основания или щелочи. рН кислоты или щелочи можно определить с помощью индикатора. Индикатор — это вещество, меняющее цвет при контакте с кислотой или щелочью. Так лакмус краснеет в кислоте и синеет в щелочи. Кислота окрашивает синюю лакмусовую бумажку в красные цвет, а красная лакмусовая бумажка в щелочи становится синей или фиолетовой. Лакмус получают из примитивных растений, называемых лишайниками. Другие растения, например, гортензия и краснокочанная капуста, также являются природными индикаторами.
Так называемый универсальный индикатор – это смесь нескольких красок. Он меняет цвет в зависимости от pH вещества. Он становится красным, оранжевым или желтым в кислотах, зеленым или желтым в нейтральных растворах и синим или фиолетовым в щелочах.
Серная кислота
Серная кислота играет важную роль в промышленности, прежде всего в производстве удобрений на основе суперфосфатов и сульфата аммония. Она также используется в производстве синтетических волокон, красителей, пластмасс, лекарств, взрывчатых веществ, моющих средств, автомобильных аккумуляторов. Когда-то серную кислоту называли минеральной кислотой, так как ее получали из серы — вещества, встречающегося в земной коре в виде минерала. Серная кислота очень активна и агрессивна. При растворении в воде она выделяет много тепла, поэтому ее нужно вливать в воду, но не наоборот — тогда кислота растворится, а вода поглотит тепло. Она — мощный окислитель, т.е. при реакциях окисления она отдает кислород другим веществам. Серная кислота также является осушителем, т.е. забирает воду, связанную с другим веществом. Когда сахар (C12H22O11) растворяется в концентрированной серной кислоте, кислота забирает у сахара воду, и от сахара остается пенящаяся масса черного угля.
Кислоты в почве
Цветы гортензии на кислотной почве синие, а на щелочной — розовыеКислотность почвы зависит от характера образовавших ее пород и от растущих на ней растений. На меловых и известняковых породах почва обычно щелочная, а на лугах, в песчаных и лесистых районах она более кислая. Кислотность также повышают кислотные дожди. Для земледелия лучше всего подходят нейтральные или слабокислые почвы, рН которых от 6,5 до 7. Разлагаясь, мертвые листья образуют органическую гуминовую кислоту и повышают кислотность почвы. Там, где почвы чересчур кислотные, в них добавляют измельченный известняк или гашеную известь (гидроксид кальция), т.е. основания, которые нейтрализуют кислоты почвы. Такие растения, как рододендроны и азалии хорошо растут на кислотных почвах. Цветы гортензии на кислотной почве синие, а на щелочной — розовые. Гортензия – природный индикатор. На кислотных почвах её цветы синие, а на щелочных розовые.
В настоящее время в химии принята теория Брёнстеда — Лоури и Льюиса, которая определяет кислоты и основания. В соответствии с этой теорией, кислоты — это вещества, способные отщеплять протон, а основания — отдавать электронную пару OH−. Можно сказать, что под основаниями понимают соединения, которые при диссоциации в воде образуют только анионы вида OH−. Если совсем просто, то щелочами называют соединения, состоящие из металла и гидроксид-иона OH−.
К щелочам принято относить гидроксиды щелочных и щелочно-земельных металлов. Все щелочи — это основания, но не наоборот, нельзя считать определения «основание» и «щелочь» синонимами.
Правильное химическое название щелочей — гидроксид (гидроокись), например, гидроокись натрия, гидроксид калия. Часто употребляются также названия, которые сложились исторически. Ввиду того, что щелочи разрушают материалы органического происхождения — кожу, ткани, бумагу, древесину, их называют едкими: например, едкий натр, едкий барий. Однако понятием «едкие щелочи» химики определяют гидроксиды щелочных металлов — лития, натрия, калия, рубидия, цезия.
Свойства щелочей
Щелочи — твердые вещества белого цвета; гигроскопичные, водорастворимые. Растворение в воде сопровождается активным выделением тепла. Вступают в реакции с кислотами, образуя соль и воду. Эта реакция нейтрализации является важнейшей из всех свойств щелочей. Кроме этого, гидроксиды реагируют с кислотными оксидами (образующими кислородосодержащие кислоты), с переходными металлами и их оксидами, с растворами солей.
Гидроксиды щелочных металлов растворяются в метиловом и этиловом спиртах, способны выдерживать температуры до +1000 °С (за исключением гидроксида лития).
Гидроксид натрия (едкий натр) используется в чистящих жидкостях, а также (как и гидроксид калия) для производства мыла. Мыло — это соль, образующаяся при реакции щелочей с кислотами растительных жиров. Жало осы выпускает щелочь, которую можно нейтрализовать кислотой, например уксусом.
Щелочи — активные химические реагенты, поглощающие из воздуха не только водяные пары, но и молекулы углекислого и сернистого газа, сероводорода, диоксида азота. Поэтому хранить гидроксиды следует в герметичной таре или, например, доступ воздуха в сосуд со щелочью организовать через хлоркальциевую трубку. В противном случае хим.реактив после хранения на воздухе будет загрязнен карбонатами, сульфатами, сульфидами, нитратами и нитритами.
Если сравнивать щелочи по химической активности, то она увеличивается при движении по столбцу таблицы Менделеева сверху вниз.
Концентрированные щелочи разрушают стекло, а расплавы щелочей — даже фарфор и платину, поэтому растворы щелочей не рекомендуется хранить в сосудах с пришлифованными стеклянными пробками и кранами, так как пробки и краны может заклинить. Хранят щелочи, обычно, в полиэтиленовых емкостях.
Именно щелочи, а не кислоты, вызывают более сильные ожоги, так как их сложнее смыть с кожи и они проникают глубоко в ткань. Смывать щелочь надо неконцентрированным раствором уксусной кислоты. Работать с ними необходимо в средствах защиты. Щелочной ожог требует немедленного обращения к врачу!
Применение щелочей
— В качестве электролитов.
— Для производства удобрений.
— В медицине, химических, косметических производствах.
— В рыбоводстве для стерилизации прудов.
Едкий натр. Самая популярная и востребованная в мире щелочь. Применяется для омыления жиров в производстве косметических и моющих средств, для изготовления масел в процессе нефтепереработки, в качестве катализатора и реактива в химических реакциях; в пищепроме.
Едкое кали. Применяется для производства мыла, калийных удобрений, электролитов для батареек и аккумуляторов, синтетического каучука. Также — в качестве пищевой добавки; для профессиональной очистки изделий из нержавеющей стали.
Гидроксид алюминия. Востребован в медицине как отличный адсорбент, антацид, обволакивающее средство; ингредиент вакцин в фармацевтике. Кроме этого, вещество применяется в очистных сооружениях и в процессах получения чистого алюминия.
Гидроокись кальция. Популярная щелочь с очень широким спектром применения, которую в быту знают под названием «гашеная известь». Используется для дезинфекции, смягчения воды, в производстве удобрений, едкого натра, «хлорки», строительных материалов. Применяется для защиты деревьев и деревянных сооружений от вредителей и огня; в пищепроме как пищевая добавка и реактив при производстве сахара.
Гидроокись лития. Востребованное соединение в химпроме как сырье; в стекольной, керамической, Фиксаналырадиотехнической индустрии; для производства смазочных материалов, электролитов; для поглощения вредных газов.
Гидроокись бария. Применяется в химпроме как катализатор, а также в пищепроме для очистки жиров, сахара.
Есть мнения что:
• Кислоты и щелочи неспособны мирно сосуществовать даже одну секунду, находясь в соприкосновении. Перемешавшись, они мгновенно начинают бурное взаимодействие. Химическая реакция с ними сопровождается шипением и разогревом и длится до тех пор, пока эти ярые антагонисты не уничтожат друг друга.
• Кислотам свойственно образовывать кислую среду, а щелочам – щелочную.
• Химики отличают щелочь от кислоты по ее поведению с лакмусовой бумажкой или фенолфталеином.
Щёлочи
Смотреть что такое «Щёлочи» в других словарях:
Щёлочи — Щёлочи гидроксиды щелочных, щёлочноземельных металлов и аммония. К щёлочам относят хорошо растворимые в воде основания. При диссоциации щёлочи образуют анионы OH− и катион металла. К щёлочам относятся гидроксиды металлов подгрупп Iа и IIа… … Википедия
не содержащий щёлочи — свободный от щёлочи — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы свободный от щёлочи EN alkali free … Справочник технического переводчика
Щёлочи — ЩЁЛОЧИ, гидроксиды щелочных (едкие щёлочи) и щёлочноземельных металлов. Щелочи сильные основания; едкие щелочи хорошо растворяются в воде, гидроксиды щёлочноземельных металлов плохо. Все щелочи чрезвычайно агрессивны, их растворы разрушают стекло … Иллюстрированный энциклопедический словарь
Едкие щёлочи — хорошо растворимые в воде гидроокиси щелочных металлов, например едкий натр NaOH, едкое кали КОН. Оказывают разъедающее действие на слизистые оболочки и кожу. Широко применяются во многих отраслях промышленности. См. Щёлочи … Большая советская энциклопедия
Щёлочи — (хим.) В настоящее время говорят почти исключительно обедких щёлочах, но прежде под Щ. разумели вообще вещества, растворы коихимеют щелочную реакцию и вкус. К числу Щ. относили тогда и карбонатыщелочных металлов. Сода и поташ, например, имеют… … Энциклопедия Брокгауза и Ефрона
ЩЁЛОЧИ — гидроксиды щелочных металлов (Li, Na, K, Rb, Cs, Fr) и щёлочноземельных металлов (Ca, Sr, Ba, Ra) (I и II группы периодической системы Д. И. Менделеева). Щ. твердые белые гигроскопические вещества. При их растворении в воде выделяется большое… … Российская энциклопедия по охране труда
заводнение раствором щёлочи — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN alkaline waterflooding … Справочник технического переводчика
оборудование для закачивания щёлочи (в пласт) — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN caustic flooding equipment … Справочник технического переводчика
раствор щёлочи — отработанная щёлочь щелочные отбросы — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы отработанная щёлочьщелочные отбросы EN alkali liquor … Справочник технического переводчика
устройство для распределения щёлочи в фильтре регенерации анионита — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN anion regeneration tank caustic distributor … Справочник технического переводчика
Щелочи
Щёлочи — гидроксиды щелочных и щёлочноземельных металлов. К щелочам относят растворимые в воде основания. При диссоциации щелочи образуют ионы OH- и ион металла.
К щелочам относятся гидроксиды металлов подгрупп Iа и IIа периодической системы, например NaOH(едкий натрий), KOH (едкий калий), Ba(OH)2 (едкий барий). Едкие щелочи — тривиальное название гидроксидов лития LiOH, натрия NaOH, калия КОН, рубидия RbOH, и цезия CsOH.
Физические свойства
Химические свойства
Поглощают H2O и CO2 из воздуха. Щёлочи широко применяются в промышленности. Важное химическое свойство щелочей — способность образовывать соли в реакции с кислотами.
Получение
Получают путём электролиза хлоридов щелочных металлов или действием воды на оксиды щелочных металлов.
Полезное
Смотреть что такое «Щелочи» в других словарях:
щелочи́ть(ся) — щелочить(ся), чу, чишь, чит(ся) … Русское словесное ударение
ЩЕЛОЧИ — ЩЕЛОЧИ, растворимые в воде основания (см.), вещества, дающие в водном растворе ион гидроксила. Ион гидроксила и обусловливает. способность Щ.: 1) реагировать с к тами с выделением тепла и образованием солей (реакция нейтрализации); 2) вызывать… … Большая медицинская энциклопедия
ЩЕЛОЧИ — (едкий натр, едкое кали, негашеная известь). По своему действию к щелочам близки сода и силикат натрия. Щелочные сточные воды поступают в водоемы с сульфатцеллюлозных, шерстеобрабатывающих, текстильных предприятий и коммунально бытового хозяйства … Болезни рыб: Справочник
ЩЕЛОЧИ — ЩЕЛОЧИ, растворимые ОСНОВАНИЯ, которые при реакции с кислотой дают соль и воду. У раствора щелочи рН выше 7, и он окрашивает лакмусовую бумагу в синий цвет. Щелочные растворы используются как чистящее средство. К сильным щелочам относятся… … Научно-технический энциклопедический словарь
Щелочи — [alkalies] растворимые в воде основания. Водные растворы щелочей характеризуется высокой концентрацией гидроксидных ионов ОН. К щелочам относятся оксиды щелочных, щелочноземельных металлов и аммония. Большинство щелочей твердые белые весьма… … Энциклопедический словарь по металлургии
Щелочи — ► alkali, base Растворимые в воде основания. Водные растворы щелочи характеризуются высокой концентрацией гидроксильных ионов ОН. Большинство щелочей – твердые белые весьма гигроскопичные вещества. Растворение их в воде сопровождается выделением… … Нефтегазовая микроэнциклопедия
Щелочи — (хим.) В настоящее время говорят почти исключительно о едких щелочах (см.), но прежде под Щ. разумели вообще вещества, растворы коих имеют щелочную реакцию и вкус. К числу Щ. относили тогда и карбонаты щелочных металлов (см. Калий). Сода и поташ … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
щелочи́ть — чу, чишь; несов., перех. Прибавлять во что л. щелочь или щелок. Щелочить воду … Малый академический словарь
ЩЕЛОЧИ — водные соединения окисей щелочных и щелочно земельных металлов (натрия, кальция и др.). Все Щ. растворимы в воде … Сельскохозяйственный словарь-справочник
Что такое щёлочь? Что относится к щелочам?
К щёлочям относят:
Гидроксиды щёлочноземельных металлов (кальций, стронций, барий, радий).
Основания, которые хорошо растворяются в воде, относятся к щёлочям.
В частности, к ним можно отнести вещества:
NaOH (гидроксид натрия, едкий натр)
Ba(OH)2 (гидроксид бария, едкий бариат)
KOH (гидроксид калия)
Взаимодействие с кислотами:
Это основное свойство щелочей, данную реакцию называют реакцией нейтрализации. В её результате образуется соль и вода.
Fe(OH)3 + 3HCL = FeCl3 + H2O.
За прохождением реакций можно наблюдать по изменениям окраски индикаторов.
Применение:
Щелочами называются растворимые в воде основания металлов. Металлы эти так и называют: щелочные, щелочноземельные. Это калий, кальций, барий, натрий, литий, цезий, рубидий, магний и другие.
Примеры щелочей: гидроксид натрия (едкий натр), гидроксид калия (едкое кали, каустический поташ), гидроксид кальция.
Щёлочи нейтрализуются кислотами, в результате реакции остаётся соль металла и вода.
Щелочью можно определить как основание, которое растворяется в воде.
Например, гидроксид натрия, гидроксид калия и карбонат натрия являются щелочами.
Что такое щелочь, в какие реакции вступают самые известные из них
Химия – наука, изучающая различные реакции, протекающие в природе, а также взаимодействия одних соединений с другими. Основными веществами здесь являются кислоты и щелочи, реакции между которыми обычно называются нейтрализацией. Они приводят к образованию растворимой в воде соли.
Что такое щелочь
Гидроксиды щелочных (металлы первой группы главной (А) подгруппы в периодической таблице химических элементов Д. И. Менделеева) и щелочноземельных (металлы второй группы главной (А) подгруппы, включая кальций) металлов, которые бурно взаимодействуют с водой и полностью в ней растворяются, называются щелочами. Так как они способны разрушать органический материал (кожу, древесину, бумагу), их называют едкими. Например, гидроксид калия (KOH) – едкий калий, бария (Ba(OH)2) – едкий барий и так далее.
Физические свойства сильных оснований
Исходя из определения, что такое щелочь, можно добавить, что эти гидроксиды также представляют собой твердые гигроскопичные (способные поглощать из воздуха пары воды) вещества белого цвета. К самым сильным щелочам относятся гидроксиды цезия CsOH и радия Ra(OH)2. Реакции щелочей чаще всего сопровождаются выделением тепла (экзотермические). Также к физическим свойствам таких оснований можно отнести их способность растворяться в некоторых органических соединениях, например, в спиртах: метаноле и этаноле.
Химические свойства
Растворы щелочей способны вступать в различные реакции.
Сильные основания обладают способностью взаимодействовать с кислотными и амфотерными оксидами:
При реагировании с амфотерными металлами (Zn, Al и прочие) также возможно образование как расплава, так и соответствующей комплексной соли. Причем обе реакции сопровождаются выделением газообразного водорода:
Также щелочи способны реагировать с солями, в результате чего образуется другое основание и другая соль. Условием протекания реакции является то, что в результате одно из образовавшихся веществ должно быть не растворимо в воде:
NaOH + CuSO4 = Na2SO4 + Cu(OH)2.
Как уже было упомянуто ранее, щелочи и кислоты вступают в реакцию нейтрализации, образуется соль и вода:
NaOH + HCl = NaCl + H2O.
Щелочи вступают в реакцию с другими основаниями только, если это гидроксиды амфотерных металлов:
NaOH + Al(OH)3 = Na[Al(OH)4].
Некоторые из них могут вступать во взаимодействие со многими органическими веществами: эфирами, амидами, многоатомными спиртами:
2C2H6O2 + 2NaOH = C2H4O2Na2 + 2H2O (продукт реакции – алкоголят натрия).
Как получают сильные основания
Щелочи получают разными способами как в промышленности, так и в лабораториях.
В промышленной индустрии существуют несколько методов получения щелочей: пиролиз, известковый, ферритный, электролиз, который делится на диафрагменный, мембранный и ртутный методы на жидких и твердых катодах.
Это электролиз растворов хлоридов натрия и калия, после чего на аноде и катоде выделяются хлор и водород, и получаются соответствующие гидроксиды:
При пиролизе в 1000 градусов на первом этапе происходит образование оксида натрия:
Na2CO3 = Na2O + CO2.
На втором этапе полученный охлажденный оксид растворяют в воде, в результате чего и получается необходимая щелочь:
Na2O + H2O = 2NaOH.
В лабораториях также применяется электролиз. Еще щелочи могут получиться путем воздействия на соответствующие металлы водой или взаимодействия солей этих металлов с другими основаниями, в результате чего получается необходимая щелочь и нерастворимый в воде второй продукт реакции – соль.
2Cs + 2H2O = 2CsOH + H2.
В результате действия воды на оксид лития получается щелочь:
Li2O + 2H2O = 2LiOH + H2.
Применение
Опираясь на само определение того, что такое щелочь, можно понять, что они находят широкое применение не только в промышленности, но и в быту:
Меры предосторожности
Становится очевидным, что такие щелочи, как гидроксиды натрия, лития, калия, цезия и прочие, способны сильно повреждать и обжигать кожу и слизистые оболочки глаз даже при попадании туда мельчайших частиц соединения. Чтобы предотвратить это, необходимо носить защитные очки, резиновые перчатки, а также спецодежду, которая обработана специальными веществами, не позволяющими материалу взаимодействовать со щелочами.
Кислоты, щелочи и основания с точки зрения химии
Что же представляют собой кислоты, щелочи и основания с химической точки зрения? Читай внимательно и запоминай. Смотри не запутайся!
Что такое кислота?
Кислоты представляют собой молекулы, которые при растворении в воде высвобождают ион водорода. Ионы — это положительно и отрицательно заряженные частички, которые придают кислотам их свойства.
Давай рассмотрим этот процесс на примере соляной кислоты — HCI. Если соляную кислоту соединить с водой, она распадется на ион водорода (Н+) и ион хлора (CI ). Так как в составе молекулы воды также есть водород, то при распаде соляной кислоты общее количество ионов водорода в растворе увеличится.
А что происходит со щелочами при попадании в воду? В воде щелочи высвобождают гидроксид-ионы. Например, гидроксид натрия (NaOH) — щелочь. При соединении с водой он распадается на ионы натрия (Na+) и гидроксид-ионы (ОН ). Когда гидроксид-ионы встречаются с ионами водорода воды, общее количество ионов водорода в растворе сокращается.
Что такое основание?
Основание — это соединение, химически противоположное кислоте. В состав основания входят ионы металлов и связанные с ними гидроксид-ионы. Эти вещества способны присоединять ионы водорода (Н+) из кислоты. Когда основание смешивается с кислотой, оно полностью нейтрализует его свойства, а в результате реакции образуется соль.
Например, с точки зрения химии хорошо знакомая тебе зубная паста — это основание, которое нейтрализует кислоту, оставшуюся во рту после приема пищи.
ЗАПОМНИ! В связи с тем, что ионы существуют только в растворах, свои свойства кислоты проявляют также лишь в растворах.
Что такое щелочь?
Щелочи — это соединения, в состав которых входят ион металла и гидроксид-ион (ОН-). К щелочам химики относят гидроксиды щелочных и щелочноземельных металлов. Щелочи представляют собой вещества белого цвета, которые хорошо растворяются в воде. Более того, растворение всегда сопровождается очень активным выделением тепла. Щелочи вступают в реакцию с кислотами, образуя соль и воду.
Щелочи очень активны! Они способны поглощать из воздуха не только водяные пары, но и молекулы углекислого газа, сероводорода и т.д. Поэтому хранят щелочи в очень герметичной таре. Концентрированные щелочи разрушают стекло, а иногда даже фарфор. Если сравнивать щелочи с кислотами, то щелочи могут вызвать более сильные ожоги, так как они очень быстро проникают в ткань, и их практически невозможно смыть водой.
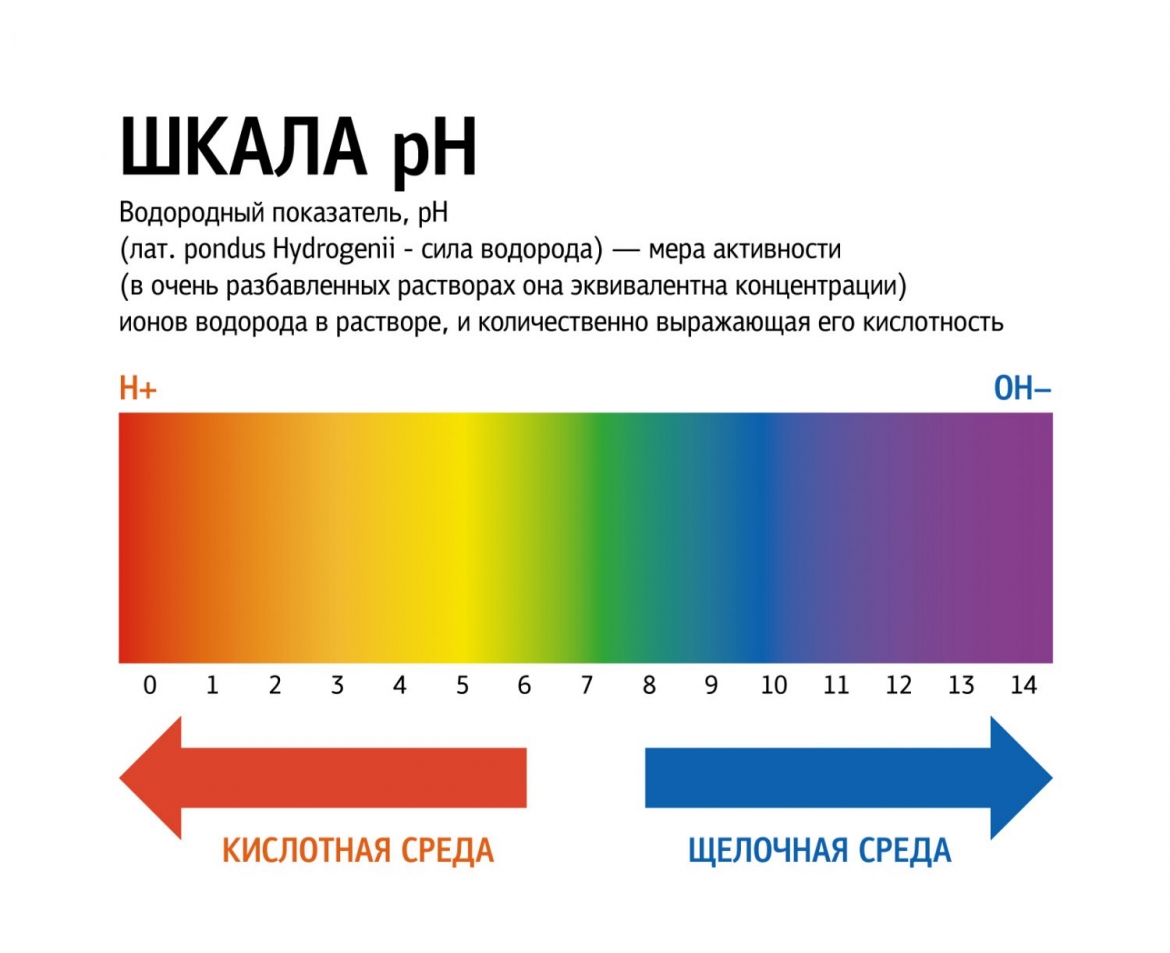
Шкала pH
Почему одни жидкости — кислоты, а другие — щелочи? Оказывается, все дело в типе ионов. Если в жидкости больше концентрация ионов водорода, такая жидкость является кислотой, а если гидроксид-ионов, то щелочью.
Шкала pH используется для измерения кислотности или щелочности раствора от 0 до 14.
Если pH раствора находится в пределах 0—7, то такой раствор считается кислотным, при этом раствор с pH = 0 — самый кислый. Растворы с pH в пределах 7—14 являются щелочами, при этом раствор с pH = 14 считается самым едким и опасным.
Если pH раствора равен 7, то такой раствор является нейтральным, так как концентрация ионов водорода равна концентрации гидроксид-ионов. Пример нейтрального раствора — чистая вода.
Что такое показатель pH?
В переводе с латинского pH (potentia hydrogeny) означает «сила водорода», т.е. активность ионов водорода в водном растворе.
Как химики определяют наличие воды в веществе?
Они берут бесцветный сульфат меди (CuSO4) и добавляют его в вещество. Если воды нет, то порошок остается бесцветным, однако даже при минимальном количестве воды он становится синим.
Концентрированные кислоты и щелочи
Ядовитые жидкости находятся не только в школьных лабораториях, они и вокруг нас. Это различные средства бытовой химии (стиральные порошки и пятновыводители), цветочные удобрения и ядохимикаты, лаки и краски, клеи и растворители, бензин и дизельное топливо, аккумуляторные, тормозные и прочие технические жидкости, а на кухне — уксус и уксусная кислота.
Совершенно очевидно, что все вышеупомянутые вещества должны использоваться строго по назначению и в соответствии с определенными правилами, указанными на этикетке каждого средства. К сожалению, несоблюдение мер безопасности при работе с ядовитыми средствами может привести к серьезным проблемам со здоровьем: отравлению, различным повреждениям кожи и слизистых оболочек.
ВНИМАНИЕ! Обязательно запомни следующую информацию: кислоты с очень низким показателем pH (менее 2) и щелочи, pH которых выше 13, являются чрезвычайно опасными!
Кислоты и щелочи в природе
ОСТОРОЖНО! Как правило, концентрированные кислоты и щелочи есть во всех школьных каби нетаххимии, и пользоваться ими можно только под руководством учителя.
Применение щелочей
Щелочи широко применяются в различных отраслях промышленности, медицине и быту. Например, каустическая сода используется для растворения жиров и входит в состав многих моющих средств, применяется при производстве целлюлозы, масел, дизельного топлива. Также щелочи используют для изготовления мыла, искусственных волокон, различных красителей и т.д.
Кислоты в почве
Оказывается, кислоты есть и в почвах, а способность почвы проявлять свойства кислот называется кислотностью. Этот показатель зависит от наличия в земле ионов водорода. От кислотности почвы зависят рост и развитие растений. Большинство из них предпочитает нейтральные или близкие к ним почвы. Однако есть ряд растений, которые отлично себя чувствуют именно на кислотных почвах, например рододендроны, гортензии, азалии. Некоторые сорта гортензии могут менять цвет бутонов в зависимости от условий выращивания и кислотности почвы. Ученые выяснили, что на цвет бутонов влияет наличие алюминия!
Большинство садовых почв характеризуется достаточным содержанием этого элемента. В кислой среде соединения алюминия превращаются в растворимые и становятся доступными для растений, поэтому и вырастают бутоны голубого цвета. В нейтральной или щелочной среде алюминий находится в виде нерастворимых соединений, поэтому он и не поступает в растения. В результате на таких почвах растут бутоны розового цвета.
Кислоты и щелочи в нашем организме
Для переваривания пищи организм использует желудочный сок, в состав которого входят соляная кислота и различные ферменты. Иногда, особенно после переедания, мы можем почувствовать боль в желудке. Чаще всего для снятия неприятных ощущений достаточно принять антацидный, или противокислотный, препарат, основное действие которого направлено на нейтрализацию соляной кислоты в желудке. Как правило, все антациды — щелочи, и именно они нейтрализуют повышенную активность кислот.
Основания
О чем эта статья:
Основания (гидроксиды) — это сложные вещества, которые состоят из катиона металла и гидроксильной группы (OH).
Общая формула оснований: Me(OH)n, где Me — химический символ металла, n — индекс, который зависит от степени окисления металла.
Примеры оснований: NaOH, Ba(OH)2, Fe(OH)2.
Названия оснований
Названия гидроксидов строятся по систематической номенклатуре следующим образом:
Пишем слово «гидроксид».
Указываем название второго химического элемента в родительном падеже.
Если второй элемент имеет переменную валентность, то указываем валентность элемента в этом соединении в скобках римской цифрой.
Примеры названий оснований:
Ni(OH)2 — гидроксид никеля (II);
Al(OH)3 — гидроксид алюминия.
У некоторых оснований существуют и тривиальные названия. Собрали их в таблице.
Тривиальные названия некоторых оснований
Классификация оснований
По растворимости в воде
В зависимости от растворимости в воде выделяют:
щелочи. Эти основания растворимы в воде: NaOH, KOH, Ba(OH)2 и другие. Ca(OH)2, хотя малорастворим, тоже относится к щелочам из-за своей едкости;
нерастворимые основания. К таким основаниям относятся Fe(OH)2, Cu(OH)2 и другие;
амфотерные гидроксиды. К амфотерным относятся те основания, которые образованы металлами со степенью окисления +3 или +4. Эти основания отличаются тем, что проявляют как основные свойства, так и кислотные.
Также есть основания, которые относятся к амфотерным, но образованы металлом с иной степенью окисления: Zn(OH)2, Pb(OH)2, Sn(OH)2, Be(OH)2.
Напомним, что растворимость мы проверяем по таблице растворимости кислот и оснований в воде.
По числу гидроксогрупп
В зависимости от количества гидроксильных групп, способных замещаться на кислотный остаток, выделяют следующие виды оснований:
однокислотные: KOH, NaOH;
Физические свойства оснований
Основания при обычных условиях — это твердые кристаллические вещества без запаха, нелетучие, чаще всего белого цвета. В таблице приведены основания, которые имеют иную окраску.
Гидроксид лития LiOH
Гидроксид магния Mg(OH)2
Гидроксид кальция Ca(OH)2
Химические свойства оснований
Растворы щелочей изменяют окраску индикатора
Гидроксид-ионы, которые содержатся в растворе щелочи, взаимодействуют с индикатором, образуя новые соединения. Признак реакции — окраска раствора.
Взаимодействие с кислотными оксидами
Щелочи вступают в реакцию с любыми кислотными оксидами. Нерастворимые основания взаимодействуют только с кислотными оксидами, которые соответствуют сильным кислотам.
Кислотный оксид + основание = соль + вода
Взаимодействие с кислотами
Щелочи вступают в реакцию со всеми кислотами. Нерастворимые основания могут взаимодействовать только с сильными кислотами.
Основание + кислота = соль + вода
Взаимодействие основания с кислотой называют реакцией нейтрализации — это частный случай реакции обмена.
Взаимодействие с солями
Основания взаимодействуют с растворимыми солями по обменному механизму. В результате такой реакции должен выделиться осадок или газ (CO2, SO2, NH3).
Основание + соль = другое основание + другая соль
Термическое разложение
При нагревании нерастворимые основания разлагаются на соответствующий оксид (степень окисления металла остается неизменной) и воду.
Нерастворимое основание оксид металла + вода
Взаимодействие амфотерных гидроксидов со щелочами
Продукты реакции зависят от условий ее проведения.
При сплавлении двух оснований:
Амфотерный гидроксид (тв) + щелочь (тв) = средняя соль + вода
Если реакция проводится в растворе:
Амфотерный гидроксид (р-р) + щелочь (р-р) = комплексная соль
Получение оснований
Взаимодействие металла с водой
Активные металлы (металлы групп IA и IIA, кроме Be и Mg) активно взаимодействуют с водой при обычных условиях с образованием щелочей.
Нерастворимые основания данным способом получить невозможно, за исключением Mg(OH)2.
Металл + вода = гидроксид металла + водород
Гидроксид магния можно получить данным способом, но только при нагревании:
Взаимодействие оксидов щелочных и щелочноземельных металлов с водой
Этим способом получают только растворимые в воде основания.
Оксид металла + вода = щелочь
Электролиз
Гидроксид натрия и калия в промышленности получают с помощью электролиза — через раствор хлорида калия проводят постоянный электрический ток:
Электролиз хлорида натрия протекает по аналогичной схеме.
Получение нерастворимых оснований при взаимодействии соли со щелочью
Растворимая соль + щелочь = нерастворимое основание + другая соль
Вопросы для самопроверки
Вспомните определение оснований и приведите 2 примера этих веществ.
Какие виды оснований существуют? Чем они отличаются?
К какому виду оснований относится Zn(OH)2?
Взаимодействуют ли основания с основными оксидами? Приведите примеры веществ, с которыми основания вступают в реакцию.
Можно ли получить гидроксид алюминия с помощью взаимодействия алюминия с водой?
Основания и другие темы по химии изучать интереснее, когда понимаешь, как применять знания в реальной жизни. На онлайн-курсах по химии в Skysmart преподаватели приводят яркие примеры: от процессов в природе до использования химических реакций в промышленности. Приходите учиться — вводный урок бесплатный!
Щёлочи
К щелочам относятся гидроксиды металлов подгрупп Iа и IIа (начиная с кальция) периодической системы, например NaOH (едкий натр), KOH (едкий калий), Ba(OH)2 (едкий барий). В качестве исключения можно отнести к щелочам гидроксид одновалентного таллия TlOH, который хорошо растворим в воде и является сильным основанием. Едкие щёлочи — тривиальное название гидроксидов лития LiOH, натрия NaOH, калия КОН, рубидия RbOH и цезия CsOH. Название «едкая щёлочь» обусловлено свойством разъедать кожу и слизистые оболочки, вызывая сильные ожоги, бумагу и другие органические вещества.
Из-за очень большой химической активности щёлочных металлов едкие щёлочи долгое время не удавалось разложить и они потому считались простыми веществами. Одним из первых предположение о сложном составе едких щелочей высказал Лавуазье. Основываясь на своей теории о том, что все простые вещества могут окисляться, Лавуазье решил, что едкие щёлочи — это уже окисленные сложные вещества. Однако подтвердить это удалось лишь Дэви в начале XIX века после применения им электрохимии.
Щёлочи – наши помощники
Сведения о растворимости в воде можно брать из таблицы растворимости. Р – растворимые основания, то есть щёлочи, м – малорастворимые, н – нерастворимые, черта «–» означает, что такого основания не существует.

В обычных условиях являются твёрдыми веществами. Имеют вид белых порошков, легко впитывающих влагу. Требуют хранения в банках из толстого стекла с широким горлышком или полиэтиленовых емкостях.
Получение оснований
Щёлочь образуется в результате реакции металла и воды с большим выделением теплоты.
2Na + 2H2O>2NaOH + H2
CaO + H2O>Ca(OH)2.
Гидроксиды натрия и калия образуются при воздействии на раствор электрического тока:
KCl + 2H2O>2KOH + H2 + Cl2.
Свойства оснований
Щёлочи реагируют
1. С кислотными оксидами:
2КОН+SO3>K2SO4+H2O.
Щёлочи способны растворять оксидную плёнку алюминия (амфотерного оксида):
2. С кислотами:
NaOH+HCl>NaCl+HOH.
Можно определить, осталась ли щёлочь, если добавить 1-2 капли раствора фенолфталеина. Щёлочь прореагировала полностью, если малиновый цвет окрашивания раствора не появился.
Реакция между основанием и кислотой – реакция нейтрализации. Подобные реакции часто применяют с целью очищения сточных вод промышленных предприятий от щелочей и кислот. Продукты таких реакций – соли, которые более безопасны для окружающей среды. Очень эффективной и экономически выгодной является нейтрализация стоков различных производств.
3. С солями. Это реакции обмена. Происходят в растворе, при этом исходная соль должна быть водорастворимой. А получаемое вещество – нерастворимым:
2NaOH+Mn(NO3)2=Mn(OH)2v+2NaNO3
4. С галогенами.
На холоде: Cl2 + 2NaOH = NaClO+NaCl+H2O.
При нагревании: 3Cl2+6NaOH = NaClO3+5NaCl+3H2O.
Расплавить можно только гидроксиды натрия и калия (температуры плавления соединений составляют 322о и 405о соответственно).
Безопасность в работе со щелочами
Химические ожоги, причиняемые щелочами, в том числе едким натром и едким кали, намного опаснее, чем химические ожоги от кислот. Ожог усугубляется, если кусочек кристаллического вещества прилипает к коже.
Щёлочи способны разъедать много материалов, вызывать серьёзные ожоги на коже и слизистых оболочках, поражать глаза. Поэтому гидроксид натрия называют «едким натром», а гидроксид калия – «едким кали». При работе со щелочами и их растворами, нужно соблюдать осторожность. При попадании раствора щелочи на кожу, нужно сразу смыть его большим количеством воды. Затем обработать это место слабым раствором уксусной или борной кислоты. И опять промыть водой.
Что за вещество «нашатырный спирт»?
Во взаимодействие вступает небольшое количество растворённого аммиака и одновременно распадается на исходные вещества, на что указывает знак «-» в уравнении. Гидроксид аммония, подобно щелочам, изменяет окрашивание индикатора, взаимодействует с кислотными оксидами, кислотами и солями.
2NH4OH+СО2>(NH4)2СО3+H2O
NH4OH+HCl>NH4Cl+H2O
NH4OH+Pb(NO3)2>Pb(OH)2v+2NH4NO3.
Применение оснований

Нашатырный спирт используют не только для того, чтобы привести человека в сознание. С его помощью можно отлично вымыть окна, используя 1 столовую ложку препарата на 1 литр воды. Затем нужно вытереть поверхность бумажными полотенцами.
Если смешать 1 часть нашатырного спирта с 1 частью уксуса, а потом протирать полученным раствором поверхность утюга, то он станет чистым. Но не стоит думать, что получится мгновенный эффект. Поверхность нужно аккуратно потереть.
Широко применяют, прежде всего, гидроксиды кальция и натрия. Гашёная известь – это гидроксид кальция Сa(OH)2. Её используют, как вяжущий материал в строительстве. Смешивают с песком и водой. Полученную смесь наносят на кирпич, штукатурят стены. В результате взаимодействия основания с углекислым газом и оксидом силициума (IV), смесь твердеет. Известь способна поглощать кислые газы. Также может впитывать токсичные вещества, поэтому для здоровья жильцов белить комнату предпочтительнее, чем красить.
Также гидроксид кальция используют в сахарной промышленности, сельском хозяйстве, при изготовлении зубных паст, получении многих веществ.
Гидроксид натрия (каустическую соду) используют при производстве мыла в реакции щёлочи с жиром, при изготовлении лекарств, в кожной промышленности, для очищения нефти. Каустическая сода применяется для чистки масляных пятен. Всем известный «Крот» для труб представляет собой раствор гидроксида натрия, способный растворять жиры и даже волосы.

Щёлочи разъедают стекло и фарфор. Растворяют белковые вещества.
Применяются в медицине в качестве антисептиков, раздражающих и прижигающих препаратов. При заболеваниях пищеварительной системы щелочные минеральные воды действуют оздоравливающе. Эффективны в лечении подагры, стоматита, в лечении заболеваний дыхательной системы. Являются мочегонным средством. Нейтрализуют отравление кислотами.
Немаловажно участие щелочей в изготовлении каучука, искусственного волокна, красителей, очищения предметов из металла, обработки деревянных поверхностей. Являются хладагентом холодильных установок. Используются в сельском хозяйстве, лёгкой промышленности и металлургии.
Щелочные продукты питания
Различают кислые, щелочные и нейтральные продукты питания. Среди щелочных продуктов можно перечислить зелень, репу, огурцы, хрен, сельдерей, лимоны, свеклу, морковь, капусту, цитрусовые, смородину, виноград, вишню, сухофрукты, картофель, перец, помидоры, чеснок.

Примечательно, что в составе нейтральных продуктов содержатся и кислоты, и щёлочи. Это растительное, сливочное масло.
Щёлочи активно используются человеком. При этом следует помнить и в обязательном порядке соблюдать правила техники безопасности.
ЩЕЛОЧИ
Щёлочи — общее название сильных водорастворимых оснований. В медицине щелочи применяют как раздражающие, прижигающие, дезинфицирующие и антисептические средства. Гидроксид кальция — гашеную известь (см. Известь) в виде водных растворов (известковая вода, Aqua calcarea) применяют для нейтрализации кислот.
К щелочам прежде всего относятся гидроксиды щелочных металлов (см.) NaOH, КОН, называемые обычно едкими щелочами (см. Едкий натр, Едкое кали). Свойствами щелочей обладают также гидроксиды щелочноземельных металлов (см.) — Ca(ОН)2, Ba(ОН)2, а также гидроксид аммония NH4OH (см. Аммиак), водные растворы алифатических аминов (см.) и гидразина (см.), гидроксиды тетраалкиламмония. Сходным со щелочами химическим действием обладают щелочные соли слабых кислот (см. Кислоты и основания) — карбонаты (сода, поташ), тетрабораты (например, Na2B4O7), трехзамещенные фосфаты (например, Na3PO4) и др. Свойства едких щелочей проявляют водные растворы алкоголятов щелочных металлов (см. Спирты). В водных растворах едкие щелочи почти полностью диссоциируют (см. Диссоциация в химии) на ионы щелочного металла и гидроксила (ОН-), благодаря чему они являются самыми сильными основаниями, этим же обусловлена высокая основность гидроксидов тетраалкиламмония, не уступающая едким щелочам. Меньшая основность щелочноземельных гидроксидов и гидроксида аммония NH4OH связана с меньшей степенью их диссоциации. Щелочные свойства солей слабых кислот объясняются их гидролизом с образованием едких щелочей: Na2CO3 + Н2O = NaHCO3 + NaOH.
Щелочи — гидроксиды щелочных и щелочноземельных металлов — бесцветные кристаллические вещества, они гигроскопичны, особенно едкие щелочи, расплывающиеся на воздухе. Все щелочи энергично поглощают диоксид углерода (углекислый газ СO2) из воздуха, превращаясь в карбонаты, поэтому их хранят герметически закрытыми. Едкие щелочи (кроме гидроксида лития LiOH) хорошо растворимы в воде (до 50% и выше), а также в метиловом и этиловом спиртах. Гидроксиды щелочноземельных металлов растворимы в воде умеренно, их растворимость повышается от Ca(ОН)2 к Ba(ОН)2. Растворение щелочи в воде происходит со значительным выделением тепла вследствие образования гидратов (см. Гидратация). Растворы щелочи имеют значения pH (см. Водородный показатель), равные приблизительно 11 — 14, и резко изменяют окраску кислотно-щелочных индикаторов (см.). При взаимодействии с кислотами щелочи образуют соли (см.), что широко используется на практике не только для нейтрализации кислот, но и как аналитический метод (см. Нейтрализации метод). При обработке щелочью жиров (см.) происходит их омыление (см.), в результате чего образуются соли жирных кислот — мыла (см.). Едкие щелочи обладают большой химической активностью и реагируют со многими веществами и материалами. Некоторые металлы — алюминий, цинк, олово и др. — реагируют с растворами едких щелочей, например алюминий корродируется даже слабыми щелочами (содой, аммиаком). В концентрированных растворах и особенно в расплавленном состоянии едкие щелочи разрушают стекло, фарфор и даже платину (в присутствии окислителей, в том числе воздуха), что следует учитывать при работе с расплавленными щелочами (в этих случаях используют посуду из железа, никеля или серебра). Едкие щелочи разъедают и разрушают животные и растительные ткани вследствие гидролитического действия на белки, однако растительные ткани подвергаются такому действию щелочи в меньшей степени.
Применение щелочей в дезинфекции основано на их свойствах гидролизовать белки, омылять жиры, расщеплять углеводы, разрушать микробную клетку (см. Дезинфекция, Дезинфицирующие средства).
Из щелочи наиболее активным является едкий натр, или каустическая сода (NaOH), который обладает бактерицидным, вирулицидным, а в высоких концентрациях при повышенной температуре — спороцидным действием; его 2—4% растворы применяют при кишечных и капельных инфекциях бактериальной и вирусной этиологии, а 10% раствор, нагретый до 75°, — при сибирской язве. Этими растворами обеззараживают помещения предприятий общественного питания, овчинно-шубных заводов, складских помещений для сырья животного происхождения, а также Помещений для животных.
Метасиликат натрия (смесь Na2O и SiO2) обладает бактерицидными, отбеливающими и моющими свойствами; его ограниченно применяют для дезинфекции при кишечных и капельных инфекциях бактериальной этиологии, так как 2% раствор метасиликата натрия портит краску, резиновые перчатки, обесцвечивает ткани, на стеклах оставляет несмываемые пятна. Карбонат натрия (сода) обладает слабым бактерицидным действием, его 1 — 2% растворы используют в качестве подсобного средства при кипячении с целью обеззараживания посуды, белья, предметов ухода за больными, а также для влажно-механической уборки помещений, чистки оборудования, мебели.
Гидроксид аммония NH4OH (см. Аммиак) обладает слабыми бактерицидными свойствами и используется в основном для нейтрализации формальдегида после обработки им различных объектов.
Негашеная известь CaO применяется для обеззараживания поверхностей путем их побелки из расчета 1 л 10% водного раствора (известкового молока) на 1 м2, а также для обработки выделений и почвы.
Щелочи как профессиональные вредности
Щелочи применяют в текстильной, бумажной, кожевенной промышленности, мыловарении и др. В организм человека они могут попадать с вдыхаемым воздухом или через рот (при случайном или умышленном приеме внутрь). Щелочи оказывают резкое раздражающее и прижигающее действие на кожу и слизистые оболочки. Едкие щелочи глубже, чем кислоты (см. Серная кислота, Соляная кислота), проникают в ткани, обезвоживают их, омыляют жиры, образуют с белками щелочные альбуминаты, вызывая колликвационный некроз. Тяжесть поражения зависит от концентрации и температуры раствора щелочи, величины его pH. При попадании на кожу щелочи вызывают ожоги (см.), заживление которых протекает более длительно, чем в случае воздействия кислот, так как в процесс вовлекаются глубже расположенные ткани. Общетоксическое действие щелочи выражено слабо и проявляется преимущественно в случаях хронического течения отравления.
При постоянном соприкосновении щелочи с кожей возможно развитие узелковых дерматитов (см.), появление болезненных, длительно не заживающих язвочек (типа «птичьих глазков»), экземы (см.). Кожа становится сухой, между пальцев образуются трещины, ногти истончаются, ломаются, деформируются, отделяются от ногтевого ложа. Прекращение контакта с щелочью приводит к быстрому выздоровлению.
При хроническом воздействии пыли или аэрозоля щелочи на дыхательные пути могут развиться хронические риниты (см.), фарингиты (см.), бронхиты (см.), эмфизема легких (см.). В результате заглатывания пыли или частиц аэрозоля возникают гастриты (см.), в ряде случаев могут наблюдаться язвенные поражения слизистой оболочки желудка.
При остром отравлении аэрозолями или пылью щелочи в высоких концентрациях, попавшими в дыхательные пути с вдыхаемым воздухом, происходит резкое раздражение слизистой оболочки верхних дыхательных путей, развивается трахеобронхит. При остром пероральном отравлении щелочью возникает ожог ротовой полости, пищевода, желудка, мучительная рвота, понос с кровью, сильная жажда, задержка мочи, позже — развивается токсический нефроз, пневмония, гнойный медиастинит, эмпиема плевры, сердечная недостаточность вплоть до коллапса и шока. Иногда отмечают ларингоспазм, отек гортани и легких, психомоторное возбуждение (особенно при отравлении гидроксидом аммония). Нередко происходит перфорация стенки желудка, иногда отмечают пищеводно-желудочные трудно останавливаемые кровотечения, перитонит и (без своевременной профилактики) образование стенозов пищевода, кардиального и пилорического отделов желудка более обширных, чем при отравлении кислотами.
При попадании щелочи в глаза возникает острое раздражение конъюнктивы, помутнение и изъязвление роговицы, повреждения более глубоких слоев глаза — радужки, стекловидного тела и сетчатки, следствием чего может быть слепота.
Первая помощь и неотложная терапия при попадании щелочи на кожу заключается в немедленном смывании щелочи струей воды в течение 5—10 минут, после чего на пораженное место кладут примочки из 5% раствора лимонной, виннокаменной или уксусной кислот. Если щелочь попала в глаза, их немедленно промывают обильной струей воды в течение 10—30 минут, при попадании в глаза гидроксида кальция глаза промывают 5% раствором хлористого аммония или 0,01% раствором тетацина кальция, после чего закапывают 0,5% раствор дикаина или 1 % раствор новокаина.
Экспертиза трудоспособности
Вопросы экспертизы трудоспособности, медицинской и трудовой реабилитации при интоксикациях щелочами решаются с учетом выраженности клинических симптомов интоксикации и гигиенической характеристики условий труда.
Профилактические мероприятия при работе с щелочью предусматривают герметизацию погрузки и выгрузки ГЦ., непрерывность технологического процесса; аппаратура должна быть снабжена укрытиями с местной вытяжной вентиляцией (см.). Под особым контролем должны находиться пылящие процессы (дробление, транспортировка и др.), а также работа с горячими растворами щелочи. Рабочие должны быть обеспечены защитными очками (см.), респираторами (см.), спецодеждой (см. Одежда специальная) и перчатками. Периодически проводятся медосмотры (см. Медицинский осмотр).
Предельно допустимая концентрация в воздухе рабочей зоны установлена для едких щелочей (в пересчете на едкий натр) 0.5 мг/м3, для карбоната кальция (известняка) — 6 мг/м3, карбоната натрия (соды кальцинированной)— 2 мг/м3.
Щелочи в судебно-медицинском отношении
При судебно-химическом исследовании щелочи выделяют из биологического материала путем диализа. При щелочной реакции к диализату прибавляют спиртовой раствор фенолфталеина и избыток хлорида бария. Сохранение диализатом розовой окраски свидетельствует о наличии в нем щелочи. Химическую природу катиона (Na+,К+,Са2+) устанавливают по образованию характерного кристаллического осадка при добавлении к диализату пиросурьмянокислого натрия, винно-каменной кислоты и оксалата аммония; по посинению красной лакмусовой бумажки при отрицательной пробе на сероводород определяют ионы NH. В основе количественного определения щелочи лежит титрование водной вытяжки из исследуемой ткани кислотой в присутствии индикатора (см. Титриметрический анализ).
В задачу судебно-медицинской экспертизы при освидетельствовании потерпевших может входить установление степени тяжести телесных повреждений, причиненных действием щелочи, а при исследовании трупов — установление отравления щелочью как причины смерти. Оценка степени тяжести телесных повреждений в этих случаях проводится обычным порядком (см. Повреждения в судебно-медицинском отношении); диагностика отравления щелочью как причины смерти производится на основании оценки анамнестических и клинических данных, результатов вскрытия трупа, с химических и гистологических исследований.
Библиогр.: Авдеев М. И. Судебно-медицинская экспертиза трупа, с. 367, М., 1976; Вашков В. И. Руководство по дезинфекции, дезинсекции и дератизации, с. 96, М., 1956; он же, Антимикробные средства и методы дезинфекции при инфекционных заболеваниях, с. 33, М., 1977; Вредные вещества в промышленности, под ред. Н. В. Лазарева и И. Д. Гадаскиной, т. 3, с. 320, Л., 1977; 3агора Э. Промышленная офтальмология, пер. с польск., с. 111 и др., М., 1961; Некрасов Б. В. Основы общей химии, т. 2, с. 213 и др., М., 1973; Руководство по судебно-медицинской экспертизе отравлений, под ред. Р. В. Бережного и др., с. 79, М., 1980; Судебная медицина, под ред. А. Р. Деньковского и А. А. Матышева, с. 229, Л., 1976.
А. И. Точилкин; И. В. Буромский (суд.), E. Н. Марченко (гиг.), Н. Ф. Соколова (эпид.).
что такое щелочь?
Гидроксид натрия (лат. Natrii hydroxidum; другие названия — каустическая сода, каустик, едкий натр, едкая щёлочь) — самая распространённая щёлочь, химическая формула NaOH. В год в мире производится и потребляется около 1860 миллионов тонн едкого натра.
Интересна история тривиальных названий как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разъедать кожу, бумагу, и другие органические вещества, вызывая сильные ожоги. До XVII века щёлочью (фр. alkali) называли также карбонаты натрия и калия. В 1736 г. французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия — кальцинированной содой (по растению Salsola Soda из рода Солянка, из золы которого её добывали), а карбонат калия — поташем. В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium — калий.
Щелочи
Смотреть что такое «Щелочи» в других словарях:
щелочи́ть(ся) — щелочить(ся), чу, чишь, чит(ся) … Русское словесное ударение
ЩЕЛОЧИ — ЩЕЛОЧИ, растворимые в воде основания (см.), вещества, дающие в водном растворе ион гидроксила. Ион гидроксила и обусловливает. способность Щ.: 1) реагировать с к тами с выделением тепла и образованием солей (реакция нейтрализации); 2) вызывать… … Большая медицинская энциклопедия
ЩЕЛОЧИ — (едкий натр, едкое кали, негашеная известь). По своему действию к щелочам близки сода и силикат натрия. Щелочные сточные воды поступают в водоемы с сульфатцеллюлозных, шерстеобрабатывающих, текстильных предприятий и коммунально бытового хозяйства … Болезни рыб: Справочник
ЩЕЛОЧИ — ЩЕЛОЧИ, растворимые ОСНОВАНИЯ, которые при реакции с кислотой дают соль и воду. У раствора щелочи рН выше 7, и он окрашивает лакмусовую бумагу в синий цвет. Щелочные растворы используются как чистящее средство. К сильным щелочам относятся… … Научно-технический энциклопедический словарь
Щелочи — Щёлочи гидроксиды щелочных и щёлочноземельных металлов. К щелочам относят растворимые в воде основания. При диссоциации щелочи образуют ионы OH и ион металла. К щелочам относятся гидроксиды металлов подгрупп Iа и IIа периодической системы,… … Википедия
Щелочи — ► alkali, base Растворимые в воде основания. Водные растворы щелочи характеризуются высокой концентрацией гидроксильных ионов ОН. Большинство щелочей – твердые белые весьма гигроскопичные вещества. Растворение их в воде сопровождается выделением… … Нефтегазовая микроэнциклопедия
Щелочи — (хим.) В настоящее время говорят почти исключительно о едких щелочах (см.), но прежде под Щ. разумели вообще вещества, растворы коих имеют щелочную реакцию и вкус. К числу Щ. относили тогда и карбонаты щелочных металлов (см. Калий). Сода и поташ … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
щелочи́ть — чу, чишь; несов., перех. Прибавлять во что л. щелочь или щелок. Щелочить воду … Малый академический словарь
ЩЕЛОЧИ — водные соединения окисей щелочных и щелочно земельных металлов (натрия, кальция и др.). Все Щ. растворимы в воде … Сельскохозяйственный словарь-справочник
ЩЁЛОЧИ
ЩЁЛОЧИ — гидроксиды щелочных металлов (Li, Na, K, Rb, Cs, Fr) и щёлочноземельных металлов (Ca, Sr, Ba, Ra) (I и II группы периодической системы Д. И. Менделеева). Щ. — твердые белые гигроскопические вещества. При их растворении в воде выделяется большое количество теплоты. Щ. разъедают животные ткани, многие соприкасающиеся с ними материалы. Едкие Щ. — самые сильные основания. К ним относятся: гидроксид натрия (едкий натр) NaOH, гидроксид калия (едкое кали) KOH, а также LiOH, RbOH, CsOH. Щ. широко применяются в промышленности.
Смотреть что такое «ЩЁЛОЧИ» в других словарях:
Щёлочи — Щёлочи гидроксиды щелочных, щёлочноземельных металлов и аммония. К щёлочам относят хорошо растворимые в воде основания. При диссоциации щёлочи образуют анионы OH− и катион металла. К щёлочам относятся гидроксиды металлов подгрупп Iа и IIа… … Википедия
не содержащий щёлочи — свободный от щёлочи — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы свободный от щёлочи EN alkali free … Справочник технического переводчика
Щёлочи — ЩЁЛОЧИ, гидроксиды щелочных (едкие щёлочи) и щёлочноземельных металлов. Щелочи сильные основания; едкие щелочи хорошо растворяются в воде, гидроксиды щёлочноземельных металлов плохо. Все щелочи чрезвычайно агрессивны, их растворы разрушают стекло … Иллюстрированный энциклопедический словарь
Едкие щёлочи — хорошо растворимые в воде гидроокиси щелочных металлов, например едкий натр NaOH, едкое кали КОН. Оказывают разъедающее действие на слизистые оболочки и кожу. Широко применяются во многих отраслях промышленности. См. Щёлочи … Большая советская энциклопедия
Щёлочи — (хим.) В настоящее время говорят почти исключительно обедких щёлочах, но прежде под Щ. разумели вообще вещества, растворы коихимеют щелочную реакцию и вкус. К числу Щ. относили тогда и карбонатыщелочных металлов. Сода и поташ, например, имеют… … Энциклопедия Брокгауза и Ефрона
заводнение раствором щёлочи — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN alkaline waterflooding … Справочник технического переводчика
оборудование для закачивания щёлочи (в пласт) — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN caustic flooding equipment … Справочник технического переводчика
раствор щёлочи — отработанная щёлочь щелочные отбросы — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы отработанная щёлочьщелочные отбросы EN alkali liquor … Справочник технического переводчика
устройство для распределения щёлочи в фильтре регенерации анионита — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN anion regeneration tank caustic distributor … Справочник технического переводчика
Щёлочь или щёлок?
Для этого заглянем в словарь:
К щелочам относятся хорошо растворимые в воде основания след. металлов:
Щелочные растворы используются как чистящие средства.
А примерами едких щелочей можно назвать едкий кали и едкий натр.
С помощью едких кали и натра можно, например, сделать растворимыми большинство нерастворимых веществ, а самые сильные кислоты и удушливые пары можно благодаря щелочам лишить всей их жгучести и ядовитости.
Едкие щелочи — очень своеобразные вещества.
На вид это беловатые, довольно твердые камни, ничем как будто не примечательные.
Но попробуйте взять едкое кали или натр и зажать его в руке. Вы почувствуете легкое жжение, почти как от прикосновения к крапиве. Долго держать в руке едкие щелочи было бы нестерпимо больно: они могут разъесть кожу и мясо до кости.
Вот почему их называют «едкими», в отличие от других, менее «злых» щелочей — всем известных соды и поташа. Из соды и поташа, кстати сказать, почти всегда и получались едкие натр и кали.
Кому впервые приходилось погрузить пальцы в раствор едкой щёлочи, тот с удивлением заявляет:
— Как мыло!
И это совершенно правильно. Щёлочь — скользкая, как мыло. Больше того: мыло потому и «мыльно» на ощупь, что его изготовляют с помощью щелочей. Раствор едкой щёлочи и на вкус напоминает мыло.
А теперь, что же такое щёлок?
Для производства мыла лучше всего подходит древесная зола. Причём это должны быть лиственные породы деревьев, так как хвойные породы содержат смолы и их зола не пригодна для таких целей.
Это белое кристаллическое вещество, хорошо растворимое в воде. Для получения поташа используют золу из злаков и водорослей, так как именно калия больше всего в растворимой части растительных остатков (белая «зола» от костра — в основном поташ). Поташ применяют для изготовления жидкого мыла. Поташ зарегистрирован в качестве пищевой добавки Е 501.
Слово поташ произошло от нем. Роttаsсhе – то же от Роtt «горшок» и Аsсhе «зола», потому что щелочную золу получали путем кипячения сожженных частей растений в горшке.
Щелочь: формула, свойства, применение
Каждый сталкивался с таким понятием, как щелочь, но не каждый может точно сказать, что же это такое. Особенно это относится к тем, кто давно окончил школу и начал забывать уроки химии. Что же это за вещество? Какова формула щелочи в химии? Каковы ее свойства? Рассмотрим все эти вопросы в данной статье.
Определение и основная формула
Начнем с определения. Щелочью называется хорошо растворимое в воде вещество, гидроксид щелочного (1-ая группа, основная подгруппа в таблице Менделеев) или щелочноземельного (2-ая группа, основная подгруппа в таблице Менделеева) металла. Стоит заметить, что бериллий и магний, хотя и принадлежат к щелочным металлам, щелочей не образуют. Их гидроксиды относят к основаниям.
Реакции
Щелочи взаимодействуют и с амфотерными оксидами (ZnO, Al2O3). При этом образуются нормальные или комплексные соли. Самая типичная из таких реакций оксид цинка + едкая щелочь. Формула такой реакции:
В показанной реакции образуется нормальная соль натрия Na2ZnO2 и вода.
Реакции щелочей с амфотерными металлами протекают по тому же механизму. Приведем в качестве примера реакцию алюминий + щелочь. Формула реакции:
Это пример реакции с образованием комплексной соли.
Взаимодействие с индикаторами
Другой доступный индикатор, фенолфталеин, в щелочной среде приобретает малиновый окрас. Однако в очень концентрированном растворе (показатель водорода близок к 14) фенолфталеин остается бесцветным, как и в нейтральной среде. Потому лакмус при работе с концентрированными щелочами использовать предпочтительнее.
Метиловый оранжевый индикатор в щелочной среде приобретает желтый окрас, при уменьшении pH среды цвет меняется от желтого до оранжевого и красного.
Физические свойства щелочей
Химический ожог щелочью
При использовании неразбавленных щелочей всегда стоит помнить, что они являются едкими веществами, которые при попадании на открытые участки тела вызывают покраснение, зуд, жжение, отек, в тяжелых случаях образуются пузыри. При длительном контакте такого опасного состава со слизистой органов зрения возможно наступление слепоты.
Щелочь и ее виды

Те, кто знаком с историей мыловарения, слышали, что раньше мыло получали, смешивая животные или растительные жиры со щелоком, в свою очередь полученным из золы. В таком случае вопрос снимается, но неужели и в наши дни щелочь делают из древесной золы?
Нет, но оказывается, что сырье для производства щелочей не менее натурально. Гидроокись калия получают из хлорида калия, который встречается в природе в виде минералов, а натрия гидроокись изготавливается путем электролиза хорошо нам знакомой поваренной соли (хлорида натрия).
Итак, несмотря на то, что в его составе присутствует щелочь, мыло с нуля действительно натуральный продукт. Однако у многих начинающих мыловаров все равно остаются вопросы о щелочи. Какую именно использовать? Чем они различаются? Что за странные аббревиатуры ХЧ и ЧДА?
Давайте попробуем вместе разобраться.
Не так давно ко мне на мастер-класс случайно попали две девочки-школьницы. И они задали вопрос, который, если честно, на некоторое время поставил меня в тупик: «А что же такое щелочь?».
Конечно, мы все можем прочитать в Википедии, что к щелочам относятся хорошо растворимые в воде гидроксиды щелочных и щелочноземельных металлов, но я попробую сформулировать более простое, пусть и не совсем научное определение:

Есть довольно много разных щелочей, но нас с Вами будут интересовать только две из них: КОН и NaOH.
КОН также называют гидроокисью калия, каустическим поташем, едким кали. Химическое «имя» NaOH – натрий гидроокись, кроме этого он также известен как едкий натр или каустическая сода.
Многие химические вещества, получаемые в промышленности, содержат примеси и бывают разной степени очистки. Для создания мыла с нуля щелочи могут быть двух степеней очистки: химически чистыми (ХЧ) и чистыми для анализа (ЧДА). КОН чаще всего встречается ХЧ, гидроокись натрия купить можно обоих видов. Если у Вас есть выбор, то рекомендую взять ХЧ, в ней крупинки одинакового размера, их будет проще растворить. Внешне такая щелочь похожа на сахар. В ЧДА встречаются как более крупные кусочки, так и совсем мелкая пыль.

В свою очередь, для твердого мыла используется гидроокись натрия.
Купить щелочь сейчас не составляет труда, но не спешите сразу варить мыло, сначала как следует изучите теоретические основы, в том числе обязательно ознакомьтесь с техникой безопасности при работе со щелочью.
Я знаю многих мыловаров, которые делают исключительно мыло из основы, так как боятся работать со щелочью. Мыло с нуля, конечно, далеко не самое безопасное хобби, но, хорошо изучив теорию и купив необходимые средства защиты, Вы сведете все риски к нулю.