Что такое прокинетики
Роль прокинетиков в терапии нарушений моторики желудочно-кишечного тракта.
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– К нам присоединился хорошо известный профессор Симаненков Владимир Ильич.
Владимир Ильич Симаненков, профессор:
– Мне представляется, что деятельность интернет-сессий чрезвычайно важна и полезна в свете стратегической линии последипломного образования концепции непрерывного профессионального образования. Я всю жизнь проработал в Северо-Западном университете. Когда человек приезжает раз в пять лет, большая часть информации устарела, и на коротком цикле восстановить это все чрезвычайно сложно. И когда в режиме нон-стоп проводятся такие сессии, в любом уголке нашей огромной Родины врачи-интернисты могут получить самые свежие знания из первых уст. Потому что у вас выступают лидеры мнений – люди, которые имеют и огромный собственный опыт и, кроме того, находятся в гуще информационных потоков по всем основным разделам.
Уважаемые коллеги, мое сегодняшнее сообщение посвящено роли прокинетиков в терапии нарушений моторики. Как писал профессор Шептулин, не бывает заболеваний пищеварительной системы, которые не сопровождались бы теми или иными моторными расстройствами. Другой вопрос, что условно выделяют первичные моторные расстройства, куда включают неэрозивные формы рефлюкской болезни, функциональную диспепсию, дисфункцию сфинктера Одди, дискинезию желчного пузыря, синдром раздраженной кишки, синдром функционального запора. И вторичные моторные расстройства с диспепсией, диареей или запором.
А как же нам помочь этим пациентам? Условно ваш покорный слуга разделил все препараты на две большие подгруппы. Это лекарственные средства прямо влияющие на моторику и лекарственные средства опосредованно влияющие на моторику. Дефицит времени не позволяет мне рассмотреть правую графу более детально. Но если мы с вами вспомним, например, ингибиторы протонной помпы. С одной стороны это самые мощные антисекреторные препараты. Но с другой стороны, меняя РН в антральном отделе, они меняют скорость антродуоденального перехода. И так можно было бы обсудить каждый из представленных классов.
Давайте посмотрим на левую группу. Это лекарственные средства прямо влияющие на моторику. Можно выделать четыре основных группы. Это нормокинетики, спазмолитики, блокаторы моторики и прокинетики. Нормокинетики – это препараты, которые влияют на эндорфинные рецепторы в пищеварительной системе. И у нас зарегистрировано два препарата – это даларгин и тримебутин. Группа спазмолитиков представлена пятью подгруппами. Наибольшее распространение имеют миотропные спазмолитики, и из них можно выделить три основных группы: это блокаторы натрия, блокаторы кальция и ингибиторы фосфодиэстеразы четвертого типа. Что касается блокаторов моторики типа лоперамида, они не используются для лечения и имеют обрывающий характер, например, при диарейном синдроме. И прокинетики, о которых мы сегодня поговорим подробнее.
Итак, прокинетики. У нас с вами, к сожалению, только четыре прокинетика. Это метоклопрамид, домперидон, итоприд и прукалоприд. Я желтеньким пометил цизаприд и мосаприд, поскольку их регистрация прекращена. Почему? Как оказалось, лекарственные средства, влияющие на дофаминергические рецепторы, потенциально могут ухудшать прогноз сердечнососудистых заболеваний или увеличивать вероятность их развития. И регистрация в ряде зарубежных стран этих двух прокинетиков была прекращена. Итак, в России зарегистрировано четыре прокинетика, из них прукалоприд, который появился на нашем рынке около двух лет тому назад, является энтерокинетиком, то есть он селективно работает на толстую кишку. Что касается верхних отделов желудочно-кишечного тракта, то у нас есть три препарата: метоклопрамид, домперидон и итоприд. Давайте с ними разбираться.
Прежде чем поговорить о каждом из них, я хотел бы процитировать статью Владимира Трофимовича Ивашкина с соавторами 2012 года, где рассматривались перспективные прокинетики. Но я сейчас не буду останавливаться на детальном их рассмотрении. Ожидать, что в ближайшие два-три года они будут зарегистрированы в России, не приходится. Пока у нас их нет и будем ориентироваться на те, что зарегистрированы.
Есть такое понятие NNT – «Number needed to Treat». Этот параметр отражает количество пациентов, которое необходимо лечить данным образом, чтобы предотвратить один дополнительный эпизод заболевания или добиться положительного исхода для одного пациента по сравнению с контрольной группой, то есть с группой, в которой обычно применяется плацебо. Идеальный случай, когда NNT=1, тогда всем пациентам, которые получали это лекарство, стало лучше, а в контрольной группе ни у кого лучше не было. Но как мы понимаем, учитывая плацебо-эффекты, NNT=1 – это некий идеал. Чем больше NNT, тем менее эффективно лечение.
Зачем я вам напомнил этот показатель? Существуют данные об NNT для различных методов лечения такого моторного расстройства как функциональная диспепсия. Я обратил бы ваше внимание на первую строчку – это эрадикация Helicobacter pylori. Обратите внимание, что NNT для этого метода лечения – 17. И это значит следующее. В Маастрихтском соглашении сказано, что в странах с высокой инфицированностью Helicobacter pylori при функциональной диспепсии нужно проводить эрадикацию Helicobacter pylori. Вероятно, мы с вами не будем спорить с Маастрихтом-4, но мы с вами видим NNT, и мы можем сказать, что надеяться на кардинальные изменения клинических проявлений функциональной диспепсии после эрадикации очень трудно. А теперь два других строчки: это ингибиторы протонной помпы и прокинетики. Для ингибитора протонной помпы NNT – 10, а для прокинетиков – 4. К чему я клоню? Конечно, не к тому, что не нужно использовать ингибиторы протонной помпы при моторных расстройствах желудка. Нет, но к тому, что в ряде случаев клиническая эффективность прокинетиков, по меньше мере, не будет уступать ингибиторам, а в ряде случаев будет превышать. И все эти данные получены путем мета-анализа, то есть обладают высокой степенью доказательности.
Теперь давайте вернемся к тем препаратам, о которых я говорил ранее. Что касается метоклопрамида, то это препарат, который на нашем рынке свыше 40 лет. Он является антагонистом рецепторов серотонинергических третьего типа, антагонистом дофаминергических рецепторов второго типа и агонистом рецепторов серотонина четвертого типа. И проблема в том, что этот препарат хорошо проходит через гематоэнцефалический барьер. Отсюда его влияние как на периферию, на нижнюю треть пищевода, желудок и дуоденум, так и на ЦНС. И вы видите, что побочные эффекты, они были зарегистрированы сразу после регистрации, экстрапирамидные нарушения, сонливость, астенизация. Но по мере многолетнего использования данного препарата было показано, что частота этих нарушений велика. И 26 июля 2013 года Европейское медицинское агентство (EMA) поручило Комитету по контролю за лекарственными средствами сформулировать изменения в использовании препаратов, содержащих метоклопрамид. Я не буду зачитывать все, скажу, что в сухом остатке. А в сухом остатке получается, что, во-первых, не нужно лечить метоклопрамидом больше пяти дней, во-вторых, не превышать дозу 30 миллиграмм и, в-третьих, нужно учитывать, что метоклопрамид не рекомендуется для лечения функциональных расстройств желудка, изжоги или при нарушениях антродуоденального перехода.
И кому тогда вообще назначать метоклопрамид? Судя по литературным данным, остается одно, но существенное показание – это пациенты, страдающие онкологической патологией и получившие химиотерапию, с упорными рвотами, тошнотой и так далее. Этим пациентам можно назначать метоклопрамид.
Теперь поговорим о домперидоне. Домперидон также на нашем рынке достаточно давно. Мы знаем, что он является селективным D2 антагонистом, то есть блокирует рецепторы дофаминов второго типа. И исходно описанные побочные эффекты рассматривались как очень редкими. Что значит очень редкие? Это значит, что они появлялись реже, чем один раз по сравнению с тысячью случаев применения. Это связано с низкой проницаемостью гематоэнцефалического барьера по отношению к этому лекарственному средству. Но последние годы появились новые данные о возможности негативного влияния на сердечнососудистую систему домперидона. Первоначально забили тревогу у нас. Департамент государственного регулирования лекарственных средств направил производителям препаратов, содержащих домперидон, рекомендации об изменении инструкции по применению данных препаратов и о переводе их из безрецептурного в рецептурный статус. Но, наблюдая за продажами в аптеках за литературой, я как-то не заметил последствий этого письма. А в 2010 году в Европе были опубликованы результаты двух новых эпидемиологических исследований. И было показано, что у пожилых больных старше 60-ти лет, получавших высокие дозы домперидона, повышается риск развития жизнеугрожающих желудочковых аритмий и внезапной сердечной смерти. И получение вот этих двух работ привели к тому, что в 2011 году регуляторные органы Великобритании приняли соответствующее решение, и в марте этого года Европейское медицинское агентство поручило Комитету по контролю лекарственных средств обобщить все данные, посвященные рискам, пользе и так далее побочным эффектам домперидона. К сожалению, судя по сайту, доклад этого комитета пока не опубликован. Но что же делать практическим врачам по отношению к этому препарату? Я думаю, что нужно сформулировать следующим образом: если у человека имеется хроническая сердечная недостаточность, если у него имеется удлинение интервала QT на электрокардиограмме, если он пожилой, то лучше на сегодняшний день от назначения домперидона воздержаться.
И теперь давайте посмотрим на итоприд. Как и предшествующий препарат, он блокирует дофаминергические рецепторы второго типа. Но кроме того, он блокирует фермент холинэстеразу – фермент, который в норме расщепляет ацетилхолин. В результате он работает не только через аденилатциклазу, но и увеличивает период полураспада ацетилхолина, и в результате плотность и воздействие на D2 рецепторы как бы снижается. И в результате мы пока не имеем сообщений о негативном влиянии итоприда на интервал QT. Это плюсы фармакокинетики. Обратите внимание, что он метаболизируется без участия цитохрома Р450, значит мы можем не опасаться лекарственных взаимодействий нежеланных.
Теперь ключевой вопрос о брендах и дженериках. 21 ноября наш министр, профессор Скворцова выступала на президиуме правительства Российской Федерации. И в своем выступлении она подчеркнула, что Россия находится на третьем месте в мире по удельному весу дженериков. Хорошо это или плохо? Наверное, надо сначала спросить – а каково качество этих дженериков? И возвращаясь к этой теме, хочу подчеркнуть, что у нас зарегистрировано два итоприда. Это брендовый препарат Ganaton и дженериковый препарат Itomed. Когда мы сравниваем дженерик и бренд, нас интересует их эквивалентность. Существует три вида эквивалентности: фармацевтическая, терапевтическая и биоэквивалентность. И парадокс заключается в том, что ни FDA (Food and Drug Administration), ни Европейское медицинское агентство, ни российский законодатель не требует доказать терапевтическую эквивалентность дженериков. В нашем законе 2010 года сказано и/или терапевтическая эквивалентность. Но какая же дженериковая компания сама пойдет на проведение крайне дорогостоящих исследований терапевтической эквивалентности. Поэтому большинство компаний ограничивается проверкой биоэквивалентности на здоровых молодых ребятах.
В классификаторе Римский Консенсус III выделяют два основных варианта функциональной диспепсии: постпрандиальный дистресс-синдром и эпигастральный болевой синдром. И Римские критерии III рекомендуют три основных подхода: ингибиторы протонной помпы, эрадикация Helicobacter pylori и прокинетики. И наша кафедра решила провести инициативное исследование – изучить клиническую эффективность препарата Itomed и посмотреть на его дизайн – открытое, контролируемое, рандомизированное, с параллельными группами, моноцентровое.
Вот дизайн этого исследования. Суть такая: путем рандомизации были выделены группы, которые получали Itomed, и группы, которые только по требованию редко получали не всасывающийся антацид. И что у нас получилось? Как правило, мы имеем дело с комбинированными нарушениями моторики. Римские критерии III выделили эпигастральный болевой синдром и постпрандиальный дистресс-синдром. А у наших реальных больных всегда ли эти два синдрома выделены в чистом виде? По нашим данным, чаще всего имеется сочетание и тяжести в эпигастрии, и чувство раннего насыщения, и боли в эпигастральной области. И посмотрите на динамику симптомов. Вы видите, что в рандомизированном исследовании Itomed показал свою клиническую эффективность. И обратите внимание, он влияет отчетливо на гастроэзофагеальный рефлюкс. А у пациентов с постпрандиальным синдромом он действует нетолько на тяжесть в эпигастральной области, не только на раннее насыщение, но и на боли в эпигастральной области. А вот не диспептические симптомы у пациентов с постпрандиальным дистресс-синдромом под влиянием Itomed особенно никак не изменились, точнее, они изменились, но так же, как при использовании плацебо.
Вообще проблема плацебо в гастроэнтерологии крайне сложная, по некоторым авторам достигает 42% плацебо-эффект. Поэтому создается море возможностей для различных терапевтических спекуляций. Качество жизни улучшается. Конечно, когда перестает беспокоить боль и тяжесть, конечно, улучшается качество жизни и уменьшается тревожность. И кроме того, под влиянием данного лекарственного средства улучшается и физиологический, и психологический компонент здоровья. И на этой картинке видно, что у всех пациентов улучшение несомненное.
Я благодарю вас за внимание. Но прежде, чем закончить, я хотел бы сказать следующее. Уважаемые коллеги, мне представляется, что мы с вами несколько деформировали структуру лекарственных назначений при моторных расстройствах. Порой мы используем препараты, влияющие на пищеварение, на кислотопродукцию, забывая о том, что в основе многих функциональных расстройств лежит моторная дисфункция и диссоциация секреторно-моторная. Мне думается, что арсенал интерниста, арсенал гастроэнтеролога не очень широкий пока, но у нас есть препараты, и мы должны знать и плюсы их, и минусы.
Прокинетики сегодня: между Сциллой и Харибдой
В статье приведена сравнительная оценка клинической эффективности и безопасности применения домперидона и итоприда при функциональной диспепсии.
This article provides a comparative evaluation of domperidone and itopride clinical efficacy in functional dyspepsia and security.
Большинство заболеваний пищеварительного тракта так или иначе протекает с нарушениями моторной функции пищевода, желудка, тонкой или толстой кишок. Двигательные расстройства провоцируют застой, ретроградный пассаж содержимого, включающего агрессивные для верхних отделов желудочно-кишечного тракта (ЖКТ) компоненты, и могут формировать основные симптомы заболевания. При функциональной диспепсии, гастроэзофагеальной рефлюксной болезни и др. в настоящее время применяют лекарственные средства — прокинетики.
Прокинетики — препараты, усиливающие моторную активность органов пищеварительного тракта и препятствующие антиперистальтическим сокращениям гладкой мускулатуры. Прокинетическое действие обусловлено влиянием на различные рецепторы: метоклопрамид и домперидон блокируют дофаминовые рецепторы, мозаприд стимулирует 5-НТ4-рецепторы, итоприд оказывает комбинированное подавляющее действие на дофаминовые рецепторы и ацетилхолинэстеразу.
В современной Классификации фармакологических групп места для прокинетиков не предусмотрено. Применяемые в РФ препараты, обладающие прокинетической активностью, относятся к двум фармакологическим группам: «Стимуляторы моторики ЖКТ, в том числе рвотные средства» (итоприд), «Противорвотные средства» (метоклопрамид, домперидон). Цизаприд и тегасерод к настоящему моменту отозваны с фармацевтического рынка в связи с большим количеством случаев побочных кардиальных эффектов.
Метоклопрамид является антагонистом дофаминовых D2-рецепторов, серотониновых 5-НТ4-рецепторов, в высоких дозах обладает способностью блокировать 5-НТ3-рецепторы, чем обусловлен его противорвотный эффект. Препарат, кроме того, является прямым миостимулятором для гладкомышечной мускулатуры. Фармакодинамическими эффектами метоклопрамида являются повышение тонуса нижнего пищеводного сфинктера, усиление моторики (тонуса и амплитуды сокращений) желудка и тонкой кишки, ускорение опорожнения желудка, улучшение антродуоденальной координации. Препарат нормализует отделение желчи (повышает давление в желчном пузыре и желчных протоках, уменьшает спазм сфинктера Одди, устраняет дискинезию желчного пузыря). Однако за счет высокой проницаемости через гистогематические барьеры метоклопрамид часто вызывает экстрапирамидные расстройства, оказывает седативный эффект, увеличивает секрецию пролактина, вызывает транзиторное повышение уровня альдостерона.
Наиболее часто в настоящее время используются препараты домперидон и итоприд.
Домперидон является высокоселективным блокатором периферических D2-рецепторов, не проникает через гематоэнцефалический барьер, в связи с чем у него не наблюдаются побочные эффекты, присущие метоклопрамиду. На серотониновые рецепторы, в отличие от названных выше препаратов, домперидон не влияет. Домперидон увеличивает тонус нижнего пищеводного сфинктера, моторную активность желудка и двенадцатиперстной кишки, улучшает антродуоденальную координацию.
Наиболее значимыми побочными действиями домперидона считаются гиперпролактинемия и связанные с ней гинекомастия, галакторея и аменорея. Частота гиперпролактинемии при стандартном курсе терапии составляет 1,3%. Возможно развитие экстрапирамидных расстройств, но они возникают, по данным клинических исследований, у 0,05% больных. К числу менее значимых нежелательный реакций, возникающих при использовании домперидона, следует отнести сухость во рту (1,9%), головную боль (1,2%), диарею (0,2%) и кожную сыпь (0,1%) [1].
Итоприд является антагонистом D2-рецепторов и блокатором ацетилхолинэстеразы. Препарат в минимальной степени проникает через гематоэнцефалический барьер. Кроме того, описано модуляторное влияние итоприда на гипоталамо-гипофизарно-адреналовую систему благодаря повышению концентрации соматостатина, мотилина и снижению уровней холецистокинина и адренокортикотропного гормона [2]. Побочными эффектами итоприда являются лейкопения, тромбоцитопения, аллергические реакции, гиперпролактинемия, тошнота, желтуха, тремор и др.
Несмотря на то, что основные фармакодинамические эффекты, побочные действия домперидона и итоприда изучены и описаны, сегодня ведутся горячие дискуссии по поводу сравнительной безопасности этих двух препаратов. Первый объект дискуссии — влияние прокинетиков на интервал QT; второй — особенности метаболизма, определяющие риски лекарственных взаимодействий при применении того или иного препарата… Или не определяющие…
Проблеме удлинения интервала QT в последние годы уделяется повышенное внимание как к установленному и достаточно распространенному предиктору фатальных нарушений ритма, приводящих к внезапной смерти. Синдром удлиненного интервала QT представляет собой сочетание удлинения этого интервала на стандартной электрокардиограмме (ЭКГ) и угрожающей жизни полиморфной желудочковой тахикардии (torsade de pointes — «пируэт»). Пароксизмы желудочковой тахикардии типа «пируэт» клинически проявляются эпизодами потери сознания и нередко заканчиваются фибрилляцией желудочков, являющейся непосредственной причиной внезапной смерти. Сейчас для оценки продолжительности интервала QT используют не абсолютную, а корригированную, независимую от частоты сердечных сокращений и пола величину (QTc), рассчитываемую по формуле Базетта. Удлинение интервала QT диагностируют при QTc, превышающем 0,44 с.
Причины возникновения синдрома удлиненного интервала QT (нарушений деятельности ионных каналов, удлиняющих время реполяризации миокарда) условно делят на две группы — врожденные и приобретенные.
К врожденным причинам относятся 13 установленных на сегодняшний день молекулярно-генетических вариантов каналопатий, клиническое течение которых варьирует от благоприятного, не требующего лечения, до злокачественного, требующего пожизненной терапии или хирургического вмешательства [4, 5].
Приобретенные причины: пожилой возраст, заболевания сердца (острый инфаркт миокарда, постинфарктный кардиосклероз, атриовентрикулярная блокада, миокардиты, кардиомиопатии, застойная сердечная недостаточность, ревмокардиты, перикардиты, пороки сердца и др.), синусовая брадикардия, заболевания головного мозга (острые нарушения мозгового кровообращения, субарахноидальные геморрагии, хроническая цереброваскулярная недостаточность, опухоли), травмы (грудной клетки и черепно-мозговые), эмболии, тромбозы, нарушения электролитного обмена (гипокалиемия, гипокальциемия, гипомагниемия), гипофункция щитовидной железы, феохромоцитома, многократная рвота, синдром Кона, автономная нейропатия у больных с сахарным диабетом I и II типов, гепатиты, заболевания почек, крови, алкоголизм (у мужчин, не у женщин), малобелковая диета, нервная анорексия, отравление фосфорорганическими соединениями, ртутью, действие яда скорпиона, ятрогенное воздействие [3, 6–15].
Ятрогенные причины пролонгированного интервала QT:
1) оперативные вмешательства на головном и спинном мозге, шее, органах грудной клетки, стволовая ваготомия;
2) применение препаратов, удлиняющих продолжительность интервала QT (антиаритмическая моно- или комбинированная терапия (классы IA, IC, III антиаритмиков), некоторые нейролептики, анксиолитики, нормотимики, антидепрессанты, противогистаминные препараты, диуретики, сердечные гликозиды, фторхинолоны, макролиды, прокинетики).
Наиболее четко проблема ятрогенного синдрома удлиненного QT обозначена в неврологии и психиатрии. Антиконвульсанты, антипсихотики, анксиолитики, нормотимики и антидепрессанты способны блокировать калиевые, натриевые каналы (при дефекте гена SCN5 A) и кальциевые каналы определенных типов, вызывая их функциональную недостаточность [12, 16–18]. Частота побочных эффектов психотропной терапии, по данным клинических исследований, может достигать 75%. У пациентов с психическими заболеваниями наблюдается более высокий риск внезапной смерти. Так, показано 2–5-кратное увеличение частоты внезапной смерти у больных шизофренией, по сравнению с пациентами без этого заболевания [6–8]. Описаны случаи внезапной смерти, связанной с увеличением продолжительности интервала QT, у пациентов, длительно принимавших трициклические антидепрессанты [11]. База данных о кардиотоксичности препаратов, применяемых в других областях медицины, формируется.
Таким образом, прокинетики почти теряются в представленном многообразии причин развития синдрома удлиненного QT. Риск возникновения фатальных аритмий имеется и при погрешностях в диете, и при компенсированных заболеваниях внутренних органов, и при применении препаратов с, как считают, высоким профилем безопасности (диуретиков, макролидов, фторхинолонов и др.).
Перед назначением препарата, удлиняющего QT, в том числе прокинетика, следует учитывать наличие перечисленных выше факторов риска и оценивать возможность лекарственных взаимодействий при назначении комплексной терапии.
Факторы, увеличивающие риск лекарственного пролонгирования QT у лиц без врожденного или приобретенного синдрома удлиненного QT:
Например, на фоне приема кетоконазола или эритромицина (ингибиторы CYP3A4) замедляется метаболизм цизаприда (субстрат CYP3A4). Подобные сочетания опасны в плане развития синдрома удлиненного QT. В случае с макролидом эта опасность усиливается, так как и эритромицин, и цизаприд являются блокаторами калиевых каналов [14].
Европейское Медицинское Агенство информировало о начале ревизии данных о препаратах, содержащих домперидон. Ревизия была инициирована Бельгийским Федеральным агентством по лекарственным средствам и средствам медицинского назначения (FAMHP). Ранее побочные действия домперидона были рассмотрены Рабочей группой по фармаконадзору, которая в 2011 году рекомендовала пересмотр и обновление информации по препаратам, содержащим домперидон, в которой должен быть отражен риск кардиальных побочных эффектов и должны содержаться рекомендации по применению домперидона у пациентов с заболеваниями сердца [19].
Что касается влияния итоприда на продолжительность интервала QT, данные по этому препарату представляются неполными. Доступные критическому осмыслению сведения о влиянии итоприда на интервал QT отсутствуют. Представленные фирмой Axcan Pharma результаты исследования свидетельствовали о том, что даже в дозах, значительно превышающих терапевтические, увеличение продолжительности QTc у здоровых добровольцев не достигло 5 мс, что позволило сделать вывод об отсутствии влияния препарата на интервал QT. Однако общее количество участвовавших в исследовании больных говорит о том, что рано ставить точку в этом вопросе (суммарное количество пациентов в 4 группах равно 162) [20].
Окончательное же заключение об отсутствии влияния исследуемого препарата на продолжительность интервала QT должно быть сделано после более тщательной оценки безопасности на более поздних стадиях клинических исследований в различных целевых популяциях [21, 22]. И с участием большего количества пациентов. Исследования по безопасности итоприда у пацентов европейской популяции (а это важно, см. далее) с врожденным и приобретенным синдромом удлиненного QT не проводились. Не представлены данные о лекарственных взаимодействиях итоприда с препаратами, увеличивающими продолжительность интервала QT.
Означают ли приведенные сведения более высокий риск применения домперидона с точки зрения влияния на интервал QT, по сравнению с другими препаратами, оказывающими такой же эффект? Это означает лишь то, что для домперидона накоплено больше сведений по данной проблеме, достаточных для всестороннего анализа его кардиотоксичности, и высокую заинтересованность специалистов разных уровней в комплексной оценке безопасности широко используемого препарата и снижении риска. Для других препаратов, например итоприда, таких данных недостаточно. Это при том, что при лечении функциональной диспепсии есть «существенная польза» (результат метаанализа) от назначения домперидона и «нет пользы» (результаты отдельных клинических исследований) от применения итоприда [23]. В исследовании, правда, сравнительно небольшом, с комплексной оценкой воздействия различных доз итоприда на параметры моторной активности ЖКТ у здоровых лиц не было обнаружено статистически значимого влияния препарата на опорожнение желудка, транзит химуса от ротовой полости до слепой кишки, объем желудка натощак, максимально переносимый объем и совокупную оценку симптомов в ответ на введение стандартной питательной смеси [24]. По результатам двух (международного и североамериканского) исследований, в которых сравнивалось влияние итоприда (n = 203) и плацебо (n = 207) на симптомы функциональной диспепсии, эффективность итоприда не отличалась от эффективности плацебо [25]. Была более ранняя публикация G. Holtmann, N. J. Talley с соавт. (2006), где сделано утверждение об эффективности итоприда при функциональной диспепсии [26]. На данную публикацию имеется множество ссылок в отечественной литературе. Однако более поздняя публикация N. J. Talley с соавт. от 2008 года фактически опровергает более ранние данные [25]. Имеются, правда, многочисленные публикации российских и зарубежных (азиатские страны) авторов, в которых приводятся данные исследований, свидетельствующих о эффективности итоприда при функциональной диспепсии [27–30].
Отсутствие исчерпывающих данных по безопасности итоприда в европейской популяции связано с тем, что препарат не зарегистрирован в США и в большинстве стран ЕС. На основании данных, представляемых исследователями азиатских стран, невозможно делать выводы о высоком профиле безопасности итоприда для пациентов — представителей европейской популяции и малых этносов РФ из-за особенностей его метаболизма. Преимуществом итоприда называют единственно возможный путь его биотрансформации: с помощью одной из форм флавин-содержащих монооксигеназ (FMOs), FMO3. Т. е. метаболизм итоприда не зависит от активности цитохрома P-450. Но хорошо ли это?
Наряду с цитохромом Р-450, и другие системы участвуют в биотрансформации ксенобиотиков, в том числе лекарственных средств. Пока не получила должного внимания система флавин-содержащих монооксигеназ (ФСМ), хотя осознание ее значимости в метаболизме существенно растет. У человека обнаружено 5 функциональных форм фермента. Из них в большей степени представлена третья форма (ФСМ3). У новорожденных ФСМ3 нет, есть ФСМ1. В последующим в печени происходит замена ФСМ1 на ФСМ3 [31]. Для генов, кодирующих ФСМ, характерен генетический полиморфизм. Система ФСМ формировалась для детоксикации катионов, при этом катионы флоры и фауны разных географических регионов имели и имеют значительные различия. Поэтому предположительно в разных популяциях людей развивались особые варианты изоформ ФСМ, метаболизирующие разные химические соединения [32, 33].
С одной стороны, у лекарственных препаратов, метаболизирующихся ФМО, можно ожидать меньшую вариабельность фармакокинетики и меньшее количество лекарственных взаимодействий при совместном применении с индукторами или ингибиторами, так как изоформы ФМО плохо индуцируются и ингибируются [32]. С другой стороны, если мы говорим о высокой безопасности в азиатских популяциях итоприда, который биотрансформируется только с помощью ФМО3, а активность ФМО3 зависит от генетического полиморфизма, и у ФМО3 различных географических регионов могут быть разные субстраты, можем ли мы утверждать, что препарат безопасен у пациентов в РФ? Требуются масштабные клинические исследования.
Нельзя забывать, что между субстратами ФМО3 может возникнуть конкуренция за метаболизирующий фермент, что может привести к увеличению их биодоступности и замедлению выведения. Субстратами ФМО3 являются триметиламин, тирамин (из пищи), никотин, часто применяемые лекарственные препараты циметидин, ранитидин, кетоконазол, тамоксифен, итоприд и др. [33].
При заболеваниях печени было бы логичным ожидать снижение активности ФМО, между тем данных об изменениях фармакокинетики итоприда при заболеваниях печени/печеночной недостаточности, сведений о безопасности препарата при этих состояниях не представлено, соответствующих указаний и противопоказаний в инструкции нет [34]. По некоторым данным, окончательная трансформация ФМО печени от ФМО1 к ФМО3 происходит к 18 годам [35]. Таким образом, назначение итоприда лицам до 18 лет рискованно. Противопоказанием по инструкции, утвержденной в РФ, является детский возраст (до 16 лет).
Приведенные сведения свидетельствуют, что до широкого применения итоприда в российских популяциях необходимы масштабные исследования по безопасности его использования именно в этих популяциях. Домперидон как множество других препаратов метаболизируется с помощью CYP3A4. Его применение в составе комбинированной терапии не должно приводить к ятрогенным клинически значимым лекарственным взаимодействиям, так как субстраты, индукторы и ингибиторы CYP3A4 хорошо изучены и широко представлены в доступной литературе. А совместного назначения домперидона и ингибиторов CYP3A4 следует избегать.
Еще одним объектом дискуссии по домперидону является его лекарственное взаимодействие с ингибиторами протонной помпы (ИПП). Доказано, что при повышении внутрижелудочного рН снижается биодоступность домперидона. Максимальная концентрация прокинетика на фоне приема омепразола снижается на 16% [36]. В связи с этим в некоторых, в основном устных, докладах утверждается, что нельзя применять домперидон одновременно (в один прием) с ИПП. Однако исследований, свидетельствующих о высокой эффективности совместного применения этого прокинетика и ИПП, проведено достаточно много [37, 38]. Так как ИПП вызывают многочасовую блокаду кислотопродукции, перекрывающую время между приемами очередных доз препаратов, не имеет значения, применяется ли домперидон одновременно с ИПП или с каким-либо временным интервалом.
Таким образом, домперидон не является более кардиотоксичным, чем другие препараты, пролонгирующие QT, но не стоит забывать о необходимости индивидуальной оценки риска развития синдрома удлиненного QT. Эффективность итоприда при функциональной диспепсии продолжает обсуждаться, этот препарат не имеет доказанных преимуществ перед домперидоном по безопасности в европейской популяции и малых этнических популяциях РФ.
Литература
* ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
** ФГБУН НЦБМТ ФМБА России, Москва
Перспективы применения нового прокинетика с двойным механизмом действия в терапии гастроэзофагеальной рефлюксной болезни
И.В. Маев, А.А. Самсонов, А.Н. Одинцова, Е.В. Белявцева, М.Г. Задорова
ГОУ ВПО РГМУ Росздрава, Москва Обсуждаются проблема развития гастроэзофагеальной рефлюксной болезни (ГЭРБ) и тактика ее лечения с учетом основных патогенетических механизмов. На сегодняшний день ведущим направлением в лечении ГЭРБ является кислотосупрессивная терапия, в частности, с использованием ингибиторов протонной помпы (ИПП). Однако с учетом того, что даже самые эффективные ИПП не влияют на первопричину болезни – нарушение двигательной функции пищеварительного тракта, при лечении больных ГЭРБ дополнительно показано использование лекарственных средств, обладающих прокинетическим эффектом на верхние отделы желудочно-кишечного тракта. Препаратом нового поколения прокинетиков является итоприда гидрохлорид (Ганатон) – антагонист дофаминовых D2-рецепторов и блокатор ацетилхолинестеразы. Особенности фармакодинамики и фармакокинетики Ганатона позволяют применять его у больных ГЭРБ в режиме длительной противорецидивной терапии как в комбинации с ИПП, так и в виде монотерапии.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, нижний пищеводный сфинктер, дуодено-гастральный рефлюкс, прокинетики, итоприда гидрохлорид, ингибиторы протонной помпы
В развитии многих распространенных гастроэнтерологических заболеваний, в первую очередь гастроэзофагеальной рефлюксной болезни (ГЭРБ), важную роль играют нарушения двигательной функции пищеварительного тракта. В основе развития ГЭРБ лежит нарушение моторно-эвакуаторной функции органов эзофагогастродуоденальной зоны, приводящее к систематическим, длительным забросам в пищевод желудочного и дуоденального содержимого, являющегося повреждающим агрессивным агентом для слизистой оболочки пищевода.
Патогенетические механизмы развития ГЭРБ
Считается, что ГЭРБ развивается как результат дисбаланса между агрессивным воздействием забрасываемых компонентов и трехступенчатой системой защиты пищевода, включающей противорефлюксные барьеры, механизмы очищения от кислоты и тканевую резистентность [1–3]. Компоненты, определяющие повреждающие свойства забрасываемых веществ, представлены соляной кислотой, пепсином, солями желчных кислот (связанными и свободными) и панкреатическими ферментами. Повреждение пищевода определяется значением рН желудочного содержимого. Если значение рН нейтральное или щелочное, как у пациентов после гастрэктомии или с атрофическим гастритом, повреждающими агентами являются свободные соли желчных кислот и ферменты поджелудочной железы. Вместе с тем ионы водорода являются основным повреждающим агентом рефлюктата, причем их способность оказывать повреждающее действие зависит и от времени воздействия, и от концентрации, т. е. от рН [2, 4].
Антирефлюксные барьеры, представляющие первую ступень трехступенчатой защиты пищевода, включают нижний пищеводный сфинктер (НПС), интраабдоминальный сегмент пищевода, диафрагмальные ножки, диафрагмально-пищеводную связку, розетку слизистой оболочки и острый угол Гиса [5]. Большое значение придается снижению базального давления в области НПС [6]. НПС и диафрагма – главные структуры, ответственные за создание высокого давления (от 10 до 30 мм рт. ст.) в желудочно-пищеводном переходе. Эта зона предотвращает рефлюкс, поскольку отделяет две смежные зоны низкого давления: в полости желудка (на 5 мм рт. ст.выше атмосферного давления) и в полости пищевода (на 5 мм рт. ст. ниже атмосферного давления). Тоническое давление, создаваемое гладкой циркулярной мышцей НПС, усиливается при сокращении ножек диафрагмы во время вдоха и выдоха и в моменты, когда повышается внутрижелудочное давление, например при чихании, кашле, наклоне туловища [5]. В покое тоническое сокращение НПС поддерживается кроме внутренностного тонуса его мышцы холинергическими возбуждающими нейронами. Краткое расслабление НПС при проглатывании пищи сопровождается перистальтической волной, которая закрывает и очищает просвет пищевода.
Как у здоровых людей, так и при ГЭРБ наблюдается такое явление, как преходящее, транзиторное расслабление НПС [7, 8], которое вызывается чаще всего растяжением стенок желудка при приеме пищи для уменьшения внутрижелудочного давления путем сброса воздуха из газового пузыря желудка (отрыжка воздухом). При этом кроме отрыжки воздухом (часто при расслаблении НПС) возникновение рефлюкса желудочного содержимого объясняется тем, что преходящие расслабления НПС сохраняются в зоне высокого давления так же длительно (около 20 секунд), как и расслабления НПС, инициированные глотанием, но при этом не возникает очищающей просвет пищевода перистальтической волны [9]. У больных ГЭРБ описанные явления отмечаются часто, длительно [10] и являются причиной появления симптомов заболевания (изжоги, отрыжки, срыгивания).
В целом при ГЭРБ описаны три основные ситуации, когда возникает патологический рефлюкс: при преходящем расслаблении НПС, недостаточной функции НПС и вследствие повышенного внутрибрюшного давления.
Причина частого преходящего расслабления НПС при ГЭРБ остается неясной. Вместе с тем все большее число исследователей склоняются к мнению о взаимосвязи патологии запирательного механизма НПС при ГЭРБ с нарушенной моторной активностью желудка, его замедленным опорожнением, приводящим к растяжению стенок органа, или с повышенной чувствительностью к нормальному растяжению желудка, в т. ч. на фоне воспалительного процесса в стенке желудка [11–14]. По мнению Трухманова А.С., с патофизиологической точки зрения ГЭРБ является кислотозависимым заболеванием, развивающимся на фоне первичного нарушения двигательной функции верхних отделов пищеварительного тракта [11]. Более того, ряд авторов утверждают, что нарушение моторной функции желудка может быть важным, если не главным, фактором возникновения и развития ГЭРБ [13, 15–17]. Особое внимание уделяется таким нарушениям моторики желудка и 12-перстной кишки, как желудочные дисритмии, сопровождающиеся замедленной эвакуацией из проксимальных отделов желудка, нарушения антродуоденальной координации и дуодено-гастральный рефлюкс (ДГР) [18–21]. Примечательно, что для антродуоденальной дискоординации характерными симптомами являются изжога, отрыжка кислым, горьким, срыгивание пищи, т. е. характерные симптомы ГЭРБ.
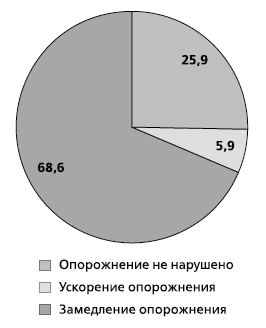
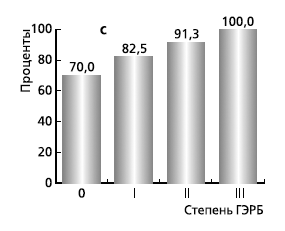
При изучении нами моторной активности желудка и 12-перстной кишки методом динамической гастросцинтиграфии у 204 пациентов с ГЭРБ выявлено значительное преобладание (68,6%) случаев замедленной желудочной эвакуации (рис. 1). Причем при III степени ГЭРБ по классификации Savary–Miller данный тип дисмоторики наблюдался в 100% случаев.
Рис. 1. Частота выявления нарушений эвакуаторной
функции желудка у больных ГЭРБ
(данные динамической гастросцинтиграфики) (%)
Периферическая компьютерная электрогастроэнтерография (ПКЭГЭГ) в 76% случаев выявила изменения по типу функциональной дискоординации моторики желудка и 12-перстной кишки. Причем до приема пищи 23,2% пациентов демонстрировали сниженную электрическую активность желудка при нормальных показателях моторной активности 12-перстной кишки с последующей нормализацией моторики желудка после приема пищи. У 45,8% больных натощак обнаружена повышенная электрическая активность 12-перстной кишки с нормализацией моторной активности после пищевой стимуляции при неизмененных показателях электрической активности желудка, т. е. транзиторная гиперкинезия 12-перстной кишки. В 31% случаев были выявлены пониженные показатели электрической активности 12-перстной кишки натощак, которые нормализовались после пищевой стимуляции с одновременным отсутствием каких-либо изменений электрической активности на частотах желудка. Характерно, что во всех трех случаях, но с разной частотой, наблюдался ДГР, который значительно чаще (93%) регистрировался у пациентов со вторым вариантом дисмоторики.
В целом частота выявления ДГР у всех больных ГЭРБ методом ПКЭГЭГ составила 82,4%, возрастая прямо пропорционально степени тяжести болезни (рис. 2). Это подтверждает данные о том, что с ростом степени тяжести ГЭРБ растет и число смешанных рефлюксов (содержимое желудка + содержимое 12-перстной кишки). Такая закономерность не может не учитываться, т. к. именно смешанные рефлюксы в большом числе случаев приводят к такому грозному осложнению ГЭРБ, как пищевод Барретта (появление в пищеводе цилиндроклеточной метаплазии плоского эпителия с угрозой развития в дальнейшем аденокарциномы).
Рис. 2. Частота выявления ДГР
у пациентов ГЭРБ методом ПКЭГЭГ
Также важную роль в патогенезе ГЭРБ играет нарушение моторики самого пищевода, включающее изменение силы и продолжительности перистальтических сокращений, повышение или снижение тонуса его сфинктеров. В патогенезе ГЭРБ имеют значение ослабление перистальтики пищевода, которое приводит к замедлению его опорожнения и снижению сократительной способности стенок пищевода при рефлюксе; снижение давления НПС; избыточная релаксация и деструктуризация его антирефлюксной функции [2].
Немаловажная роль в возникновении моторных нарушений пищевода и желудка, лежащих в основе развития ГЭРБ, отводится дисбалансу парасимпатического и симпатического звеньев нервной регуляции органов желудочно-кишечного тракта (ЖКТ) и как следствие его – нарушению перистальтической активности. Вегетативная регуляция моторно-эвакуаторной активности органов эзофагогастродуоденальной зоны осуществляется с участием основных рецепторов (холинергических, адренергических, дофаминергических, серотониновых, мотилиновых, холецистокининовых) и важнейших мессенджеров, включая гастроинтестинальные гормоны, стимулирующие (ацетилхолин, мотилин, гастрин, серотонин, инсулин, субстанция Р) и тормозящие, угнетающие моторную активность (дофамин, секретин, холецистокинин, оксид азота, глюкагон, соматостатин, энкефалины, вазоактивный интестинальный пептид). Одним из важнейших мессенджеров, оказывающих угнетающее влияние на гладкомышечные элементы желудка, является дофамин, секретируемый в отдельных участках желудочной стенки и действующий через специализированные, здесь же расположенные дофаминовые рецепторы. Дисбаланс координирующего действия стимуляторов и ингибиторов моторики органов пищеварительного тракта, выражающийся, к примеру, в избыточной дофаминовой активности, приводит к гипомоторной дискинезии пищевода, желудка, 12-перстной кишки вплоть до появления некоординированных сокращений, антордуоденальной дискоординации, функциональному гастро- и дуоденостазу. При этом часто наблюдается параллельное снижение давления в НПС, развиваются недостаточность кардии и патологический гастроэзофагеальный рефлюкс.
Определенное значение в развитии моторных нарушений, лежащих в основе патогенеза ГЭРБ, имеют влияние на моторику некоторых компонентов пищи (жиров, шоколада, цитрусовых, томатов, кофе, алкоголя и др.), а также прием медикаментозных средств (холинолитиков, β-адреноблокаторов, антагонистов кальция и доноров оксида азота – нитратов) и курение.
К органическим причинам, приводящим к развитию ГЭРБ, относят рефлюкс при грыже пищеводного отверстия диафрагмы, связанный с исчезновением угла Гиса – важного анатомического элемента запирательного механизма кардии [2].
Все вышесказанное указывает на то, что нарушение моторной активности верхних отделов ЖКТ в патогенезе ГЭРБ является определяющим фактором, который создает условия для контакта агрессивного содержимого желудка со слизистой оболочкой пищевода, возникновения морфологических изменений и клинических проявлений болезни.
Тактика лечения ГЭРБ
Вместе с тем на сегодняшний день ведущим направлением в лечении ГЭРБ является устранение закисления в пищеводе путем блокады кислотной продукции, осуществляемой обкладочными железами желудка с помощью ингибиторов протонной помпы (ИПП); связывания агрессивных компонентов желудочного содержимого; создания препятствия для контакта последних со слизистой оболочкой пищевода (путем применения антацидов, альгинатов).
Следует сказать, что данный подход к лечению ГЭРБ продиктован, с одной стороны, реальными успехами в купировании не только клинических, но и морфологических проявлений болезни, предотвращением осложнений, а при длительной поддерживающей кислотосупрессивной терапии – и стабилизацией состояния на нормальных показателях закисления пищевода. С другой стороны, до последнего времени в арсенале терапевта, гастроэнтеролога отсутствовали эффективные и безопасные средства для коррекции моторных расстройств у больных ГЭРБ, которые бы позволяли осуществлять достаточно длительный контроль моторики, не вызывая побочных эффектов, свойственных имеющимся на фармакологическом рынке прокинетикам.
В связи с этим на сегодняшний день препаратами выбора в лечении ГЭРБ, эффективно подавляющими кислотную секрецию в желудке, являются ИПП, особенно последнего поколения (пантопразол, рабепразол). При эрозивных формах болезни они становятся обязательным компонентом.
Однако следует иметь в виду, что даже самые эффективные на сегодняшний день ИПП не влияют на первопричину болезни – нарушенную функцию запирательного механизма кардии, моторику желудка и 12-перстной кишки, поэтому после прекращения их приема у большей части больных сравнительно быстро возникает рецидив заболевания. В ряде случаев ИПП не устраняют некоторые симптомы, чаще всего ассоциируемые с нарушением моторики пищевода и желудка, гиперчувствительностью желудка к растяжению. В подобных случаях при лечении больных ГЭРБ дополнительно показано использование прокинетиков.
Разбирая особенности средств, обладающих прокинетическим эффектом на верхние отделы ЖКТ, необходимо отдельно остановиться на следующих препаратах:
Опыт применения перечисленных прокинетиков при ГЭРБ, особенно таких препаратов, как метоклопрамид, домперидон и цизаприд, как в нашей стране, так и за рубежом достаточно велик, однако из-за большого спектра побочных эффектов, вызываемых препаратами прежних поколений, и кратковременности их действия целесообразность применения последних нередко ставилась под сомнение [25, 26].
Ганатон в лечении ГЭРБ
Препаратом нового поколения прокинетиков, хорошо зарекомендовавшим себя (по данным нескольких мета-анализов) при лечении ГЭРБ и функциональной диспепсии, зарегистрированным за рубежом, а с 2007 г. и в России, является итоприда гидрохлорид – Ганатон (от “gastric natural tone” – восстанавливающий нормальный тонус желудка). Это новый препарат с комбинированным механизмом действия, являющийся антагонистом дофаминовых D2-рецепторов и блокатором ацетилхолинестеразы. Итоприда гидрохлорид активизирует высвобождение ацетилхолина, одновременно препятствуя его деградации. Он обладает минимальной способностью проникать через гематоэнцефалический барьер, не влияет на продолжительность интервала Q-T и не взаимодействует с лекарственными средствами, метаболизирующимися ферментами системы цитохрома Р450, в т. ч. ИПП, часто применяемыми в лечении ГЭРБ и функциональной диспепсии. Итоприда гидрохлорид оказывает выраженное противорвотное действие, усиливает пропульсивную моторику желудка и ускоряет его опорожнение.
Открытые клинические исследования итоприда гидрохлорида в США, Японии, Германии, Индии и других странах показали высокую клиническую эффективность препарата у больных функциональной диспепсией, хроническим гастритом, диабетическим гастропарезом и ГЭРБ. Препарат отличает хорошая переносимость и отсутствие значимых побочных эффектов. У пациентов с функциональной диспепсией и диабетическим гастропарезом итоприд эффективно стимулирует сократительную способность желудка, ускоряет его опорожнение, устраняет антродуоденальную дискоординацию [27–29].
При использовании итоприда гидрохлорида в составе комбинированной терапии с ИПП у пациентов с ГЭРБ обнаружено, что данный прокинетик достоверно усиливает сократительную активность НПС, что подтверждается увеличением давления в его области, а также усиливает моторную активность желудка, ускоряет желудочную эвакуацию и нормализует нарушенную гастродуоденальную координацию [30]. Важной положительной стороной использования итоприда при ГЭРБ является не только быстрый и стойкий клинический эффект, но и возможность его длительного применения без развития каких-либо значимых побочных эффектов. Так, Inoue K. и соавт. (1999), применяя итоприд по 50 мг 3 раза в сутки в течение 7 недель у больных хроническим гастритом с явлениями рефлюкс-эзофагита, получили хороший клинический эффект: исчезновение жалоб у 67% пациентов с изжогой в отсутствие побочных эффектов [31].
Имеется и отечественный положительный опыт использования Ганатона для лечения больных ГЭРБ. Так, Минушкин О.Н. и Лощинина Ю.Н. (2008) проводили лечение больных ГЭРБ 0–I стадии рецидивирующего течения препаратом Ганатон (в режиме монотерапии) в стандартной дозе (50 мг 3 раза в сутки) в течение 25 дней. На фоне монотерапии Ганатоном изжога была полностью купирована к концу первой недели у 90% больных, а эпителизация эрозий пищевода после полного курса лечения зарегистрирована у всех пациентов с эрозивной формой ГЭРБ. Зарегистрирована также положительная динамика вегетативного статуса и показателей качества жизни пациентов по шкале SF-36 (Short-Form Health Survey).
Таким образом, с появлением на отечественном рынке эффективного и безопасного прокинетика итоприда гидрохлорида (Ганатона) открываются новые возможности проведения полноценной патогенетической терапии ГЭРБ, включая коррекцию моторных расстройств пищевода, желудка и 12-перстной кишки, восстановление их нормальной миоэлектрической активности и взаимной координации.
Применение Ганатона у больных ГЭРБ возможно как в режиме монотерапии при легких формах болезни, так и в составе комбинированного с ИПП лечения.
По-видимому, с учетом особенностей фармакодинамики и фармакокинетики препарата Ганатон возможно его применение у больных ГЭРБ в режиме длительной противорецидивной терапии и в комбинации с ИПП, и в режиме монотерапии. При этом не исключена коррекция стандартных доз обеих составляющих в сторону уменьшения.
Моторные нарушения пищеварительного тракта: терапия прокинетиками
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Прокинетические препараты (прокинетики) — это лекарственные средства, которые усиливают и координируют мышечные сокращения желудочно-кишечного тракта (ЖКТ), включая координацию между различными сегментами кишечника, тем самым усиливая движение внутрипросветного содержимого. В обзоре рассмотрены современные подходы к применению прокинетиков в лечении моторных нарушений со стороны ЖКТ. Представлены результаты исследований различных классов лекарственных средств, обладающих прокинетическим действием и нацеленных на различные патофизиологические механизмы, включая нарушение антродуоденальной координации, проявляющиеся субъективными симптомами и объективной задержкой опорожнения желудка. Многие из описанных лекарственных средств на сегодняшний день не зарегистрированы в РФ. Использующееся в настоящее время в клинической практике и зарегистрированное в РФ лекарственное средство домперидон по-прежнему сохраняет актуальность: при лечении пациентов с функциональной диспепсией, гастропарезом и гастроэзофагеальной рефлюксной болезнью рекомендуется его прием в комбинации с ингибиторами протонной помпы. Домперидон оказывает противорвотный эффект, обладает благоприятным профилем безопасности при использовании по зарегистрированным показаниям.
Ключевые слова: функциональная диспепсия, гастроэзофагеальная рефлюксная болезнь, гастропарез, прокинетики, задержка опорожнения желудка, антродуоденальная координация, противорвотный эффект.
Для цитирования: Ахмедов В.А. Моторные нарушения пищеварительного тракта: терапия прокинетиками. РМЖ. Медицинское обозрение. 2022;6(5):252-257. DOI: 10.32364/2587-6821-2022-6-5-252-258.
V.A. Akhmedov Omsk State Medical University, Omsk, Russian Federation
Prokinetic agents, or prokinetics, are medications that increase and coordinate muscle contractions in the gastrointestinal (GI) tract, including the coordination between various segments of the intestine, and thereby promote the transport of intraluminal content. This paper reviews the current approaches to the use of prokinetics for GI motor disorders. The author addresses the studies on various classes of drugs with prokinetic action that target different pathological mechanisms (including abnormalities of anthro-duodenal coordination manifesting with subjective symptoms and objective delay in stomach emptying). Meanwhile, to date, many of these medications are not approved in the Russian Federation. Domperidon, a drug that is currently used in routine practice and approved in Russia, still proves to be relevant. In functional dyspepsia, gastroparesis, and gastroesophageal reflux disease, this medication is recommended in combination with proton pump inhibitors. Domperidon provides an antiemetic effect and has a favorable safety profile when used for approved indications.
Keywords: functional dyspepsia, gastroesophageal reflux disease, gastroparesis, prokinetics, delay in stomach emptying, anthro-duodenal coordination, antiemetic effect.
For citation: Akhmedov V.A. Gastrointestinal motor disorders: treatment with prokinetics. Russian Medical Inquiry. 2022;6(5):252–258 (in Russ.). DOI: 10.32364/2587-6821-2022-6-5-252-258.
Введение
Прокинетические препараты (прокинетики) — это лекарственные средства, которые усиливают и координируют мышечные сокращения желудочно-кишечного тракта (ЖКТ), включая координацию между различными сегментами кишечника, тем самым усиливая движение внутрипросветного содержимого [1]. Прокинетики проявляют фармакологическую активность в селективных областях ЖКТ, что определяется расположением рецепторных мишеней для их фармакологического действия.
Виды нарушений моторики желудка
Существуют три преобладающие двигательные дисфункции, которые могут приводить к различным проявлениям или симптомам у пациентов с функциональной диспепсией: задержка опорожнения желудка, дисфункция аккомодации желудка и пилорическая дисфункция. Симптомами, связанными с задержкой опорожнения желудка, являются тошнота, рвота и вздутие в верхней части живота, при этом боль не является типичным симптомом задержки опорожнения желудка [2]. Нарушения аккомодации желудка обычно связаны с постпрандиальным дистресс-синдромом, компонентом функциональной диспепсии. Так, среди пациентов с клиническими симптомами постпрандиального дистресс-синдрома около 25% имеют задержку опорожнения желудка, около 25% — нарушение аккомодации желудка и около 25% — сочетание этих моторных дисфункций [3].
Выявление нарушений опорожнения желудка требует точного теста. В настоящее время существуют три прямых и одно косвенное измерение аккомодации желудка. К трем прямым методам относятся: однофотонная эмиссионная компьютерная томография, измерение проксимального объема желудка с помощью баростата (для чего нагнетается давление воздуха внутри податливого полиэтиленового баллона и поддерживается постоянным с помощью электронного насоса, всасывающего или нагнетающего воздух, а непрерывный мониторинг объема внутри баллона обеспечивает измерение объема желудка) [4], внутрипросветная манометрия с высоким разрешением в проксимальном отделе желудка [5]. Косвенное измерение аккомодации желудка происходит путем приема питательного напитка с постоянной скоростью его поступления до достижения максимально допустимого, этот метод позволяет оценить ощущение в желудке [6]. Применение данного метода также позволяет косвенно оценить аккомодацию желудка, если калорийность напитка составляет менее 750 ккал, поскольку существует линейная корреляция между применением данного метода и объемом аккомодации желудка, измеренным баростатом, при калорийности жидкого питания ниже 750 ккал [6]. Проводились попытки использовать двухмерную визуализацию области проксимального отдела желудка сразу после приема пищи для оценки аккомодации желудка, однако впоследствии было установлено, что эти измерения неточные по сравнению с трехмерным изображением, и поэтому метод 2D-визуализации требует дальнейшей валидации [7].
Была продемонстрирована взаимосвязь между ускорением опорожнения желудка и улучшением симптомов на фоне применения домперидона [2]. Нарушения опорожнения желудка могут быть уменьшены путем воздействия на специфические рецепторы, включая серотонинергические 5-HT4, а также рецепторы дофамина D2/3 и рецепторы нейрокинина 1 (NK1) [8]. Фактически подходы к улучшению постпрандиальной аккомодации были связаны с уменьшением симптомов функциональной диспепсии, например с использованием серотонинергического агониста 5-HT1A буспирона, или с использованием акотиамида — антагониста ацетилхолинэстеразы и антагониста пресинаптических М1 и М2 мускариновых рецепторов [8]. Эти мускариновые рецепторы участвуют в ингибировании высвобождения ацетилхолина. Следовательно, являясь антагонистом этих рецепторов и ингибируя ацетилхолинэстеразу, акотиамид приводит к повышению локального уровня ацетилхолина, который является стимулирующим передатчиком в кишечной нервной системе и парасимпатических нервных путях [9].
Нарушения функции привратника трудно оценить неинвазивно, и на сегодняшний день доступны два подхода, требующие внутрипросветных измерений. Это антропилородуоденальная манометрия и применение устройства Endoflip (эндоскопический функциональный зонд для визуализации просвета желудка). При проведении антропилородуоденальной манометрии используются близко расположенные манометрические датчики для измерения давления и определяется активность привратника по комбинации фазовых и тонических сокращений, а также по комбинации активности антрального и дуоденального фазового давления при манометрическом отслеживании [10].
Устройство Endoflip представляет собой длинный (8 или 16 см) зонд, состоящий из 16 парных электродов для импедансной планиметрии, установленных на катетере и расположенных внутри баллона, который заполнен проводящей жидкостью (баллон обычно раздувается при введении 40–50 мл жидкости); электроды возбуждения на обоих концах баллона генерируют слабый электрический ток. Электроды импеданса измеряют напряжение, по которому устройство вычисляет площади поперечного сечения согласно закону Ома (напряжение сопротивления / ток) на каждом интервале между электродами. Таким образом, измеряя давление одновременно с площадью поперечного сечения, можно рассчитать индекс растяжимости [11].
Прокинетические препараты — новые и хорошо изученные
Несколько агонистов 5-НТ4-рецепторов «нового поколения» являются селективными для 5-HT4-рецепторов без риска побочных эффектов, к ним относятся прукалоприд, велусетраг, наронаприд и фелцисетраг [12] (последние три препарата в РФ не зарегистрированы). Прукалоприд одобрен Европейским агентством по лекарственным средствам (European Medicines Agency, EMA) и Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (U.S. Food and Drug Administration, FDA) для лечения хронических запоров. В рандомизированном плацебо-контролируемом перекрестном исследовании с участием 34 пациентов с моторными расстройствами верхних отделов ЖКТ (28 c идиопатическим, 6 с диабетическим гастропарезом) часть из них получали прукалоприд по 2 мг 1 р/сут, часть — плацебо в течение 4 нед. с 2-недельным отмывочным периодом. Прукалоприд был эффективен в облегчении симптомов, вызванных общим гастропарезом, по индексу кардинальных симптомов субшкалы тошноты/рвоты, сытости / сытости и вздутия живота, при этом также улучшалась общая оценка качества жизни пациентов [13]. Аналогично была показана эффективность велусетрага при лечении пациентов с диабетическим и идиопатическим гастропарезом [14]. Внутривенное введение фелцисетрага сопровождалось значительным ускорением опорожнения желудка, транзита по тонкой кишке и опорожнения толстой кишки по сравнению с использованием плацебо у пациентов с гастропарезом и ранее подтвержденной задержкой опорожнения желудка; при этом препарат хорошо переносился [15]. В рандомизированном исследовании [16] в двух параллельных группах препарат фелцисетраг (TAK-954), вводимый пациентам на искусственной вентиляции легких и с непереносимостью энтерального питания, определяемой как остаточный объем желудка ≥200 мл, привел к увеличению доли пациентов с нормальным опорожнением желудка по сравнению с метоклопрамидом, назначаемым по 10 мг 4 р/сут. Велусетраг и фелцисетраг (TAK-954) не оказывали существенного влияния на тонус коронарных сосудов по данным фармакологических исследований. Кроме того, эти препараты не оказывали негативного влияния на сердечный ритм и функцию тромбоцитов [17]. Фелцисетраг обладает высоким сродством (pKi 9,4) к человеческим рекомбинантным 5-НТ4-рецепторам с более чем 2000-кратной селективностью по отношению к этим рецепторам [18].
Другим потенциальным механизмом усиления нервно-мышечной функции желудка является противовоспалительный эффект, который может способствовать стимуляции блуждающего нерва. Это было продемонстрировано с помощью агониста 5-HT4 прукалоприда, который модифицировал реакцию клеток T2-хелперов и уменьшал интенсивность развившейся послеоперационной кишечной непроходимости [19].
При расстройствах верхних отделов ЖКТ, связанных с повышенной чувствительностью желудка, таких как функциональная диспепсия, дофаминергический антагонист D2/3 тразпиробен (TAK-506) (в РФ не зарегистрирован) принимался в виде питательного напитка в течение 1 нед., что приводило к значительному увеличению объема желудка по сравнению с исходным уровнем [20]. Более того, в плацебо-контролируемом исследовании [21] назначение антагониста рецептора NK1 апрепитанта сопровождалось улучшением клинических симптомов гастропареза, включая тошноту. Данный эффект может отражать известное влияние антагонистов рецепторов NK1 на рвотный центр в стволе головного мозга, сходное с действием, связанным с уменьшением вызванной химиотерапией рвоты. Другой потенциальный механизм симптоматического эффекта может быть связан с увеличением объема желудка натощак и аккомодации без негативного влияния на опорожнение желудка, что было продемонстрировано в исследовании с участием здоровых добровольцев [22]. Как показали результаты рандомизированного контролируемого исследования [23], применение нового антагониста рецептора NK1 — традипитанта (в РФ не зарегистрирован) сопровождалось улучшением симптомов гастропареза в течение 4 нед.
Еще одним перспективным направлением улучшения моторики желудка является применение агонистов рецепторов грелина. Грелин состоит из 28 аминокислот, преимущественно локализуется в желудке, стимулирует аппетит. Введение фармакологической дозы рекомбинантного человеческого грелина повышало тонус проксимального отдела желудка за счет центральных и периферических эффектов [24], а в некоторых исследованиях он также ускорял опорожнение желудка у пациентов с гастропарезом [25]. Синтетический пентапептид, агонист рецептора грелина (RM-131), обладает в 130 раз более мощным действием, чем природный грелин [26, 27]. Агонист рецепторов грелина реламорелин увеличивает частоту дистальных антральных сокращений, не препятствуя аккомодации желудка и не изменяя насыщение после приема пищи у здоровых добровольцев, что отличает его действие от действия макролидного антибиотика эритромицина [28].
Одним из перспективных направлений прокинетической терапии является воздействие на дно желудка. Исследования показали, что применение акотиамида улучшает аккомодацию и опорожнение желудка после приема жидкой пищи [32] и улучшает симптомы у пациентов с функциональной диспепсией [33]. Применение некоторых агонистов рецепторов 5-НТ4, таких как тегасерод (в РФ не зарегистрирован), у пациентов с функциональной диспепсией с нормальным опорожнением желудка также сопровождалось усилением аккомодации желудка [34]. Это служит обоснованием для их применения при функциональной диспепсии. В исследовании с использованием одновременного измерения аккомодации желудка и опорожнения в ответ на употребление в пищу круто сваренных яиц было показано, что у некоторых пациентов нарушение опорожнения может быть результатом чрезмерной аккомодации желудка с задержкой движения твердой пищи от фундального до антрального отдела [35]. Это наблюдение предполагает, что стимуляция проксимального отдела желудка с уменьшенной аккомодацией желудка может фактически усилить опорожнение желудка у пациентов с гастропарезом.
В последние годы все чаще признается, что у пациентов, длительно принимающих опиоидные препараты, может развиться гастропарез [36]. Опиоиды могут вызывать пилорическую дисфункцию в дополнение к угнетению моторной функции антрального отдела, что способствует задержке опорожнения желудка [37]. Поэтому важно оценить, может ли целевое воздействие на привратник или ингибирование действия опиоидов быть терапевтическим подходом к лечению задержки опорожнения желудка, частично обусловленной пилорической дисфункцией. Хотя классический фармакологический подход к лечению нарушения функции привратника при гастропарезе включает инъекции ботулинического токсина (имеется опыт, свидетельствующий о его эффективности, особенно при инъекциях в более высоких дозах) [38], но проведенное плацебо-контролируемое исследование [39] не продемонстрировало эффективности данного метода.
Домперидон — доказанная эффективность и безопасность
В большинстве стран только два препарата одобрены к применению для лечения гастропареза: метоклопрамид и домперидон. Оба лекарственных средства являются антагонистами дофаминовых (D2) рецепторов. Действие эндогенного трасмиттера дофамина заключается в ингибировании высвобождения ацетилхолина, что сопровождается снижением моторики желудка и проксимального отдела тонкой кишки [40]. Эти ингибирующие эффекты эндогенного дофамина устраняются при назначении антагонистов D2-рецепторов. В целом метоклопрамид и домперидон показали сходную эффективность в отношении облегчения симптомов, хотя побочные эффекты со стороны центральной нервной системы чаще наблюдались при применении метоклопрамида [41].
Важно, что домперидон оказывает противорвотный эффект. Рекомендуемая начальная доза домперидона при гастропарезе составляет 10 мг внутривенно и может быть увеличена (при необходимости) до 20 мг внутривенно перед сном. В недавно проведенном в Японии исследовании применение домперидона оказалось безопасным в I триместре беременности, не вызвав повышенного риска общих серьезных врожденных пороков развития у плода [42]. Безопасность домперидона в отношении развития тяжелых желудочковых аритмий была подтверждена в недавно проведенном исследовании [43], в котором применение препарата не увеличивало риск развития нарушений ритма и было таким же безопасным, как применение итоприда и мозаприда (в РФ не зарегистрирован). Систематический обзор 28 исследований показал уменьшение симптомов у 64%, уменьшение случаев госпитализации у 67% и ускорение опорожнения желудка у 60% пациентов с диабетическим гастропарезом, при этом риск побочных эффектов со стороны центральной нервной системы был намного ниже, чем при применении метоклопрамида, поскольку домперидон не проникает через гематоэнцефалический барьер [44]. Безопасное применение домперидона в качестве препарата, купирующего рвоту, было описано еще в 1977 г. у 27 пациентов с развившейся послеоперационной тошнотой и рвотой [45]. В клинической практике рекомендуемая доза домперидона составляет от 10 мг 3 р/сут и перед сном (последний прием) [44]. Рекомендуется избегать его применения только тем пациентам, скорректированный интервал QTc у которых на электрокардиограмме составляет >470 мс для мужчин и >450 мс для женщин [46].
В проведенном исследовании было показано, что ночной дуоденогастральный рефлюкс желчи и рН желудка у пациентов с функциональной диспепсией значительно уменьшались после лечения домперидоном (p=0,015, p=0,021) [47]. Оценка тяжести ночных диспепсических симптомов также была значительно снижена после лечения домперидоном (p=0,010, p=0,015, p=0,026), что положительно коррелировало со снижением ночного рефлюкса желчи или рН желудка (r=0,736, r=0,784, r=0,753 или r=0,679, r=0,715, r=0,697, p=0,039, p=0,036, p=0,037 или p=0,043, p=0,039, p=0,040) [47]. Следовательно, при возникновении у пациентов с функциональной диспепсией ночных диспепсических симптомов, которые могут быть связаны с чрезмерным ночным дуоденогастральным рефлюксом желчи, терапия домперидоном может облегчить эти симптомы.
Аналогичный позитивный эффект был получен при включении домперидона в терапию пациентов с хроническим поверхностным гастритом. В качестве объектов исследования были отобраны 96 пациентов с хроническим поверхностным гастритом, которые были разделены на контрольную группу (n=48) и тестовую группу (n=48) с использованием двойного слепого метода [48]. Пациенты в контрольной группе получали омепразол, в то время как пациенты в тестовой группе получали домперидон в комбинации с омепразолом. Наблюдались и анализировались клинические эффекты в обеих группах. После лечения улучшение показателей в тестовой группе, где дополнительно назначался домперидон, было выше, чем в контрольной группе (р ® ) в качестве противорвотного средства сохраняет свою актуальность. В проведенном в 2019 г. исследовании [49] при опросе оказалось, что около 45% опрошенных итальянских врачей назначали профилактические противорвотные средства в начале лечения опиоидами. Наиболее часто назначались для этой цели прокинетики, такие как метоклопрамид и домперидон (84%), за ними следовали антагонисты 5-НТ3-рецепторов (8%), нейролептики (6%) и кортикостероиды (2%). В проведенном исследовании [50] по оценке безопасности домперидона при лечении тошноты и рвоты, связанной с инфузией дигидроэрготамина у пациентов с мигренью, было проанализировано 103 последовательные госпитализации 90 пациентов, поступивших для внутривенного введения дигидроэрготамина. Большинство пациентов были направлены на лечение хронической мигрени с аурой (n=53), остальные — на лечение мигрени без ауры (n=46). Домперидон вводился в 85 из 103 случаев и хорошо переносился в дозах до 80 мг/сут. Значительный побочный эффект в виде акатизии наблюдался лишь у одного пациента. Исходная ЭКГ со скорректированным интервалом QT (QTc) была получена у всех пациентов. Повторная ЭКГ после домперидона проведена у 21 пациента, исходные характеристики которых не отличались от группы в целом. Интервал QTc не различался до и после введения домперидона. Таким образом, домперидон оказался безопасным при лечении тошноты, связанной с инфузией дигидроэрготамина в стационаре.
На рынке РФ зарегистрировано около 20 различных торговых наименований лекарственных средств с международным непатентованным наименованием действующего вещества «домперидон». Особого внимания заслуживают отечественные дженерики, так как обычно они имеют преимущество по цене, например препарат Мотилорус®, производимый в Самарской области. Мотилорус® выпускается в лекарственной форме диспергируемых таблеток, обладает мятным вкусом и соответствует всем необходимым требованиям по качеству.
В недавно вышедших рекомендациях по ведению пациентов с функциональной диспепсией, основанных на доказательной медицине, в качестве терапии второй линии рекомендуется применение прокинетических препаратов, в частности антагонистов дофаминовых рецепторов (уровень доказательств B) и агонистов 5-НТ4-рецепторов (уровень доказательств B) [51]. Что касается обновленных рекомендаций по диагностике и лечению рефрактерной гастроэзофагеальной рефлюксной болезни (ГЭРБ), то добавление прокинетиков в схему лечения пациентов не позволяло достигать лучшего контроля за симптомами заболевания, однако способствовало улучшению показателей качества жизни [52]. В недавно проведенном метаанализе [53] публикаций, включающих рандомизированные контролируемые исследования по сравнению комбинированного применения ингибиторов протонной помпы (ИПП) плюс прокинетик с монотерапией ИПП в отношении общего улучшения симптомов ГЭРБ, проводился анализ 16 исследований с участием 1446 пациентов (719 в группе ИПП плюс прокинетик и 727 в группе монотерапии ИПП). По результатам данного исследования показано, что лечение пациентов с ГЭРБ с применением ИПП плюс прокинетик приводило к значительному уменьшению симптомов ГЭРБ независимо от типа прокинетика, рефрактерности и этнической принадлежности пациентов. Кроме того, было обнаружено, что лечение пациентов с применением ИПП плюс прокинетик в течение не менее чем 4 нед. было эффективнее по сравнению с монотерапией ИПП в отношении общего показателя улучшения симптомов, при этом нежелательные явления, наблюдаемые в ответ на лечение комбинацией ИПП плюс прокинетик, не отличались от тех, которые наблюдались при монотерапии ИПП [53].
Заключение
В настоящее время проведены обширные исследования по изучению воздействия различных классов лекарств, обладающих прокинетическим действием, нацеленных на различные патофизиологические механизмы, включая нарушение антродуоденальной координации, проявляющиеся субъективными симптомами и объективной задержкой опорожнения желудка. Полученные результаты открывают хорошие перспективы для разработки эффективных методов лечения функциональной диспепсии и гастропареза. Использующийся на сегодняшний день в клинической практике препарат домперидон (например, препарат Мотилорус ®) по-прежнему сохраняет актуальность: при лечении пациентов с функциональной диспепсией, гастропарезом и ГЭРБ рекомендуется его прием в комбинации с ИПП.
Сведения об авторе:
Ахмедов Вадим Адильевич — д.м.н., профессор, заведующий кафедрой медицинской реабилитации ДПО ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-7603-6093.
Контактная информация: Ахмедов Вадим Адильевич, e-mail: v_akhmedov@mail.ru.
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 04.04.2022.
Поступила после рецензирования 27.04.2022.
Принята в печать 26.05.2022.
About the author:
Vadim A. Akhmedov — Dr. Sc. (Med.), Professor, Head of the Department of Medical Rehabilitation, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-7603-6093. Contact information: Vadim A. Akhmedov, e-mail: v_akhmedov@mail.ru.
Financial Disclosure: author has no financial or property interest in any material or method mentioned.
Сегодня и завтра прокинетиков
Аркадий Александрович Шептулин, профессор, доктор медицинских наук:
– Мы переходим к следующему докладу. Я коснусь вопроса, связанного с применением прокинетиков. Я начну с того, что потребность в применении прокинетиков очень велика, и связано это с широким распространением заболеваний, при которых отмечается нарушение двигательной функции желудка. Эти заболевания можно разделить на две группы. Прежде всего, это заболевания с первичным нарушением двигательной функции желудка – там, где эти нарушения лежат в основе развития заболевания. К ним относится, в частности, гастроэзофагеальная рефлюксная болезнь. Мы традиционно считаем, что это кислотозависимое заболевание, что соляная кислота является конечным виновником воспаления слизистой оболочки пищевода. Но три патогенетических фактора из четырех обусловлены нарушением моторики: это снижение тонуса нижнего пищеводного сфинктера и, как следствие, увеличение числа спонтанных расслаблений нижнего пищеводного сфинктера и увеличение числа эпизодов гастроэзофагеального рефлюкса. Это повышение внутрижелудочного давления, чаще всего обусловленное нарушением эвакуаторной функции желудка, что тоже провоцирует рефлюкс, и это нарушение пищеводного клиренса, нарушение способности пищевода быстро удалять обратно попавшее в него содержимое. Все эти три фактора в конечном счете способствуют удлинению времени контакта слизистой оболочки пищевода с соляной кислотой.
К заболеваниям с первичным нарушением двигательной функции желудка относятся функциональная диспепсия, в частности, ее дискинетический вариант, то есть вариант, который сопровождается возникновением ощущения тяжести и переполнения в подложечной области после еды, и раннее насыщение также обусловлено нарушением, замедлением моторики желудка.
Ну и, наконец, такое очень сложное заболевание, как идиопатический гастропарез, по последним данным это даже не столько гастроэнтерологическое, сколько психиатрическое заболевание. Но тем не менее конечным проявлением его является нарушение эвакуаторной функции желудка.
Ну и, наконец, вы видите, очень многочисленной является группа заболеваний с вторичным нарушением двигательной функции желудка. В частности, это диабетический гастропарез. Наверное, около 60% больных сахарным диабетом – в конце концов, из-за явления диабетической нейропатии желудочно-кишечного тракта у них замедляется опорожнение желудка, хотя клинически нарушения эвакуаторной функции проявляются далеко не всегда. Это поражение желудка при системных заболеваниях: при системной склеродермии и при дерматомиозите, когда изменяется структура стенки желудка, идет замещение мышечных волокон соединительной тканью. Это язвенная болезнь, это постваготомические расстройства, которые возникают и проявляются нарушением эвакуаторной функции желудка после пересечения веточек блуждающего нерва. Это амилоидоз с поражением желудка. Ну и это снижение функции щитовидной железы. Таким образом, это подтверждает, насколько большая потребность в препаратах, которые нормализуют, усиливают тонус, усиливают перистальтику желудка.
У нас достаточно много классов прокинетиков, то есть препаратов, усиливающих моторику желудочно-кишечного тракта, но далеко не все они применяются в реальной клинической практике. В любом учебнике по фармакологии, я помню, 40 лет назад эти препараты – Карбахолин, Физостигмин, Прозерин – я спрашиваю сейчас своих студентов третьего курса, и сейчас они остались в учебниках фармакологии. Но в реальной жизни ни Карбахолин, ни Физостигмин, и очень редко – Прозерин (только в хирургической практике), не применяются из-за системности холинергического действия.
Агонисты мотилиновых рецепторов – это интересные препараты. В частности, все антибиотики-макролиды, особенно Эритромицин, оказывают очень сильное стимулирующее действие на моторику желудка. Насколько оно сильное? Я могу такой клинический пример привести: у нас находилась девушка с инфекционным эндокардитом, мы ее готовили для перевода в институт Бакулева для хирургического лечения, но пока ждали место для перевода, проводили ей курс антибиотикотерапии. И вот, я уже не помню на каком антибиотике, мы получили нейтропенический эффект: упало содержание лейкоцитов. И мы советовались с гематологами, на какой антибиотик лучше перейти. Они посоветовали нам Эритромицин, и мы стали вводить девушке Эритромицин капельно. И после первой же капельницы с Эритромицином возникли сильнейшие боли в подложечной области: настолько сильные, что мы даже испугались, нет ли прободения язвы, повели больную на рентген, делали рентгеноскопию, нет ли свободного газа. К счастью, ничего не было, это был стимулирующий эффект Эритромицина на моторику желудка. В настоящее время Эритромицин редко применяется, только в виде коротких курсов для борьбы с послеоперационным парезом желудка и кишечника. Для длительного применения он не годится с учетом его антибактериального эффекта.
Препараты этой же группы – алемцинал, митемцинал, атилмотин, грелин, которые не обладают антибактериальным эффектом, но и их прокинетическое действие оказывается также слабее.
Еще одна группа – это агонисты опиоидных рецепторов. Известны чистые агонисты μ-опиоидных рецепторов. В частности, в литературе описан такой препарат как Алвимопан, который эффективен у больных с парезом кишечника и применяется иногда хирургами и гинекологами после операций гистерэктомии и колэктомии. Препарат, который широко применяется в нашей стране – это Тримебутин, он обладает очень интересным механизмом действия. Одновременно являясь агонистом μ- и κ-опиоидных рецепторов, он может влиять и как прокинетик за счет влияния на μ-опиоидные рецепторы, и в то же время он может действовать как спазмолитик за счет влияния на κ-опиоидные рецепторы. Он эффективен при послеоперационном парезе кишечника, а также может применяться при СРК, вариант с преобладанием боли и запоров.
Очень большие надежды возлагались на агонистов 5-HT4-серотониновых рецепторов. Это Цизаприд, Тегасерод и Прукалоприд, о котором говорила в своей лекции Елена Александровна. Врачи со стажем помнят, что у нас в конце девяностых годов был такой препарат как Координакс – это аналог Цизаприда. Он показал очень высокую эффективность при лечении СРК с запорами, при лечении функциональной диспепсии, но за счет серьезных побочных эффектов (удлинение интервала Q-T), он еще в 2000 году был изъят из обращения, хотя в любых статьях, в любых обзорах он по-прежнему фигурирует как прокинетик.
Нишу после исчезновения Цизаприда занял Тгасерод. Мета-анализ результатов применения более чем у 9000 больных показал его высокую эффективность в лечении СРК (особенно у женщин). Были хорошие результаты его применения при синдроме функциональной диспепсии. В нашей стране этот препарат не был зарегистрирован, хотя фирма Novartis имела этот препарат под названием Зелмак. Мы всегда, когда с ними встречались, с сотрудниками, спрашивали: «Когда же, когда же Тегасерод появится на нашем рынке?» Нам уклончиво отвечали, что вопрос изучается. Мы для себя объясняли это высокой стоимостью: один день лечения Тегасеродом стоит порядка 4 евро, это значит 160 рублей. Мы думали, что вряд ли фирма просто идет на регистрацию такого дорогого препарата. Ну, как говорится, все что не делается, все к лучшему, потому что в 2007 году FDA, организация в Соединенных Штатах, ответственная за контроль над продуктами питания и лекарственными препаратами, обнародовала данные сравнения применения Тегасерода очень большой группой больных и сопоставила с контрольной группой. Оказалось, что частота сердечно-сосудистых осложнений, при том что в абсолютном исчислении она, вы видите, была невысокой, но она в 11 раз превышала таковую в контрольной группе. И в 2007 году этот препарат тоже был изъят из обращения.
Прукалоприд, о котором говорила Елена Александровна. В настоящее время, вы видите, опубликованы мета-анализы двойных слепых исследований (более 5000 больных), которые свидетельствовали об эффективности и безопасности применения прукалоприда, и он разрешен в Европе, одобрен в Европе для лечения хронических запоров у женщин, у которых слабительные оказываются недостаточно эффективными.
Еще одна группа препаратов, которая, пожалуй, наиболее широкое применение нашла в нашей стране – это антагонисты допаминовых рецепторов. Они разделяются на препараты с центральным и периферическим механизмом действия одновременным. Это Метоклопрамид или Церукал, чаще всего в нашей стране применяется. И антагонисты допаминовых рецепторов с преимущественно периферическим действием, это Домперидон или аналог, наиболее известный в России – это Мотилиум. Вообще Метоклопрамид – один из наиболее старых прокинетиков, ему даже был в Соединенных Штатах Америки присвоен титул «рабочая лошадка прокинетиков», потому что очень большой опыт его применения. Но вы видите, насколько серьезны и насколько часто возникают побочные эффекты. Это прежде всего гормональный эффект – наши коллеги гинекологи шутят: «Мы очень любим ваш Церукал. Мы его даем беременным 2 раза: сначала в ранний триместр для борьбы с явлением токсикоза, а потом после родов для стимуляции лактации». Но еще более серьезным являются экстрапирамидные нарушения, возникновение судорог, мышечного гипертонуса и других двигательных нарушений. Наконец, просто когда мы стали применять, апробировали в семидесятых годах, я помню, когда только появился Метоклопрамид, он вызывал у больных какое-то немотивированное ощущение внутреннего беспокойства. Больные начинали ходить бесцельно. Поэтому надо быть очень осторожными все-таки с применением этого препарата, хотя он, конечно, остался в клинической практике.
Заслуживает внимание применение препарата с комбинированным механизмом действия, это ингибитор допаминовых рецепторов и ингибитор ацетилхолинэстеразы. Это такой препарат как Итоприда гидрохлорид, и в частности его аналог, который появился в нашей стране – это Итомед. Итоприда гидрохлорид усиливает пропульсивную моторику желудка, ускоряет эвакуацию из желудка, препарат обладает противорвотным действием и не влияет на уровень сывороточного гастрина и, соответственно, не влияет на кислотность. Итоприд не проникает через гематоэнцефалический барьер, он метаболизируется флавин-зависимой монооксигеназой и не взаимодействует с системой цитохрома Р450 – это очень важно при одновременном приеме препаратов, которые могут конкурировать за коферментную систему.
Вот показания к применению Итоприда. Это функциональная диспепсия – в нашей стране диагноз «функциональная диспепсия» ставится не так часто, основной диагноз в таких случаях, который мы ставим – это гастрит с симптомами диспепсии. Вообще, всего две страны в мире, которые ставят клинический диагноз хронического гастрита – это Россия и Япония. Понятно, почему Япония не ставит диагноз «функциональная диспепсия», а ставит диагноз гастрита – в Японии самая высокая частота рака желудка и там не могут как бы вычеркнуть гастрит из списка клинических диагнозов, но обязательно, если есть клинические симптомы, там добавляют тот или иной вариант диспепсии. Интересно, когда я буквально несколько дней назад просматривал одну из последних работ по применению прокинетиков японскую, там формулировка диагноза была буквально следующей, дословно цитирую: «клинически манифестная форма хронического гастрита, соответствующая римским критериям функциональной диспепсии». Вот такая вот сложная абракадабра была. Японцы упорно, как и мы в России, держатся за клинический диагноз «хронический гастрит», хотя включают туда функциональную диспепсию, потому что гастрит – это морфологический диагноз и определяет риск развития у больного рака желудка, а функциональная диспепсия показывает, какими лекарственными препаратами мы можем снять у больного те или иные клинические симптомы. Это диабетический гастропарез, о котором я говорил и который встречается достаточно часто при сахарном диабете, и это гастроэзофагеальная рефлюксная болезнь, которая тоже относится к заболеваниям, связанным с нарушением моторики.
Было проведено одно очень красивое исследование применения Итоприда гидрохлорида при функциональной диспепсии. Почему оно так привлекло внимание? Во-первых, очень большое количество больных, 554 человека, в проведении исследования участвовало 78 врачей, исследование проводилось под эгидой университетского госпиталя города Эссена. Это исследование курировали, то есть руководили им, два, наверное, самых видных специалиста по функциональной диспепсии – это Ник Тэлли (N. Talley) из Автстралии и Джерард Хольтманн (G. Holtmann) из Германии. Итоприд назначался в течение 8 недель, причем в трех различных дозах – 50 миллиграмм три раза в сутки, 100 миллиграмм и 200 миллиграмм три раза в сутки. И вы видите, во всех трех группах частота купирования диспепсических расстройств была достоверно выше, чем применение плацебо. И вывод, который был сделан в этом исследовании – применение Итоприда при функциональной диспепсии или, пользуясь нашим языком, при хроническом гастрите с клиническими симптомами, оправдано.
Пожалуй, набольший опыт применения Итоприда гидрохлорида в Японии. И серия больших исследований, которая была проведена в Японии, показала, что эффективность курсового применения Итоприда при лечении хронического гастрита с симптомами диспепсии достигает почти 80%. Вот буквально недавно я раскопал результаты мета-анализа, они были в прошлом году опубликованы, результаты мета-анализа эффективности применения Итоприда, это World Journal of Gastroenterology. Этот мета-анализ включал в себя 9 рандомизированных контролированных исследований более 2600 больных с функциональной диспепсией, 1200 больных, которые получали плацебо или другие прокинетические препараты. Этот мета-анализ показал, что Итоприд обладает достоверно большей эффективностью в отношении улучшения общего состояния, уменьшения чувства тяжести после еды, раннего насыщения, и частота побочных эффектов оказалась абсолютно одинаковой в обеих группах. Здесь видно – первые три значка обозначают большую эффективность Итоприда. Только боль в эпигастрии – здесь различий между Итопридом и плацебо не было. Это понятно, потому что боль при функциональной диспепсии обусловлена в основном кислотно-пептическим фактором, а не нарушениями эвакуаторной функции желудка, поэтому, естественно, не влияя уровень секреции, Итоприд не влияет и на динамику боли.
Есть работы по применению Итоприда при гастроэзофагеальной рефлюксной болезни. В частности, было показано, что применение стандартной дозы (50 миллиграмм 3 раза в сутки в течение 8 недель) приводило к улучшению клинической картины, к исчезновению изжоги у значительного числа больных и к улучшению эндоскопической картины. Кроме того, за счет снижения эпизодов рефлюкса Итоприд в итоге не только способствовал клиническому улучшению, но и уменьшал продолжительность времени снижения рН в пищеводе.
В нашей стране Олег Николаевич Минушкин применял Итоприд в течение длительного времени, 4-8 недель, и в качестве курсового лечения, и в качестве поддерживающей терапии в течение 6-9 месяцев, и тоже получил хороший эффект.
Ян Так (J. Tack) – это, наверное, лидер западноевропейской гастроэнтерологии в области изучения препаратов, влияющих на моторику, дал нам обоснование для применения Итоприда при гастроэзофагеальной рефлюксной болезни. Он провел двойное слепое плацебо-контролируемое исследование у здоровых добровольцев по влиянию Итоприда гидрохлорида на эпизоды спонтанного расслабления нижнего пищеводного сфинктера – важного патогенетического фактора ГЭРБ и показал, что Итоприд гидрохлорид предупреждает возникновение эпизодов этих спонтанных расслаблений. Это может служить объяснением его высокого эффекта при лечении ГЭРБ.
Если говорить о побочных эффектах, то вы видите, они не выражены – диарея, головная боль, все это меньше 1%. Поскольку все-таки там содержится антагонист допаминовых рецепторов, гиперпролактинемия возможна, но вы видите – она возникает у 3 из 1000 человек и, как правило, клинического значения не имеет. И, что очень важно, что результаты применения Итоприда более чем у 10 миллионов больных не выявили ни одного случая удлинения интервала Q-T.
Я здесь хотел высказать мнение двух ведущих ученых о перспективах применения Итоприда. Гастроэнтеролог Джерард Хольтман (G. Holtmann) из Германии, это его вывод на основании собственного большого опыта: «Итоприда гидрохлорид выгодно отличается от остальных прокинетиков, с одной стороны, наличием двойного механизма прокинетического действия, с другой стороны, отсутствием серьезных побочных эффектов, характерных для других прокинетиков. Это дает основание рассматривать его как препарат выбора в лечении двигательных нарушений желудка». И Ян Так (J. Tack), это был специальный симпозиум по функциональной диспепсии в Монреале в ходе Всемирного конгресса гастроэнтерологов, он выступал с докладом по этому препарату и тоже сделал вывод, что «Итоприда гидрохлорид – это высокоэффективный и безопасный представитель нового класса прокинетиков, который в будущем, возможно, займет важное место в лечении других гастроэнтерологических заболеваний, протекающих с нарушением двигательной функции желудка».
Какие же возможности есть и еще в будущем могут появиться для применения Итоприда? Это гипомоторная дискинезия желчевыводящих путей, поскольку показаны возможности прокинетического влияния на двигательную функцию желчного пузыря. Это нарушение двигательной функции кишечника, функциональные запоры, диабетическая нейропатия, потому что есть экспериментальные данные о стимулирующем влиянии Итоприда на моторику кишечника.
Если говорить в перспективе о новых прокинетиках, то здесь пока большого продвижения нет. Есть агонист гамма-амино-оксимасляной кислоты рецепторов, это Баклофен. Я встречаю в журналах и в докладах этот препарат, наверное, на протяжении 7-8 лет. Да, и уже есть мета-анализ пяти рандомизированных контролируемых исследований, он уменьшает число спонтанных расслаблений нижнего пищеводного сфинктера. Но, во-первых, клинический эффект Баклофена при ГЭРБ не был доказан. И, кроме того, вряд ли этот препарат имеет серьезное будущее, потому что основное его показание – это лечение панических атак. И я думаю, что нам нет смысла препараты с таким сильным психотропным действием применять при лечении гастроэзофагеальной рефлюксной болезни.
Два новых препарата – Арбаклофен и лезагаберан – они пока еще тоже находятся в стадии клинических исследований. Еще препарат, очень сложно его название, так называемый негативный аллостерический модулятор метаботропного рецептора глутамата-5. Он даже еще не имеет названия, он имеет пока только численную аббревиатуру. Проведены первые плацебо-контролируемые исследования, которые подтвердили фармакодинамический эффект этого препарата, но пока еще он тоже не прошел все необходимые стадии.
Возможно, когда я готовился к лекции, просматривал, я не вставил сюда, потому что мы заранее подавали презентацию, еще один препарат, который вызывает интерес как прокинетик. Он буквально последние годы появился в докладах, на страницах журналов. Это Акатиамид – это препарат, который влияет на мускариновые рецепторы и препятствует распаду ацетилхолина, за счет этого оказывает стимулирующий эффект, в частности, при функциональной диспепсии. Если я не ошибаюсь, сейчас одновременно в трех странах проводится третья фаза клинических исследований по применению Акатиамида – это в Соединенных Штатах, в Европе и в Японии, по применению его при функциональной диспепсии, вариант с замедленной моторикой. И исследования дают положительные результаты, но все равно пройдет еще несколько лет, наверное, пока он будет официально зарегистрирован.
Таким образом, в заключение я могу еще раз сказать, что заболевания с первичным или вторичным нарушением двигательной функции желудка встречаются часто; что многие препараты, применявшиеся раньше и применяемые сейчас для их лечения (Цизаприд, Метоклопрамид), обладают серьезными побочными эффектами; и в настоящее время наиболее перспективным, наверное, следует считать применение достаточно эффективного и безопасного препарата с двойным механизмом действия – Итоприда гидрохлорида.
Место и выбор прокинетика при лечении гастроэзофагеальной рефлюксной болезни
В.И. Касьяненко, д.м.н., ведущий научный сотрудник, ЦНИИ гастроэнтерологии, Москва
В статье обосновано применение прокинетика при лечении гастроэзофагеальной рефлюксной болезни, особенность и преимущество итоприда (Ганатона) перед ранее известными препаратами этой группы.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, прокинетик, итоприд (Ганатон), механизм действия, преимущество
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) является заболеванием, обусловленным нарушением перистальтики органов эзофагогастродуоденальной зоны, часто повторяющимися забросами в пищевод желудочного или дуоденального содержимого, удлинением времени экспозиции рефлюктата в пищеводе, приводящих к повреждению дистальной части пищевода [1]. Актуальность проблемы. Интерес к ГЭРБ определяется ее высокой распространенностью и ростом заболеваемости, в ряде случаев развитием тяжелых осложнений (стриктура пищевода, кровотечение из язв пищевода, пищевод Барретта, аденокарцинома и др.), а также ухудшением самочувствия больного, снижением его качества жизни [2, 3].
По данным зарубежных статистических исследований, распространенность ГЭРБ среди взрослого населения составляет от 40 до 50% [4].
По данным российских авторов, распространенность ГЭРБ (наличие изжоги и/или кислой отрыжки 1 раз в неделю и чаще на протяжении последних 12 месяцев) составляет 40–60%, причем у 45–80% лиц с ГЭРБ обнаруживается эзофагит [5].
Прокинетики: настоящее и будущее
Поиск средств, нормализующих моторно-эвакуаторную деятельность пищеварительного тракта, привлекает внимание врачей-исследователей на протяжении нескольких столетий. Вероятно, одним из первых представителей этой группы является имбирь, издревле применяемый
Поиск средств, нормализующих моторно-эвакуаторную деятельность пищеварительного тракта, привлекает внимание врачей-исследователей на протяжении нескольких столетий. Вероятно, одним из первых представителей этой группы является имбирь, издревле применяемый в традиционной китайской медицине [1] как средство, устраняющее тяжесть в животе и тошноту, обладающий слабой антагонистической активностью в отношении 5-HT3-рецепторов [2]. К настоящему времени средства, воздействующие на моторную активность пищеварительного тракта и препятствующие антиперистальтическим сокращениям гладкой мускулатуры, объединены в группу прокинетиков [3].
Прежде всего, необходимо очертить круг показаний, по поводу которых получены доказательства в эффективности применения прокинетиков.
Во-первых, заболевания пищеварительного тракта, в развитии которых существенную роль играют нарушения моторной активности пищеварительного тракта (гастроэзофагеальная рефлюксная болезнь, постпрандиальный дистресс-синдром как вариант функциональной диспепсии, язвенная болезнь с нарушением антродуоденальной координации, идиопатический гастропарез, функциональная тошнота, функциональный запор, а также синдром раздраженного кишечника — вариант с запором).
Во-вторых, применение прокинетиков в качестве противорвотных средств (например, при тошноте и рвоте, ассоциированных с приемом цитостатиков) [4].
В-третьих, диабетический гастропарез, при котором замедленное опорожнение желудка влияет на вариабельность всасывания глюкозы, что обусловливает трудности контроля гликемии и может привести к хронизации симптомов гастропареза и низкому гликемическому контролю. Сюда же следует отнести и назначение прокинетиков при гастропарезе другой этиологии [5].
Какие же препараты обладают прокинетической активностью?
Домперидон по своей химической структуре также относится к производным бензимидазола, является высокоселективным блокатором периферических допаминовых рецепторов (D) 2-го типа и в отличие от метоклопрамида лишен многих побочных эффектов ввиду отсутствия проникновения препарата через гематоэнцефалический барьер [6]. Подавляя влияние дофамина, домперидон увеличивает спонтанную активность желудка, увеличивает давление нижнего пищеводного сфинктера и активирует перистальтику пищевода и антрального отдела желудка. Препарат также усиливает частоту, амплитуду и продолжительность сокращений двенадцатиперстной кишки и уменьшает время пассажа пищевых масс по тонкой кишке.
Метоклопрамид. Метоклопрамид по своей химической структуре относится к подтипу бензамидов с несколькими прокинетическими механизмами (рис.): агонизм 5-гидрокситриптамин (НТ) 4-рецепторам, антагонизм по отношению к центральным и периферическим допамин (D) рецепторам 2-го типа, а также прямая стимуляция сокращений гладкой мускулатуры пищеварительной трубки [7].
Прокинетический эффект метоклопрамида ограничен верхними отделами пищеварительного тракта, он повышает тонус нижнего пищеводного сфинктера, усиливает моторику желудка и тонкой кишки, ускоряет опорожнение желудка, улучшает антродуоденальную координацию. Однако, наряду с доказанной эффективностью, назначение метоклопрамида ограничено развитием побочных эффектов [8] (около 30%), а именно экстрапирамидными расстройствами, головной болью, головокружением, сонливостью, депрессией и гормональными нарушениями: гиперпролактинемией с галактореей, гинекомастией, нарушениями менструального цикла.
Метоклопрамид и домперидон оказывают противорвотный эффект, который обусловлен подавлением активности хеморецепторных триггерных зон, расположенных на дне четвертого желудочка вне пределов гематоэнцефалического барьера. Однако способность действовать на аденогипофиз, также лишенный гематоэнцефалического барьера, способствует при длительном применении домперидона у части пациентов повышению уровня пролактина в сыворотке крови, приводящему к развитию гинекомастии, галактореи и аменореи. Следует подчеркнуть, что это нежелательное явление становится клинически значимым лишь при длительном применении препарата (например, если домперидон назначается у больных болезнью Паркинсона). Так, при применении домперидона в суточной дозе 80 мг (в течение 12 лет) частота нежелательных явлений не отличается от плацебо, при этом препарат переносится лучше, чем метоклопрамид в дозе 40 мг/сут [9]. Домперидон широко применяется в клинической практике как эффективный и безопасный прокинетик. Даже в странах с жесткими требованиями к отпуску безрецептурных средств этот препарат обычно продается без рецепта, например, в Германии он доступен при условии, что общая доза домперидона в упаковке не превышает 200 мг.
Итоприда гидрохлорид является одновременно антагонистом допаминовых рецепторов и блокатором ацетилхолинэстеразы. Препарат активирует освобождение ацетилхолина и препятствует его деградации, обладает минимальной способностью проникать через гематоэнцефалический барьер в центральную нервную систему, включая головной и спинной мозг. Метаболизм препарата позволяет избежать нежелательного лекарственного взаимодействия при приеме лекарственных препаратов, метаболизирующихся ферментами системы цитохрома Р450. Как показали экспериментальные и клинические исследования [10, 11], итоприда гидрохлорид усиливает пропульсивную моторику желудка и ускоряет его опорожнение. Кроме того, препарат оказывает противорвотный эффект, которой реализуется благодаря взаимодействию с D2-дофаминовыми хеморецепторами триггерной зоны.
Цизаприд — агонист 5-HT4-рецепторов с незначительной антагонистической активностью в отношении рецепторов 5-HT3, был отозван с рынка США в 2000 году в связи с многочисленными сообщениями о внезапной смерти (удлинение интервала Q-T, опасные желудочковые аритмии) [12]. В последующем были созданы препараты с аналогичным прокинетическим механизмом. Так, еще один агонист 5-HT4-рецепторов мозаприд продемонстрировал влияние на ускорение опорожнения желудка в исследованиях с участием здоровых добровольцев, а также в случаях диабетического гастропареза. В отличие от цизаприда, мозаприд оказывает незначительное влияние на активность каналов калия [13], в связи с чем имеет существенно меньший риск в отношении нарушений сердечного ритма. Прокинетическая активность другого препарата этой подгруппы — рензаприда обусловлена двумя механизмами: агонизмом с рецепторами 5-HT4 и антагонизмом по отношению к 5-HT3-рецепторам. К настоящему моменту уровень доказанности данных по эффективности и безопасности мозаприда и рензаприда не определен за недостаточностью данных. Тегасерод — агонист 5-HT4 пресинаптических рецепторов [14] с преимущественной стимуляцией перистальтической активности толстой кишки. Teгасерод улучшает консистенцию кала и способствует появлению позывов к дефекации у пациентов с хроническим запором. Однако согласно проведенным в 2007 году по инициативе FDA 29 рандомизированным, контролируемым исследованиям с коротким периодом наблюдения (1–3 месяца) тегасерод повышает риск кардиоваскулярных событий (в т. ч. стенокардии), в результате чего этот препарат был полностью изъят с американского фармацевтического рынка в апреле 2008 года. В настоящее время из препаратов этой подгруппы применяются также алосетрон и рамосетрон (антагонисты 5-HT3-рецепторов) с более хорошим профилем безопасности. Тем не менее окончательно говорить о высоком профиле безопасности средств этой подгруппы пока еще рано.
Бетанехол — агонист мускариновых рецепторов повышает давление нижнего пищеводного сфинктера, координирует сокращения дна и антрума, ускоряя опорожнение желудка [15]. Однако применение бетанехола ограничено только случаями рефрактерного к стандартной терапии гастропареза ввиду высокой частоты побочных эффектов: абдоминальная боль, бронхоспазм, дизурия, повышение артериального давления и пр.
Агонисты рецепторов мотилина. Полипептидный гормон мотилин вырабатывается в дистальном отделе желудка и двенадцатиперстной кишке, способствует повышению давления нижнего пищеводного сфинктера и повышает амплитуду перистальтических сокращений антрума, стимулируя опорожнение желудка. Антибиотик из группы макролидов эритромицин обладает прокинетической активностью как агонист рецепторов мотилина. Интересно, что эритромицин способствует опорожнению желудка и после ваготомии, а также после антрэктомии [16]. Однако в качестве прокинетика эритромицин вряд ли найдет свою терапевтическую нишу, и дело здесь не только в антибактериальном действии препарата. Эритромицин при длительном приеме (месяц и долее) в 2 раза повышает риск смертности, ассоциированной с нарушением сердечной проводимости [17]. Подобный эритромицину, хотя и менее выраженный эффект в отношении рецепторов мотилина был позднее описан и для других макролидов — азитромицина и кларитромицина. Однако, как и эритромицин, эти антибактериальные средства вряд ли когда-либо найдут применение в практике врача в качестве самостоятельных прокинетиков. Вместе с тем эти препараты дали толчок для синтеза новых молекул с агонистической активностью по отношению к рецепторам мотилина. Один из наиболее перспективных препаратов этой подгруппы — атилмотин [18] продемонстрировал влияние на ускорение опорожнения как жидкой, так и твердой пищи в исследованиях с участием здоровых добровольцев, а также у лиц с диабетическим гастропарезом. Изучение эффективности и безопасности длительного применения атилмотина, как и исследования по созданию новых средств-агонистов мотилина, продолжается. Так, в качестве одного из перспективных средств этой подгруппы прокинетиков изучаются эффекты грелина [19] — нейрогуморального нейротрансмиттера, секретируемого слизистой оболочкой желудка. Грелин относится к физиологическим стимуляторам моторики пищеварительного тракта и структурно связан с мотилином, оказывает прокинетическое действие с нормализацией эвакуации содержимого желудка у пациентов как с диабетическим, так и идиопатическим гастропарезом.
Исследователи продолжают активное изучение новых средств с направленной селективной прокинетической активностью [20], среди которых физостигмин и неостигмин — агонисты мускариновых рецепторов, стимулирующие деятельную активность кишечника и лишь незначительно улучшающие опорожнение желудка; ускоряющие желудочный транзит антагонисты рецепторов холецистокинина локсиглумид и декслоксиглумид, а также ингибитор фосфодиэстеразы-5 силденафил; альфа-2 агонист (адреномодулятор) клонидин, нормализующий эвакуацию содержимого желудка при функциональной диспепсии (постпрандиальный дистресс-синдром), замедляющий кишечный транзит со снижением висцеральной гиперчувствительности толстой кишки.
Широкий спектр показаний, при которых эффективно назначение прокинеков, а также особенности каждой из подгрупп прокинетиков (различные механизмы прокинетического влияния, профиль безопасности, преимущественная активность в отношении верхнего или нижнего этажа пищеварительного тракта) позволяют врачу в каждом клиническом случае выбрать наиболее эффективный и безопасный прокинетик.
По вопросам литературы обращайтесь в редакцию.
М. А. Ливзан, доктор медицинских наук, профессор
ГОУ ВПО «Омская государственная медицинская академия Росздрава», Омск
_575.gif)